Бронхиальная астма
Бронхиальная астма у детей – заболевание, развивающееся на основе хронического воспаления бронхов, характеризующееся периодически возникающими приступами затрудненного дыхания или удушья в результате распространенной бронхиальной обструкции, обусловленной сужением бронхов, гиперсекрецией слизи, отеком стенки бронхов.
Бронхиальная астма регистрируется в 5-10 % среди детского населения. В последние два, три десятилетия распространенность бронхиальной астмы у детей увеличилась.
Факторы риска развития бронхиальной астмы у детей многообразны. Предрасполагающими факторами могут быть атопия, гиперреактивность бронхов, наследственность.
У детей в 80 % случаев выявляется атопия, которая представляет собой способность организма к выработке повышенного количества IgE в ответ на воздействие аллергенов окружающей среды. Распространенность бронхиальной астмы у детей бывает чаще при высоком уровне IgE.
У детей чаще встречается гиперреактивность бронхов, при которой бронхиальная обструкция развивается в ответ на воздействие аллергенов. Способность к выработке повышенного количества IgE находится под генетическим контролем. Заболеваемость бронхиальной астмой ребенка от родителей, имеющих признаки атопии, чаще, чем заболеваемость ребенка от родителей, ее не имеющих.
В раннем детском возрасте бронхиальная астма встречается чаще у мальчиков, чем у девочек.
Причинные факторы . Происходит сенсибилизация дыхательных путей различными аллергенами, которые приводят клинически к манифестации бронхиальной астмы, а улучшение состояния ребенка наступает после элиминации причинно-значимого аллергена.
В различные возрастные периоды причины возникновения бронхиальной астмы различны. В возрасте до 1 года чаще астматическое состояние возникает при пищевой аллергии. В возрасте после 1 года имеют значение бытовые, эпидермальные и грибковые аллергены. В 3–4 года возрастает роль пыльцевой сенсибилизации. В последние годы возрастает сенсибилизация к химическим веществам. Бронхиальная астма у детей раннего возраста часто развивается при употреблении в пищу коровьего молока, рыбы, яиц, орехов, шоколада, клубники.
Бронхиальная астма, связанная с пищевой сенсибилизацией, характеризуется отсутствием связи приступов с сезонностью и сопровождается нарушениями со стороны желудочно-кишечного тракта.
В формировании бытовой аллергии играют роль клещи домашней пыли – клещи пироглифы Dermatophagoioles pferohyssimus, Dermatophagoioles tarinae и др. Клещи находятся в коврах, домашней обуви, мягкой мебели, под плинтусами. Для развития и размножения клещей необходима влажность выше 55 % и температура воздуха 22–26 °C.
У 70 % детей с бронхиальной астмой выявляется клещевая аллергия. При клещевой бронхиальной астме обострения возникают в весенне-осенний период, особенно в ночное время суток.
Источником эпидермальных аллергенов являются пух, перо, шерсть, перхоть, экскременты, слюна животных, а также насекомые (тараканы), корм для рыбок. Аллергеном кошки является feli, который находится в шерсти, а также секрет сальных желез, слюны и мочи кошки.
Аллергены собаки выделены из шерсти, слюны и эпителия. Следует отметить, что даже после удаления животных из дома, аллергены сохраняются в течение нескольких лет.
Наиболее частой причиной являются аллергены тараканов.
К грибковым аллергенам относятся плесневые и дрожжевые грибы. Они содержатся как внутри помещений, так и во внешней среде.
Обострение бронхиальной астмы в этих случаях наблюдается в осенне-зимний период, иногда круглогодично, когда ребенок находится в сырых, плохо проветриваемых помещениях или посещает их. В этих случаях отмечается тяжелое течение, частые рецидивы и короткие ремиссии.
При пыльцевой бронхиальной астме аллергенами являются три группы растений: деревья и кустарники, злаковые травы, сорные травы. В связи со сроками цветения обострения отмечаются в апреле-мае, июне-августе и в августе-октябре.
Приступы удушья у детей могут быть связаны с лекарственной аллергией на такие медикаменты: антибиотики пенициллинового ряда, сульфаниламиды, витамины, аспирин и другие нестероидные противовоспалительные препараты, при их введении и загрязнении окружающей среды.
Ряд промышленных химических веществ могут обладать аллергенным действием. Это присуще хрому, никелю, марганцу, формальдегиду, под воздействием загрязнения атмосферного воздуха.
К факторам, повышающим риск развития бронхиальной астмы у детей, относятся:
1) частые вирусные респираторные инфекции;
2) патологическое течение беременности матери;
3) недоношенность;
4) нерациональное питание;
5) атопический дерматит;
6) табакокурение;
7) загрязнение окружающей среды.
Способствующими факторами для развития бронхиальной астмы при загрязнении окружающей средыявляются:
1) индустриальный смог;
2) фотохимический смог за счет двуокиси азота, озона;
3) химические аллергены при производстве формальдегида, ароматических углеводородов;
4) белково-витаминные концентрации;
5) пестициды и гербициды.
У детей отмечается более высокая заболеваемость, если они проживают вблизи промышленных зон, автомагистралей.
На возникновение и течение бронхиальной астмы влияет курение. Респираторный тракт ребенка подвергается интенсивному воздействию табачного дыма. У детей, как пассивных курильщиков, выявляется сенсибилизация к экстракту табака, входящего в состав сигарет. Дети чаще болеют респираторными заболеваниями, у них выявляется повышение бронхиальной гиперреактивности.
Факторы, вызывающие обострение бронхиальной астмы . У детей могут стимулировать воспаление в бронхах и провоцировать острый бронхоспазм:
1) физическая нагрузка;
2) психоэмоциональная нагрузка;
3) изменение метеоситуации;
4) загрязнение воздуха;
5) контакт с аллергенами;
6) респираторно-вирусные инфекции.
Механизмы развития заболевания . Механизмы развития бронхиальной астмы сложны. Он состоит в формировании гиперреактивности бронхов, проявляющейся спазмом бронхиальных мышц, отеком слизистой оболочки бронхов вследствие повышенной сосудистой проницаемости и гиперсекреции слизи, что приводит к бронхиальной обструкции и развитию удушья. Бронхиальная обструкция может возникать как в результате аллергической реакции, так и в ответ на неспецифические раздражители.
В развитии бронхиальной астмы различают III стадии аллергического процесса.
I стадия – иммунологическая. В этой стадии происходит взаимодействие антигена с антителом или сенсибилизированным Т-лимфоцитом в области клеток «шокового» органа, активация тканевых и сывороточных ферментов.
II стадия – патохимическая. В этой стадии происходит освобождение из клеток гистамина, брадикинина, ацетилхолина, простагландинов.
III стадия – патофизиологическая: бронхоспазм, отек бронхов и гиперреакция железистого аппарата бронхов, вызывающие обструкцию, эмфизему легких, нарушение бронхиальной проходимости.
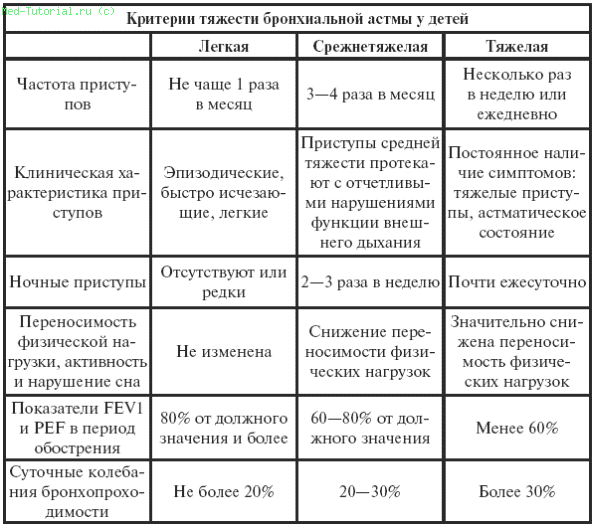
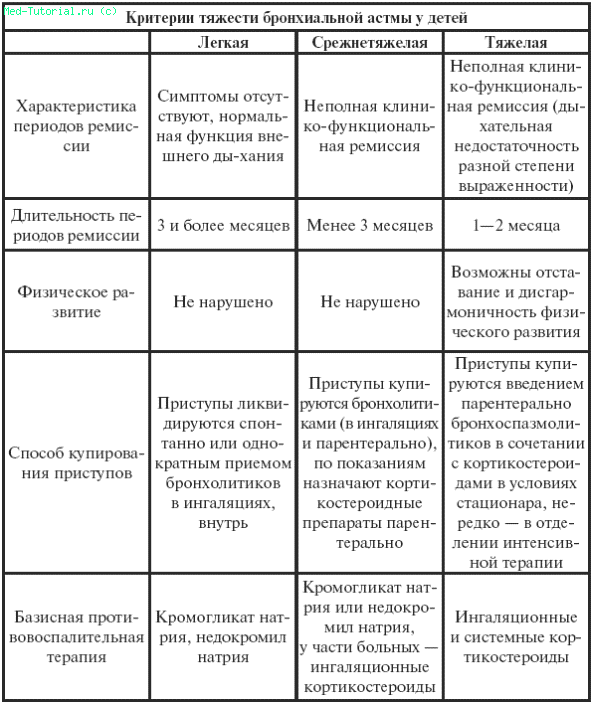
Клиника . С практической точки зрения различают легкую, среднетяжелую и тяжелую формы. Степень тяжести определяет лечебную тактику и план ведения больного.
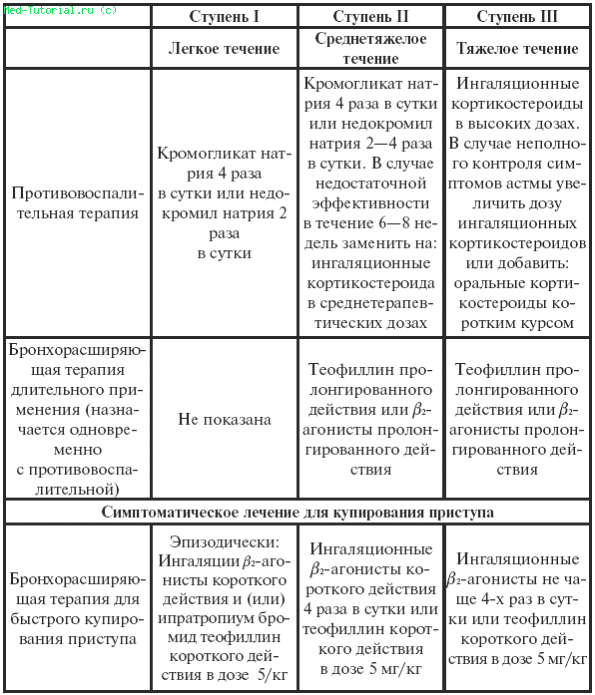
Таблица 36
Лечебная тактика и план ведения больного (Национальная программа «Бронхиальная астма у детей», 1997 год)
Окончание табл. 36
Развернутый приступ бронхиальной астмы включает в себя:
1) период предвестников;
2) приступ удушья;
3) послеприступный период.
Период предвестников длится от нескольких минут до нескольких часов, изменяется поведение ребенка, появляется слабость, головная боль, зуд, покалывание, изменяется восприятие запахов. Приступ удушья развивается остро, и резко ухудшается состояние, дыхание становится затрудненным, появляются головная боль, кашель с невозможностью отхаркивать мокроту. Кожа становится бледной с акроцианозом, а затем – цианозом.
Возникает экспираторная одышка, при которой в акте дыхания принимает участие вспомогательная мускулатура, вздутие грудной клетки. По всем легочным долям прослушиваются сухие, свистящие хрипы, тоны сердца глухие. Продолжительность приступа может быть различной, в тяжелых случаях развивается астматический статус. У детей младшего возраста в связи с большей васкуляризацией бронхов экссудативные изменения преобладают над бронхоспазмом, возникает тяжелый приступ, у детей этого возраста кашель более продолжительный. Послеприступный период продолжается от нескольких часов до нескольких недель. У ребенка появляется нормальное самочувствие.
Таблица 37
Критерии оценки тяжести приступа бронжиальной астмы у детей
Астматическое состояние делится на III стадии.
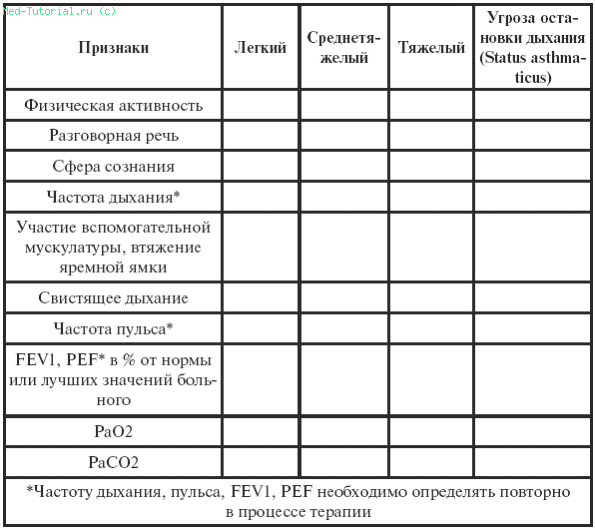
I стадия. Выражена бронхиальная проходимость. Количество хрипов незначительно, но на расстоянии выслушиваются звучные дыхательные шумы, отмечаются бледность, цианоз, тахикардия.
II стадия. Выявляется тотальная легочная обструкция. Шумы при аускультации не прослушиваются, снижается экскурсия грудной клетки, бледный цианоз, тахикардия, частый малый пульс, гипотония, нарастают психоэмоциональные расстройства.
III стадия. Гипоксемическая кома, которая характеризуется гипоксемией и гиперкапнией. Состояние крайне тяжелое, сознание отсутствует. Дыхание частое, поверхностное. Пульс нитевидный, коллапс.
Осложнениями могут быть:
1) ателектазы;
2) пневмония;
3) подкожная эмфизема;
4) спонтанный пневмоторакс;
5) легочно-сердечная недостаточность;
6) пневмосклероз.
Диагностика . Клиническая диагностика бронхиальной астмы у детей базируется на выявлении таких симптомов, как экспираторная одышка, свистящее дыхание, чувство давления в груди, кашель.
При лабораторном обследовании в крови повышено содержание иммуноглобулина Е, гистамина, брадикинина. В клиническом анализе крови – эозинофилия. В мокроте определяются спирали Курмана и кристаллы Шарко-Лейдена. Рентгенологически определяется эмфизема легких, которая может быть и при длительном течении заболевания
Лечение . Лечение астмы зависит от стадии заболевания. Лечение должно быть длительным, упорным и комплексным. Оно направлено на достижение ремиссии болезни и профилактику ее обострения, недопущение приступов удушья. Различают специфические методы лечения и неспецифические методы. Специфические методы направлены на ограничение и прекращение контакта с выявленными аллергенами и гипосенсибилизацию путем специфической иммунотерапии.
Лечение астматического статуса . Лечение и все реанимационные мероприятия проводятся в условиях стационара.
В I стадии – глюкокортикоиды, вводимые перорально или парэнтерально, внутривенно капельно эуфиллин, 2,4 % вводится внутримышечно 10 мг/кг/сут, назначаются глюкокортикоиды в возрастной дозировке (преднизолон 2–5 мг /кг/сут), антигистаминные препараты. Назначается инфузионная терапия (физраствор, 5 мл 10 %-ной глюкозы, неогемодез, реополиглюкин, гидрокарбонта натрия 4 %-ного). Проводится вибрационный массаж грудной клетки. Инфузионная терапия осуществляется умеренно, в связи с внутривенным введением эуфиллина.
Во II стадии проводится борьба с гипоксией. Назначается гелиево-кислородная смесь, бронхоскопический лаваж, промывание бронхиального дерева раствором хлорида натрия под наркозом. Дозу глюкокортикоидов повышают (60-90-200 мг каждые 90 мин) в зависимости от возраста, стартовой дозы и т. д. Если отсутствует эффект, то показана ИВЛ (искусственная вентиляция легких) с отсасыванием мокроты.
В III стадии на фоне искусственной вентиляции легких осуществляется очищение бронхиального дерева через интубационную трубку в сочетании с активным массажем грудной клетки.
После выведения из астматического состояния дозу глюкокортикоидов снижают вдвое, а затем уменьшают до поддерживающей. В период ремиссии проводится гипосенсибилизирующая терапия, санация очагов инфекции, лечебная физкультура, физиотерапия, санаторно-курортное лечение.
Основные цели лечения:
1) предупреждение беспокоящих ребенка проявлений бронхиальной обструкции – приступов удушья, одышки при физической нагрузке, кашля, ночного диспноэ;
2) эффективно купировать возникающие эпизоды преходящей бронхиальной обструкции;
3) поддерживать функцию легких.
Основные задачи лечения
1. Исключить воздействие на организм ребенка «внешнего аллергена». При пыльцевой аллергии предлагается переезд в иную местность на период цветения растений. При пищевой аллергии требуется строгое соблюдение элиминационной диеты.
2. В период ремиссии проводится специфическая десенсибилизация, для чего больному вводят постепенно возрастающие дозы «виновного» аллергена, что ослабляет реакцию организма путем индукции образования блокирующих антител, относящихся к классу иммуноглобулинов G.
3. Предупреждение секреции тучными клетками биологически активных веществ при фиксации комплекса антиген-антитело. Таким стабилизирующим влиянием обладает недокромил и др., а также адреномиметики, ингибиторы фосфодиэстеразы и антагонисты кальция.
4. Предупреждение воздействия на гиперреактивные воздухопроводящие пути триггеров: холодного воздуха, табачного дыма и других.
5. Санация любых очагов инфекции.
6. Купирование воспаления дыхательных путей.
Лечение астмы у детей требует обязательного сотрудничества между родителями и больным ребенком, между ребенком и врачом, между родителями и врачом. Ребенок должен научиться жить с астмой, контролировать ее. Родители – главные помощники в лечении астмы у детей, особенно раннего возраста. Родители должны увидеть ранние стадии спазма и воспаления и ликвидировать их. Лечение астмы у детей то же, что и у взрослых. Ребенок нуждается в удержании под контролем процесса воспаления дыхательный путей. Это особенно необходимо при тяжелом и среднетяжелом течении астмы. Если у него отмечаются приступы редко, ему необходимы лекарства, снимающие приступы. Лекарства, принимаемые детьми для лечения астмы, должны дозироваться в соответствии с возрастом. Обычно применяются специальные устройства для вдыхания противоастматических средств. Лечение бронхиальной астмы глюкокортикостероидными препаратами у детей является сложным процессом. К препаратам этой группы относятся глюкорт, альдецин, пульмикорт, бекотид, бекломет и другие лекарства последних поколений в виде дозированных аэрозолей, а также в виде таблеток: дексаметазон, целестон, полькортолон, преднизолон. Все они небезопасны из-за побочных эффектов. Глюкокортикоиды применяются для длительной профилактики приступов. Однако мощным безопасным и современным средством при лечении бронхиальной астмы все-таки являются дозированные аэрозоли. Качество жизни больных астмой в результате использования ингаляционных кортикостероидов существенно улучшается. Доза гормональных препаратов, получаемых ребенком с помощью ингаляторов, в десять раз меньше, чем при приеме таблетизированных форм. Такое применение безопасно в связи с тем, что они оказывают местное воздействие и не поступают в кровь и не действуют на функции таблетизированных форм. Ингаляционные стероиды предназначены для ежедневного применения только при очень тяжелом течении болезни и неэффективны при приступе удушья.
Существует два правила приема ингаляционных стероидных препаратов:
1) ингалирование лекарств с помощью спейсера;
2) после ингаляции необходимо прополоскать рот и горло водой.
При тяжелом течении болезни, если ингаляционные препараты не оказывают эффекта, назначаются таблетизированные стероидные препараты. В этих случаях таблетизированные препараты назначаются на 7-14 день. В первые 2–3 дня назначается максимальная доза препарата, а с 3–4 дня дозу по состоянию снижают, затем продолжается прием ингаляционных стероидов.
Таблица 38
Суточные дозы ингаляционных кортикостероидных препаратов у детей
Ингаляционные глюкокортикоиды служат основой терапии бронхиальной астмы, но в настоящее время доказано, что добавление ингаляционного β2-агониста длительного действия сальметерола тоже дает положительный эффект. Это обеспечивает лучший контроль в отношении сокращения симптомов, улучшение частоты обострений у детей с бронхиальной астмой, у детей старшего возраста и позволяет не повышать дозы гормональных препаратов. В настоящее время применяется один ингалятор для базисной терапии и для купирования симптомов. Обычно назначают комбинированный ингалятор 1–2 раза в день в дозе, соответствующей тяжести бронхиальной астмы, и β2-агонист короткого действия типа сальбутамола.
В настоящее время разработан примерный алгоритм применения лекарственных средств в приступном периоде бронхиальной астмы у детей. В начальном периоде лечения в стационаре проводится оксигенотерапия через маску, проводятся ингаляции β2-агонистов короткого действия (1–2 дозы через спейсер или небулайзер каждые 20 мин в течение часа).
Если наступает улучшение, продолжают применять ингаляционные β2-адреномиметики 2–4 раза в сутки в течение недели, прием внутрь препаратов эуфиллина, последующую базисную терапию. В случае отсутствия улучшения назначается оксигенотерапия, β2-агонисты парентерально или небулайзер, спейсер, вводится эуфиллин внутривенно капельно, по показаниям – адреналин подкожно, внутримышечно, кортикостероиды парэнтерально каждые 6 ч. В случае если и при этом нет улучшения, больного помещают в отделение интенсивной терапии, где проводятся коксигенотерапия, спазмолитическое лечение, возможно ИВЛ, лечебная бронхоскопия, даются кортикостероиды внутрь.
Если наступает улучшение, парэнтеральная терапия кортикостероидами продолжается в течение нескольких дней с постепенной отменой и переходом на ингаляционные кортикостероиды с добавлением пролонгированных метилксантинов.
В настоящее время применяют ступенчатый подход при длительном лечении бронхиальной астмы.
Таблица 39
Ступенчатый подход при лечении бронхиальной астмы
Широко применяются и немедикаментозные методы лечения бронхиальной астмы у детей. Совместное применение медикаментозных и немедикаментозных методов лечения дает наибольший эффект в лечении астмы. К ним относятся диетотерапия, дыхательная гимнастика, закаливание, массаж, иглорефлексотерапия, физиотерапия.
Назначается гипоаллергенная диета.
Для детей первого года жизни оптимальным является грудное вскармливание.
Диетический режим при бронхиальной астме должен строиться на принципах элиминации, детоксикации, динамичности и сбалансированности.
При всех формах бронхиальной астмы ограничивают продукты, содержащие гистамин. К ним относятся консервы, помидоры, шпинат, копчености.
Всем детям с бронхиальной астмой назначается индивидуальная диета с исключением аллергенных продуктов.
Широко применяется респираторная терапия путем лечения дыхания через дыхание. Это повышает устойчивость больного ребенка к гипоксическим и гиперкапническим состояниям.
Самой простой является тренировка дыхания с помощью создания положительного давления в конце выдоха. Это упражнение проводится в любом периоде болезни. Для этого используются выдыхание воздуха в сосуд, наполненный водой, через коктейльную трубочку. После глубокого вдоха ребенок медленно выдыхает воздух. Это упражнение повторяют 4–5 раз в день по 10–15 мин.
Для увеличения образования мокроты и улучшения ее отхождения используют диафрагмальное дыхание – упражнение с форсированным выдохом.
Кроме этого, применяется специальный комплекс статических и динамических упражнений, циклические методы физкультуры в периоде ремиссии: ходьба с пробежками – «ходьба-бег-ходьба».
Детям проводятся массаж и вибромассаж, лечебная физкультура, спленетерапия и горноклиматическое лечение. Из физиотерапевтических средств применяются магнитотерапия, лазерная терапия.
Многие процессы, возникающие у детей с бронхиальной астмой, нормализует иглоукалывание.
При бронхиальной астме применяется и фитотерапия, но только после консультации с лечащим врачом. Назначаются сборы, содержащие алтей лекарственный, девясил высокий, зверобой, календулу, большой подорожник, солодку голую.