9.5. ЭТИОЛОГИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА[4]
Подавляющее большинство заболеваний пародонта носит воспалительный характер, включая так называемый юношеский (ювенильный) пародонтит (в возрасте 11–21 года); исключение составляют редко встречающиеся особые формы типа дистрофии (атрофии).
Заболевания пародонта могут развиваться пол влиянием как местных причин (микроорганизмы зубного налета, окклюзионная травма), так и сочетанного воздействия местных и общих (эндогенных) факторов на фоне изменений реактивности организма. Наибольшее значение в этиологии заболеваний пародонта имеют следующие факторы:
? состояние и продукты обмена в зубной бляшке и зубном налете;
? факторы полости рта, способные усиливать или ослаблять патогенетический потенциал микроорганизмов и продуктов их обмена;
? общие факторы, регулирующие метаболизм тканей полости рта, от которых зависит реакция на патогенные воздействия.
Воспаление десен возникает под влиянием продуктов жизнедеятельности микроорганизмов микробной бляшки (мягкого зубного налета), которые состоят из эндотоксинов, экзоэнзимов и антигенного материала. Бактерии, их способность проникать в ткани, количество и видовой состав, а также конечные продукты их обмена, с одной стороны, и резистентность тканей и организма в целом — с другой, определяют характер (катаральный, язвенный, гипертрофический) и тяжесть гингивита, а также возникновение пародонтита и быстроту деструкции пародонтальных тканей.
Уместным будет здесь привести определение воспаления одного из крупнейших авторитетов в этой области академика А. М. Чернуха «Воспаление — это возникшая в ходе эволюции реакция живых тканей на местные повреждения; она состоит из сложных поэтапных изменений микроциркуляторного русла, системы крови и соединительной ткани, которые направлены в конечном итоге на изоляцию и устранение поврежденного агента и восстановление (или замещение) поврежденных тканей».
Таким образом, возникновение воспаления является первой, иногда краткой реакцией на субклеточное повреждение тканей. Эта реакция кончается длительной деструкцией ткани или полным заживлением. Вполне вероятно, что бактериальные ферменты и токсины могут непосредственно повредить ткани пародонта.
Полость рта принято рассматривать как сбалансированную биологическую систему, являющуюся следствием взаимной адаптации макро- и микроорганизмов. Нормальная микрофлора является для организма «биологическим барьером», препятствующим размножению случайной микрофлоры, в том числе патогенной. Помимо этого, аутофлора является постоянным стимулятором локального иммунитета. Это эволюционно выработанный, физиологически необходимый способ защиты от инфекции.
В полости рта насчитывается более 200 различных видов микроорганизмов. В составе микрофлоры аэробные и анаэробные бактерии, дрожжеподобные грибы, микоплазмы, простейшие. Концентрация аэробных и факультативных бактерий в I мл слюны составляет 10-7, анаэробных — 10-8. Соответственно различают постоянную (резидентную) и случайную (транзиторную) микрофлору ротовой полости. К постоянной микрофлоре полости рта принадлежат стрептококки (?- и ?-типов), сапрофитные нейссерии, лактобактерии, дифтероиды, анаэробные кокки (пептострептококки и пептококки), вейлонеллы. бактероиды, фузобактерии, лептотрихии, спирохеты и другие. К непостоянной, или случайной, микрофлоре относят грамотрицательные аэробные бактерии, в том числе E.coli, Klebsiella, Pseudomonas, Proteus, грамположительные бациллы и анаэробные клостридии.
При относительном постоянстве в количестве и составе микрофлоры наблюдаются их колебания, обусловленные гигиеническим уходом за полостью рта, возрастом, состоянием зубов и другими факторами. Следует также иметь в виду, что в полости рта микроорганизмы распределяются неравномерно. Наибольшая концентрация бактерий отмечается на корне языка, поверхности десневого края и в зубном налете (бляшке). В последнем насчитывают до 10-11 микроорганизмов в 1 г. Облигатные анаэробные виды преобладают в основном в поддесневой бляшке, а факультативные и микроаэрофилы — в наддесневой.
Роль микроорганизмов в этиологии гингивита и пародонтита. Причиной большинства основных форм гингивита и пародонтита являются бактерии, которые прикрепляются к поверхности зуба над и ниже края десны, образуя основу бактериальной бляшки.
Зубная бляшка образуется при адсорбции на поверхности в области десневой борозды микроорганизмов из ротовой жидкости. Такая адсорбция осуществляется за счет специфических гелеобразных высокоадгезивных нерастворимых в воде полимеров глюкозы, декстранов, а также белков слюны. В результате размножения микроорганизмов и синтеза ими внутриклеточного гликогеноамилопектина и внеклеточно — углеводно-резервных соединений из поступающих в полость рта с пищей рафинированных углеводов (сахарозы, глюкозы, фруктозы и др.) образуется мягкий зубной налет (зубная бляшка). По мере аккумуляции микробных отложений возникает воспаление десны При этом изменяется соотношение микроорганизмов, образующих бляшку. В начале это преимущественно образующие колонии грамположительные бактерии (стрептококки, актиномицеты), при дальнейшем росте бляшки появляются грамотрицательные кокки, а также грамположительные и грамотрицательные палочки и нитевидные формы. К основным возбудителям воспалительного процесса в пародонте относятся грамнегативные анаэробы: бактероиды, фузобактерии, спирохеты, актиномицеты, анаэробные кокки:
| Главные виды бактерий, ассоциированные с заболеваниями пародонта | |
|---|---|
| Острый язвенный гингивит | Bact. intermedius, Spirochetes |
| Гингивит беременных | Bact. intermedius |
| Пародонтит взрослых | Bact. gingivalis, Bact. intermedius |
| Локализованный юношеский пародонтит | Actinobacillus actinomycetem-comitans, Capnocytophaga |
| Быстро прогрессирующий пародонтит (БПП) взрослых (до 35 лет) | Actinobacillus actinomycetem-comitans, Bact. intermedius. Fusobacterium nucleatum, Peptostreptococcus micros, Treponema denticola, Selenomonas species |
Важнейшими бактериальными продуктами, которые вызывают воспаление и деструкцию пародонтальных тканей, являются хемотоксины, а также антигены и митогены. В результате их действия появляется усиленная миграция лейкоцитов в десневую борозду. За счет отека ослабевает эпителиальное сцепление с зубом, что позволяет грамположительным бактериям и продуктам их распада проникать в апикальном направлении в области дна зубодесневого соединения.
Образующиеся в процессе жизнедеятельности микроорганизмов большое число гидролитических ферментов, включая такие протеолитические ферменты, как коллагеназы, эластазы, приводят к разрушению и повреждению клеток десны, коллагеновых волокон пародонта, вызывая их деструкцию, образование в дальнейшем пародонтального кармана.
Прогрессирующие воспалительные изменения в пародонте протекают одновременно с дистрофическими или превалируют над ними. В зависимости от этого в тканях размножаются преимущественно те или иные виды микроорганизмов. В начале развития процесса в пародонтальных карманах преобладает факультативно-анаэробная или аэробная микрофлора, в последующем ее вытесняют облигатные анаэробы.
Характер микрофлоры десневой бороздки и пародонтального кармана при микроскопическом исследовании нативных препаратов выглядит следующим образом:
| Норма | Гингивит | Пародонтит |
|---|---|---|
| Преобладание кокковой миклофлоры, малые неподвижные палочки | Увеличение числа неподвижных и подвижных палочек, снижение количества кокков | Преимущество подвижных палочковидных и известных форм бактерий |
Что касается локализованного юношеского пародонтита (ЛЮП), то его происхождение связывают с влиянием определенных микроорганизмов, в частности Actinobacillus actinomycetemcomitans.
Быстропрогрессирующие и устойчивые к лечению формы пародонтита (БПП) характеризуются повышенным содержанием в пародонтальном кармане, кроме вышеуказанного возбудителя, и других микроорганизмов.
Особое значение в этиологии заболеваний пародонта имеет слюна: ее состав и свойства, скорость выделения, влияющая на накопление зубного налета, ее химический состав, кальцификация.
В смешанной слюне обнаружено более 60 ферментов, роль которых в развитии заболеваний пародонта полностью не выяснена, но несомненна. В частности, описана патология пародонта, развивающаяся вследствие недостатка каталазы в слюне и тканях.
Считают, что полиморфно-ядерные лейкоциты, помимо выделения повреждающих ткани ферментов, с помощью хемотаксической реакции привлекают в область поражения иммунокомпетентные клетки. Хемотаксис вызывается бактериальной бляшкой, так же как и механизм реакции антиген — антитело и комплементарной системы. В этой реакции действуют и клеточный, и гуморальный иммунный механизмы. Результаты изучения роли патогенных стафилококков в воспалительных реакциях при заболеваниях пародонта с помощью обнаружения антител к патогенным стафилококкам и другой микрофлоре пародонтального кармана позволяют связать гнойно-воспалительную реакцию с действием патогенных стафилококков. В настоящее время предполагают, что не первичная биологическая активность эндотоксинов, а циркуляция вырабатываемых в ответ на них антител играет роль в изменении реакции тканей (А.И.Воложин).
Патогенная микрофлора, вегетирующая в пародонтальном кармане и зубном налете, обладая антигенными субстанциями. оказывает сенсибилизирующее действие на ткани пародонта. Это приводит к усилению интенсивности альтерации тканей и образованию тканевых аутоантигенов, а возможно, и комплекса микроорганизм + ткань. На эти антигены иммунная система реагирует по-разному. В одних случаях развивается защитный, не нарушающий гомеостаз, иммунный ответ, сохраняющийся до тех пор, пока не нарушится функциональное состояние Т- и В-лимфоцитов. В других случаях, по мере истощения супрессорной функции Т-лимфоцитов в результате хронического воздействия аутоантигенов, начинается бесконтрольная активизация иммунного ответа на антигены, что и обусловливает клиническую выраженность симптомов и «самодвижущийся» характер этого заболевания.
Влияние бляшки и зубною камня нельзя считать чисто местной причиной, ибо их образование и активность зависят от состояния реактивности организма (изменение минерального и белкового состава слюны, десневой жидкости, их ферментативной активности, иммуноглобулинов, кининовой системы и др.).
Схему развития патологического процесса в пародонте можно представить следующим образом. Инфекционные агенты выделяют бактериальные токсины (липополисахариды, липотеновую кислоту, мурамилдипептид и др.). которые активируют остеокласты. Привлеченные в очаг воспаления полиморфно-ядерные лейкоциты, тромбоциты, моноциты и образующиеся из них макрофаги выделяют простагландины, которые могут прямо активировать остеокласты, а также действуя на макрофаги, заставляют их выделять фактор, активирующий остеокласт — ФАО [Lehner, 1983]. Локальные и системные факторы в совокупности приводят к развитию пародонтита с выраженными воспалительно-деструктивными изменениями.
Таким образом, активность воспалительного процесса в пародонте характеризуется размножением микроорганизмов в пародонтальных карманах, изменением их видового состава, повышением агрессивных свойств (образование ферментов и токсинов). Процесс резорбции кости составляет основу механизмов развития пародонтита, и главную роль в разрушении тканей, видимо, играет комплемент, активация которого комплексами антиген — антитело приводит не только к усилению синтеза простагландина Е, но и резорбции костной ткани [Lehner, 1983].
Местные травматические (ятрогенные) причины. К ним относятся дефекты протезирования (глубоко продвинутая под десну коронка, базис съемного протеза, сдавливающий десневые сосочки и др.), дефекты лечения зубов (избыток амальгамы или композитного материала) и попадание мышьяковистой пасты в межзубной промежуток, влияние мономера протезов, вредное влияние неправильно сконструированных ортодонтических аппаратов.
Из причин, способствующих появлению зубного налета, необходимо указать на анатомические особенности зубов. их расположение в дуге и кариозные поражения. Эти причины могут вызвать папиллит, гингивит и, реже, более глубокие изменения пародонта (пародонтит), причем поражения в этих случаях, как правило, носят локальный характер.
Перегрузка тканей пародонта. В эксперименте и при клинических наблюдениях показано, что такая перегрузка вызывает комплекс патологических изменений в тканях пародонта с преобладанием воспалительных и дистрофических явлений. Деструктивно-воспалительные процессы вследствие перегрузки пародонта могут наблюдаться при различных аномалиях прикуса (глубокий прикус, глубокое резцовое перекрытие, открытый, прогнатический, прогенический прикус и др.); аномалиях положения зубов (скученность зубов); при ранней потере больших и малых коренных зубов; после удаления большого количества зубов (постэкстракционные передвижения зубов); при неправильном определении показаний к мостовидному, особенно металлокерамическому, протезированию, неправильно сформированном преддверии полости рта; после хейло- и уранопластики; при бруксизме (ночное скрежетание зубами) и др. (рис. 9.10).
Характерно, что ткани пародонта (связочный аппарат, кость) сравнительно хорошо переносят вертикальную перегрузку и значительно хуже — горизонтальную. Превышение адаптационных возможностей пародонта может привести к нарушению его кровоснабжения и в дальнейшем к резорбции костной ткани. При этом морфологическим субстратом развивающихся в пародонте дистрофических изменений является тромбоз сосудов кости с последующим развитием ее резорбции.
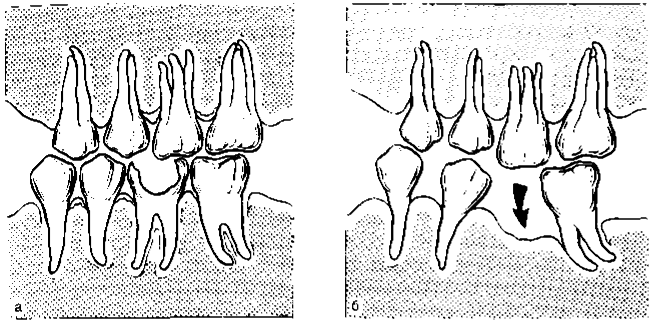
Рис. 9.10. Изменения пародонта вследствие постэкстракционного перемещения зубов (схема), а — до потери первого нижнего большого коренного зуба; б — после его потери
При травматических поражениях пародонта клинические и рентгенологические изменения локализуются обычно в области отдельных зубов или их групп.
Перегрузка пародонта всегда сопровождается изменениями гидростатического давления крови в сосудах, крово-и лимфотока и как следствие этого появлением гемо- и лимфостазов, нарушением проницаемости гистогематических барьеров, периваскулярным отеком, диапедезом форменных элементов крови, агрегацией эритроцитов, эмболией и, наконец, тромбозом сосудов. Развиваются явления гипоксии. Все это не может не сказываться на структуре пародонтальных тканей. Вследствие нарушения фиксирующей функции коллагеновых и эластичных волокон периодонта возникает подвижность зубов, их болезненность при накусывании.
В дальнейшем отмечается не только набухание, но и деструкция коллагеновых волокон. Нарушается целостность эпителиального покрова в области зубодесневого соединения, образуется пародонтальный карман с последующим наслоением воспалительных явлений за счет микрофлоры десневой щели, пролиферации и погружного роста эпителия. В дальнейшем воспалительно-деструктивный процесс приводит к резорбции межзубных костных перегородок.
Таким образом, травматические факторы могут быть причиной локализованных, но не генерализованных поражений пародонта, при этом нельзя исключать и влияние микробного фактора. Вместе с тем перегрузка отдельных зубов в значительной степени усугубляет течение генерализованных процессов, усиливая воспалительные и атрофически-резорбтивные процессы в околозубных тканях, способствуя разрушению связочного аппарата и в конечном итоге элиминации зубов.
Функциональная недостаточность (гипофункция) может быть причиной заболевания пародонта. Недостаточность функции жевания является порождением современной цивилизации. Тщательно обработанная, мягкая пища лишает ткани пародонта полноценной нагрузки, вследствие чего могут развиваться атрофические процессы. Кроме того, такая пища способствует образованию зубных отложений, являющихся нередко единственной причиной воспаления маргинального пародонта. При этом существенное значение имеет индивидуальная предрасположенность к заболеванию пародонта. Другой вариант функциональной недостаточности — локальная, например при отсутствии антагонистов, открытом прикусе и т. д. Недостаток функции жевательного аппарата снижает резистентность тканей пародонта к различным внешним воздействиям (микроорганизмы, травма), способствует одновременно отложению зубного камня. Гипофункция уменьшает местный кровоток и, следовательно, метаболизм тканей — это способствует развитию деструктивных процессов в пародонте [Логинова Н. К., Воложин А. И., 1994].
Недогрузка группы зубов или отдельных зубов неблагоприятно влияет на пародонт. Согласно теории функциональной патологии зубочелюстной системы В. Ю. Курляндского, в результате частичной адентии пародонт распадается на отдельные разнофункционирующие звенья (функционирующий центр, травматический узел и нефункционирующее звено). В пародонте разнофункционирующих, в том числе и недогруженных, зубов развиваются деструктивные процессы, однако и в этом процессе принимают участие микроорганизмы (их ферменты, токсины) зубной бляшки.
Гиперфункция пародонта при частичной потере зубов повышает их подвижность и при неблагоприятном соотношении длины коронки и корня возникает чаще всего как осложнение пародонтита, т. е. на фоне уже имеющихся воспалительно-деструктивных изменении. Естественно перегрузка опорных тканей сопровождается сосудистыми нарушениями в микроциркуляторном русле тканей пародонта.
Влияние бляшки и зубного камня на ткани пародонта нельзя считать чисто местной причиной, ибо их образование и активность зависят от состояния реактивности организма (изменение минерального и белкового состава слюны, десневой жидкости, их ферментативной активности, содержания иммуноглобулинов, кининовой системы и т. д.). Деление на общие и местные факторы носит искусственный характер, ибо, хотя местные факторы могут выступать в качестве организаторов патологического процесса, ответная реакция организма всегда определяется общими факторами.
Общие факторы. Дефицит витаминов. Большое значение для понимания патогенеза заболеваний пародонта имеют работы по изучению влияния дефицита витаминов С, В1, А, Е на состояние его тканей. Гипо- и авитаминоз С сопровождаются воспалительно-деструктивными изменениями в тканях пародонта. В настоящее время имеется достаточно убедительных данных, позволяющих считать, что при дефиците витамина С в организме нарушаются процессы образования и формирования коллагеновых волокон, ткани разрыхляются, повышается проницаемость межклеточного вещества и капилляров. Деструкции подвергаются зрелые коллагеновые структуры. Кроме того, при дефиците витамина С в организме замедляется формирование костной ткани, снижается устойчивость пародонтальных тканей к инфекции [Материалы ВОЗ, 1978]. По данным I.Egelberg (1991), ежедневное назначение витамина С в дозе 450 мг (1-я группа больных) и 100 мг витамина С в сочетании с цитрусовыми биофлавоноидами (2-я группа больных) уменьшало воспаление в десневом крае.
В литературе наблюдаются данные об изменениях в тканях пародонта при дефиците в организме витаминов А и В. Витамин А играет большую роль в процессе эпителизации десны; его недостаток ведет к снижению барьерной функции десны (альтерация десневого края), способствуя тем самым ее воспалению.
При воспалительных изменениях десны содержание витамина А в сыворотке крови снижается у 75 % больных; чем сильнее выражены явления воспаления, тем ниже содержание витамина А Однако I.Egelberg (1991), изучая действие в клинике витамина В, не отметил никаких изменений индекса гингивита.
Заболевания пародонта в эксперименте при Е-авитаминозе описаны рядом авторов. При этом усиливается свободнорадикальное пероксидное окисление липидов, образуются пародонтальные карманы, атрофируется кость, изменяется сосудистая система пародонта.
Значение общей диетотерапии в качестве дополнения к лечению пародонтита остается невыясненным, кроме назначения витамина С.
Атеросклеротическое поражение сосудов. Влияние этого фактора рассматривается в свете сосудистой концепции А. И. Евдокимова, сформулированной им еще в 1939–1940 гг. А. И. Евдокимов считает пародонтоз дистрофическим процессом, развивающимся вследствие атеросклеротических изменений сосудов пародонта в результате общего или изолированного атеросклероза. Патоморфодогические исследования, проведенные автором этой теории, выявили значительные изменения в сосудистой стенке артерий пародонта (периваскулярный склероз, утолщение сосудистых стенок, особенно средней оболочки, гиалиноз, сужение просвета, вплоть до кальциноза). Эта теория признается некоторыми учеными и в настоящее время; она подтверждает известный из эпидемиологических исследований факт возрастного увеличения частоты пародонтоза и атеросклероза.
Атеросклеротические изменения сосудов пародонта несомненно могут играть существенную роль в развитии дистрофии пародонтальных тканей и прежде всего кости альвеолярных отростков челюстей, однако эта теория в связи с появлением новых данных и пересмотром холестериновой природы самого атеросклероза должна восприниматься с некоторыми поправками. В частности, по данным ВОЗ, отложение липидов во внутренней оболочке (интиме) аорты обнаружено у 100 % детей 9-летнего возраста при низком уровне холестерина в крови. Липидные полоски одинаково часто обнаруживаются у взрослых как с высоким, так и с незначительным распространением атеросклероза.
Нервно-дистрофическая природа пародонтоза. Обоснована в работах П. А. Глушкова, Д. А. Энтина, Е. Е. Платонова, П. К. Карташова, И. О. Новика, Э. Д. Бромберг и др. Известно, что атрофически-дегенеративные изменения в тканях зависят чаще всего от нарушения их питания вследствие недостаточного кровоснабжения. Однако расстройства питания могут развиться и при хорошем кровоснабжении в случае, когда сама ткань теряет способность ассимилировать приносимые питательные вещества. При этом говорят о нервно-трофических факторах расстройства питания.
Сущность трофического влияния нервной системы заключается не только в регуляции обмена в тканях, но и в сохранении структуры тканей и достижении определенной степени их дифференцировки в процессе регенерации. Поэтому нарушение трофических процессов в результате воздействия на нервные образования рефлекторно приводит к развитию патологического процесса, относящегося по своему морфофункциональному содержанию к дистрофиям.
Снижение реактивности организма. При снижении реактивности организма и, следовательно, недостаточной силе защитных и компенсаторных механизмов может наступить развитие дистрофического процесса в пародонте. Это проявляется в физико-химических сдвигах, прежде всего в не клеточных структурах — основном веществе соединительнотканных структур (ГАГ, коллагеновые волокна), что приводит к нарушению проницаемости сосудов, кровообращения, тканевой гипоксии, изменению обмена и т. д.
Гипоксия. В литературе имеются указания о появлении гипоксии в тканях паролонта при дистрофически-воспалительной форме пародонтоза. Одним из показателей, характеризующихся уровень и особенности окислительно-восстановительных процессов в тканях, является окислительно-восстановительный потенциал. Он отражает соотношение окисленных и восстановленных форм, позволяет судить об утилизации тканями кислорода в процессе метаболизма. Изучение ОВП, проведенное Е. В. Кречиной (1988), Н. К. Логиновой (1994) и др., показало снижение его при патологии пародонта, что свидетельствует о накоплении в тканях недоокисленных продуктов. По мере развития дистрофического процесса отмечено дальнейшее уменьшение ОВП. В результате снижается барьерная функция тканей пародонта и сочетанное влияние местных и общих факторов приводит к возникновению характерных для заболеваний пародонта патологических явлений (резорбция кости, гингивит, образование пародонтального кармана и др.).
Эндокринные нарушения. Большая группа исследователей занималась изучением связи между болезнями пародонта и эндокринными заболеваниями. Были отмечены болезни пародонта при гипо- и гиперфункции шитовидной железы, околощитовидных и половых желез.
Наиболее подробно изучены изменения пародонта при сахарном диабете. Ангиопатия пародонта наряду с ангиопатией сетчатки, ночек относится к ранним и часто встречающимся поражениям — у 90–93 % больных сахарным диабетом отмечаются изменения в пародонте. В патогенезе пародонтального синдрома при сахарном диабете основное значение придается ангиопатии пародонта. В свою очередь в генезе поражения мелких сосудов первостепенная роль принадлежит диспротеинемии и в основном повышению ГАГ в крови [Ефимов А. И. и др., 1970]. Патоморфологические изменения сосудов при сахарном диабете, согласно исследованиям Д. А. Зербино (1977), носят своеобразный характер: просвет сосудистого русла не исчезает, но поражается сама сосудистая стенка. В основе диабетической микроангиопатии лежат процессы плазморрагии. Они сводятся к первичному плазматическому повреждению базальной мембраны микрососуд истого русла, а далее приводят к склерозу и гиалинозу стенки. Никакого отношения к воспалению эти изменения не имеют. Следовательно, микроциркуляторные расстройства носят первичный характер. На фоне уже имеющегося нарушения транскапиллярного обмена, повышенной проницаемости соединительнотканных структур пародонта микрофлора десневой щели (ее эндотоксины, ферменты) вызывает воспалительно-деструктивные изменения, а появляющаяся перегрузка тканей пародонта еще в большей степени усугубляет положение.
Заболевания желудочно-кишечного тракта. По данным Т. Н. Власовой (1989), одной из причин заболевания пародонта при язвенной болезни желудка и двенадцатиперстной кишки является нарушение гормональной регуляции кальциевого обмена за счет изменения функции как щитовидной, так и околощитовидных желез. Клинико-лабораторными исследованиями установлено, что у больных с патологией желудочно-кишечного тракта чаще (85–91 % случаев) выявляются воспалительные формы заболевания пародонта, реже (9—14 %) — пародонтоз.
Болезни крови и гемопоэтической системы. При анемиях наблюдаются дистрофические изменения в тканях пародонта; при острых лейкемиях у детей и взрослых отмечается проявление гиперплазии десневого края. Характерные изменения с резорбцией и остеопорозом костной ткани наблюдаются при доброкачественных нейтропениях (циклической и постоянной).
Хотя роль общих факторов в появлении и развитии воспалительных и особенно дистрофических процессов в пародонте совершенно очевидна, тем не менее интимные механизмы патогенеза большинства из них остаются нераскрытыми. Показано, что при заболеваниях желудочно-кишечного тракта, печени, почек, нервной, сердечно-сосудистой, эндокринной систем, ревматических болезнях (коллагенозы), гипертонической болезни, аллергических заболеваниях пародонт страдает чаще, чем у здоровых людей.
Комитет экспертов ВОЗ по пародонтологии (Москва. 1977) предложил схему этиологии гингивита и пародонтита, в которой понятие «фактор времени» связывается с временем созревания зубного налета (бляшки), его консистенцией, изменением микробного состава и времени контакта бляшки с тканями маргинального пародонта (схема 9.1).

Состояние свертывающей и фибринолитической системы крови:
Психосоматические факторы. В развитии пародонтальных заболеваний имеют значение ксеростомия, связанная с приемом лекарственных препаратов (седативные средства, транквилизаторы, нейролептики) при депрессивных состояниях, стресс, гиперкинезия жевательных мышц (бруксизм), сочетающаяся с психическим напряжением. Из системных факторов необходимо указать на генетическую предрасположенность (юношеские поражения пародонта), нарушения полового созревания, отклонения в структурной организации полиморфно-ядерных лейкоцитов. К лекарственным препаратам, отрицательно влияющим на ткани пародонта, относят кортикостероиды, иммунодепрессанты, гидантоин, соли тяжелых металлов, пероральные противозачаточные препараты, циклоспорин. При всех формах поражения пародонта отмечается угнетение функционального состояния соединительной ткани (вероятность более 90 %).
Иммунологические нарушения. В последние годы благодаря быстрому развитию клинической иммунологии внимание исследователей привлекли иммунологические аспекты болезни пародонта. Ряд исследователей выявили существенное ослабление специфических и неспецифических факторов защиты полости рта, свидетельствующего о значительных нарушениях в Т- и В-системах иммунитета. Определенное значение в патогенезе пародонтита играют аутоиммунные механизмы. Патология иммунной системы играет несомненную роль в воспалительно-деструктивном процессе пародонта, хотя пародонтит и тем более пародонтоз не являются типичными аутоиммунными заболеваниями. Однако при наличии воспаления в механизмах деструкции тканей пародонта аутоиммунный компонент как одно из звеньев патогенеза, несомненно, может играть важную роль.
Нормальный организм наделен весьма чувствительным иммунологическим аппаратом, способным распознавать чужеродные антигены (не только «чужие», но и с приобретенными чужеродными свойствами в динамике развития патологического процесса). Эта способность предопределяется генетически, поэтому если предрасположенность к некоторым заболеваниям наследуется по доминантному типу, то признаки болезни обнаруживаются в каждом поколении. В полной мере это, по-видимому, относится к различным видам патологии прикуса, имеющем в генезе заболевания пародонта большое значение.
Перенесенные и сопутствующие заболевания, гормональные расстройства. Эти состояния, снижая барьерную локальную резистентность пародонта, способствуют развитию аутосенсибилизации и иммунопатологического процесса с резорбцией костной ткани альвеолярных отростков челюстей.