ФР ССЗ, ДЭ и клинические симптомы
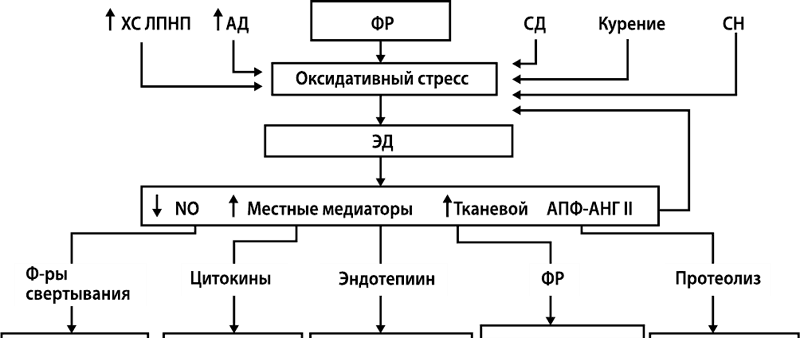
Рисунок 17.
Остановимся на роли самых главных фоновых заболеваниях.
Многие великие цари, императрицы на Руси страдали АГ и умирали от инфаркта головного мозга – одного из основных осложнений гипертонического криза. Но в те далекие времена мало знали о заболеваниях в принципе. Но список «жертв» повышения АД можно продолжить и сейчас, хотя сегодня врачи достаточно информированы в вопросах лечения АГ, и, тем не менее, большое количество людей умирают от осложнений этого заболевания.
АГ имеет свои органы-мишени: сердце, сосуды головного мозга, почки, сетчатка глаза. При длительном течении АГ происходит поражение этих органов с развитием гипертрофии миокарда ЛЖ, хронической ишемии головного мозга, нефропатии, ангиопатии сетчатки. Кроме того, АГ приводит к развитию воспаления: в несколько раз повышается уровень ИЛ – 1B, ФНО – а, ИЛ – 6 по сравнению с группой здоровых людей (рис. 18) [32].
При осложненном течении АГ развиваются так называемые ассоциированные клинические состояния – сосудистые катастрофы: ОИМ, ОНМК, отслойка сетчатки, почечная недостаточность. Все это еще раз демонстрирует полисистемность поражения с формированием сосудистой коморбидной патологии. Безусловно, АГ – важное звено этого вида коморбидности.
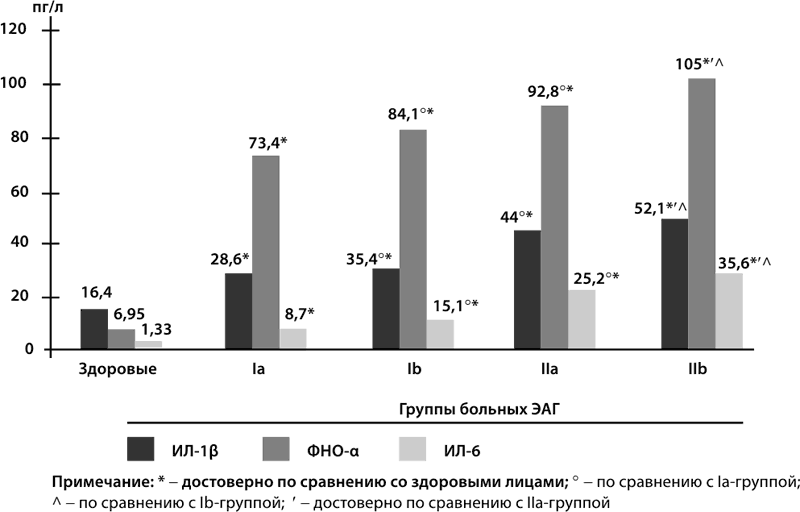
Рисунок 18.
По данным аутопсии 1566 сосудистых пациентов, умерших в стационаре, признаки АГ выявлялись в 96 % случаев. Так, наличие АГ было у 75 % мужчин и 94 % женщин, умерших от ОИМ. Сочетание АГ и ПИКС выявлялось у 55 % мужчин и 79 % женщин. А при инфаркте головного мозга признаки АГ наблюдались у 95 % мужчин и женщин.
Примерно такая же статистика и у пациентов, умерших вне стационара: из 241 пациента АГ имела место у 221 (92 %). При ретроспективном анализе амбулаторных карт выяснилось, что среднее значение АД было 154/92 мм. рт. ст. При этом 53 пациентам (24 %) гипотензивные препараты вообще не назначались. А 72 пациентам (42,8 %) из 168, которым проводилось лечение АГ, гипотензивная терапия была назначена в режиме монотерапии. Неудивительно, что лишь 13 % пациентов смогли достичь целевых уровней АД. Неудивительно и другое: каждый четвертый пациент вызывал СМП по поводу ГК, что достоверно отражает неадекватное ведение на догоспитальном этапе. Сегодня известно, что ГК – это не только повышение уровня АД. Каждый ГК усиливает стеноз церебральных и коронарных артерий, что увеличивает риск сосудистых катастроф в 17 раз, а риск смерти – в 4 раза [33]. Каждый ГК вызывает склерозирование 5–20 % терминальных приносящих артериол почки, что является причиной развития хронической болезни почек [34].
Поэтому раннее выявление АГ, диспансерное наблюдение таких пациентов, а также рациональная комбинированная гипотензивная терапия современными препаратами – важная задача амбулаторного этапа, направленная на прерывание патологической цепи развития сосудистой коморбидности и профилактику осложнений.
Другое, не менее важное, звено формирования сосудистой коморбидности – атеросклероз – хроническое системное заболевание, поражающее артерии эластического и мышечно-эластического типа с изменением всех слоев сосудистой стенки. Атеросклероз – системный процесс с большей или меньшей выраженностью в определенных артериях, с чем и связаны клинические проявления. Мультифокальный характер атеросклеротического поражения демонстрируют данные 202 аутопсий пациентов с ПИКС: атеросклероз коронарных артерий был выявлен в 100 % случаев, почечных артерий – в 74 %, церебральных сосудов – в 60 %, аорты – в 58 %, артерий ног – в 9 %. Вместе с тем при анализе амбулаторных карт этих пациентов оказалось, что статины были назначены не более чем в 10 % случаев, а ежегодный контроль за уровнем холестерина проводился лишь у 7 %. При этом высокотехнологические методы, в частности кардиохирургические и сосудистые операции, выполнялись вообще в единичных случаях, что свидетельствует о неадекватном ведении таких пациентов на амбулаторном этапе.
Развитие атеросклероза начинается еще с юного возраста, достигая клинической прогрессии в пожилом возрасте (рис. 19).

Рисунок 19.
Заболевание сопровождается локальным воспалением, отложением патологически модифицированных липидов, дисфункцией эндотелия, пролиферацией и изменением сократимости гладкомышечных клеток, развитием фиброзной ткани и кальцификацией с последующим стенозом и окклюзией, приводящим к гемодинамическим нарушениям в зоне ответственности пораженного сегмента сосуда.
Повышение АД, атерогенных липопротеидов, увеличение индекса интима-медиа – все это приводит к клиническим проявлениям АГ и атеросклеротического поражения артерий [35].
Таким образом, можно говорить о существовании универсального механизма развития сосудистой коморбидности – дисфункции эндотелия, который представлен на рис. 20.
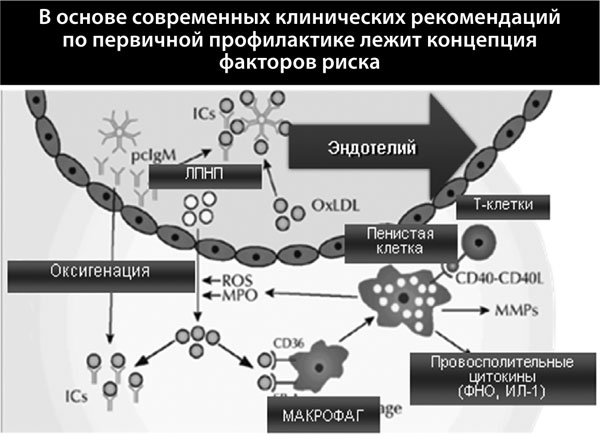
Рисунок 20.
Липопротеиды низкой плотности диффундируют в кровь через эндотелий, соединяясь с атомами кислорода; далее макрофаги поглощают эти молекулы, превращаясь в пенистые клетки, их задача – массивный выброс провоспалительных цитокинов, которые и разрушают эндотелий. В местах разрушений образуются липидные бляшки. Таким образом, при наличии факторов риска формируется «порочный круг» в виде эндотелиальной дисфункции, запускающей синтез интерлейкинов, деятельность которых приводит к потере функциональности тканей, появлению ассоциированных заболеваний, и, в конечном итоге, коморбидности. Иллюстрацией этому является, что риск СС осложнений напрямую зависит от концентрации СРБ: менее 1 мг/л – риск ССО минимальный, 1,1–1,9 мг/л – низкий, 2,0–2,9 мг/л – умеренный и более 3 мг/л – высокий. Иными словами такая корреляция СРБ с риском ССО подтверждает значимость хронического воспаления, развивающегося при сосудистой патологии.
Помимо привычных клинических форм, развивающихся при атеросклерозе (ИБС, нефроангиосклероз, АГ, хроническая цереброваскулярная болезнь), в последние годы все большее внимание клиницистов направлено на необходимость выявления поражений суставов и, в частности, остеоартрита (рис. 21).
Было показано, что в артериях, питающих сустав, выявляются атеросклеротические бляшки с признаками нестабильности – такие же изменения, как и в коронарных артериях при ОИМ. Это подтвердило исследование проф. Верткина А. Л. и проф. Наумова А. В., в котором сравнивались изменения в суставах и периартикулярных тканях у умерших коморбидных сосудистых пациентов (основная группа) и погибших при ДТП, не имеющих соматических заболеваний (контрольная группа). У всех больных с наличием коморбидной сосудистой патологии в артериях, питающих сустав, определялись изменения по типу склероза и гиалиноза, что является признаком атеросклеротического поражения. А у 92 % среди этих пациентов имелись признаки нестабильной атеросклеротической бляшки в артериях сустава. Типичные изменения в артериях, питающих сустав, как и в любых артериях, обусловило возникновение нового термина «атеросклероз суставов». К сожалению, эти последние тенденции никак не воспринимаются терапевтами, поскольку в амбулаторных картах эти факты не приводятся.
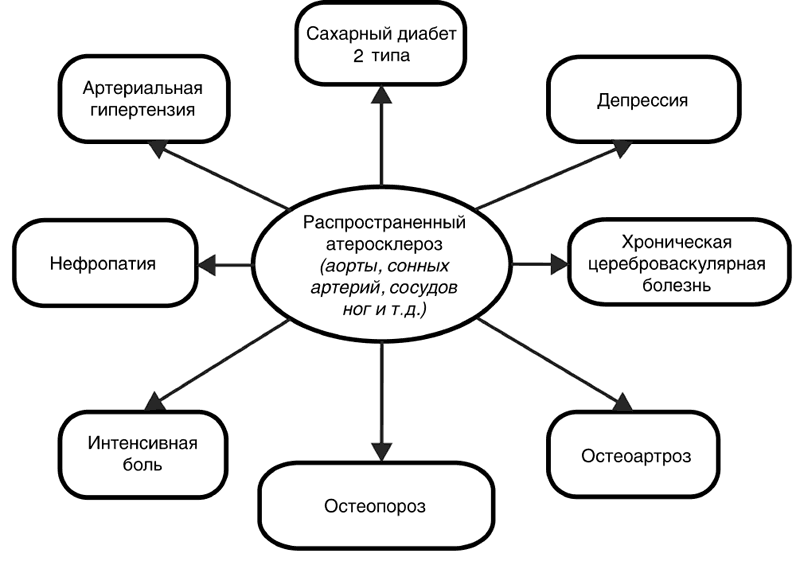
Рисунок 21.
Таким образом, пренебрежение в практической работе к широко известным факторам риска (курение, алкоголь, ожирение) и фоновым заболеваниям, таким как АГ и атеросклероз, обусловливает не только становление коморбидной патологии, но и ее прогрессирование и летальные исходы.
Еще одним фактором риска, фоновым заболеванием, приводящим к эндотелиальной дисфункции, является СД 2 типа. По прогнозам Международной Федерации Диабета к 2025 году количество больных СД в мире увеличится вдвое, а к 2030 году с этим диагнозом будет около 500 миллионов человек – грозит настоящая пандемия. По данным той же статистики ежегодно в мире каждые 10 секунд возникает 3 новых случая СД 2 типа. При этом печальное лидерство среди стран Европы по распространенности СД 2 типа принадлежит России.
При СД 2 типа развивается целая палитра изменений: диабетическая нейропатия, диабетическая микроангиопатия (ретинопатия, нефропатия), синдром диабетической стопы, диабетическая нейроостеоартропатия, диабетические макроангиопатии (ИБС, ХСН, цереброваскулярные заболевания, хронические облитерирующие заболевания артерий нижних конечностей); АГ, дислипидемия. Все это вносит существенный вклад в формирование коморбидной патологии.
Необходимо помнить, что наличие СД повышает риск неблагоприятного исхода у коморбидных сосудистых больных. Так, риск смерти от ОИМ при наличии СД у мужчин повышается в 3–4 раза, а у женщин – в 7–8 раз по сравнению с пациентами, не имеющими СД. Помимо сосудистой коморбидности СД ассоциируется так же со снижением легочной функции и развитием ХОБЛ.
Несмотря на столь грозные проявления, мы вынуждены констатировать все те же проблемы участковой службы: участковые терапевты не акцентируют внимание на СД 2 типа и не фиксируют наличие этого заболевания в медицинской документации. Так, выборочный анализ 514 амбулаторных карт показал, что в клиническом диагнозе, поставленном терапевтом амбулаторного звена, СД 2 типа присутствовал лишь у 16 из 514 больных, что составило 3 %. При этом по данным клинико-анатомической базы из 1864 умерших в стационаре 19 % пациентов имели СД
2 типа. Интересно, что уровень глюкозы крови на момент смерти у подавляющего большинства был избыточен: от 8 до 12 ммоль/л – у 218 пациентов (49 %), 12–16 ммоль/л – у 76 (17 %), более 16 ммоль/л – у 19 (4 %), что свидетельствует о неадекватном ведении этих пациентов. При этом у 84 % СД 2 типа имел осложненное течение. Среди подтвержденных при аутопсии осложнений были: пневмония (36,7 %), ХПН (27,5 %), гнойно-септические осложнения: пиелонефрит (8,3 %), гнойный бронхит (10 %), перитонит (5 %), гнойный холецистит (6,7 %).
Необходимо помнить, что на формирование коморбидной патологии и ее осложнений влияет не только клинически манифистированный СД 2 типа, но и НТГ, а также НГН. Так, у пациентов с НТГ риск сердечно-сосудистой смертности по отношению к лицам с нормогликемией составляет 1,32, а у пациентов с НГН – 1,14 [36]. Поэтому ранняя диагностика нарушений углеводного обмена – это самая адекватная профилактика осложнений СД 2 типа и важнейшая задача работы врача общей практики.
Важно подчеркнуть, что диагностика СД 2 типа проста и доступна на амбулаторном этапе – необходимо определить уровень гликемии и гликированного гемоглобина. Однако данные 241 амбула-
торных карт «сосудистых пациентов» – главная группа риска по развитию СД 2 типа – свидетельствуют, что в 54,2 % случаев уровень глюкозы вообще не определялся (рис. 22).
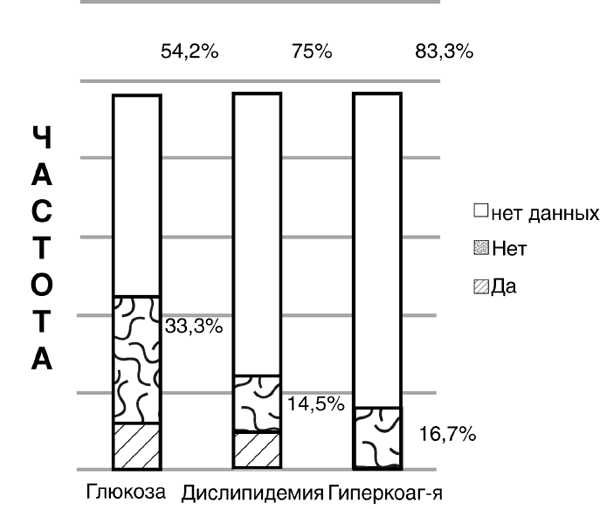
Рисунок 22.
В скрининг СД необходимо включать и оценку риска заболевания СД 2 типа в течение 10-летнего периода. Для этого разработана шкала FINDRISK (FINnish Diabetes Risk Score) (табл. 3), состоящая из 7 простых вопросов, на которые должен ответить пациент [37].
После суммации полученных баллов, можно узнать суммарный риск развития СД 2 типа в ближайшие 10 лет (табл. 4).
Таблица 3. Шкала FINDRISK
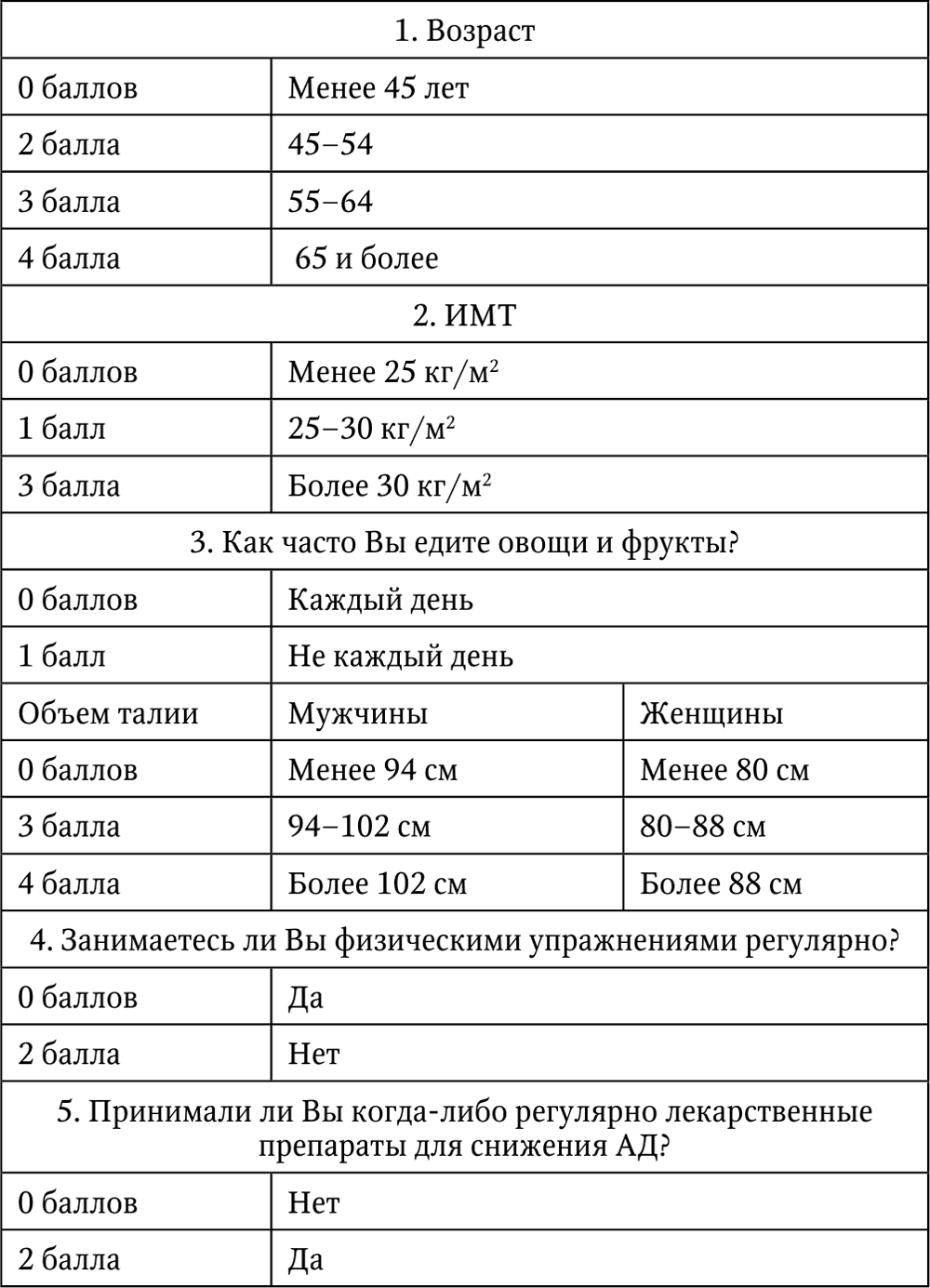

Таблица 4.
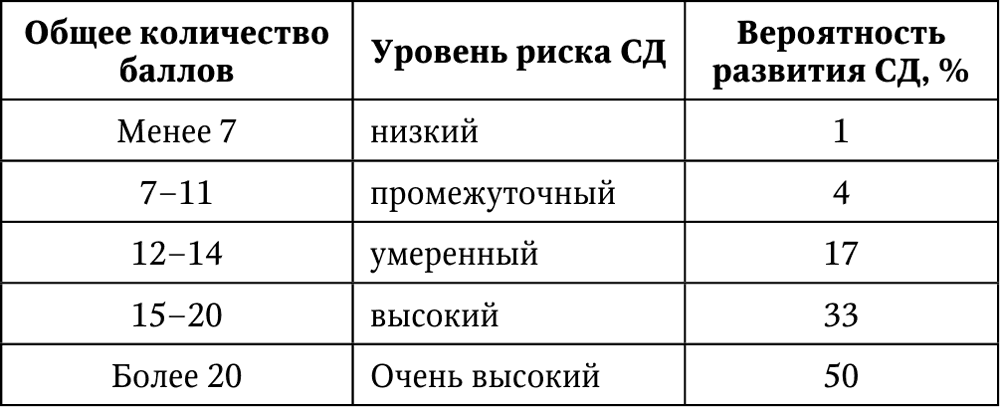
При выявлении с помощью данной шкалы высокого и очень высокого риска развития СД 2 типа, такого пациента необходимо взять на тщательный динамический амбулаторный мониторинг.
Анализ медицинской документации коморбидных больных с ПИКС позволил выделить наиболее распространенные у них и другие заболевания, в том числе ДГПЖ, хронический пиелонефрит, ЖКБ (рис. 23, 24).
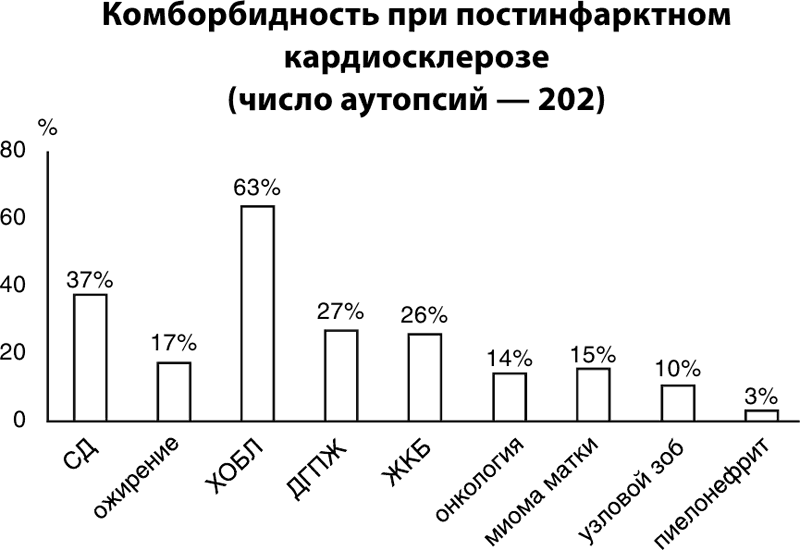
Рисунок 23.
Так же необходимо помнить и о возрастной инволюции, приводящей к дефициту половых гормонов, в том числе и тестостерона, что влияет не только на снижение половой функции, но и является фактором риска развития соматической патологии, в первую очередь, сосудистой. Нами была выявлена распространенность андрогенного дефицита у 721 пациента с ССЗ (рис. 25).
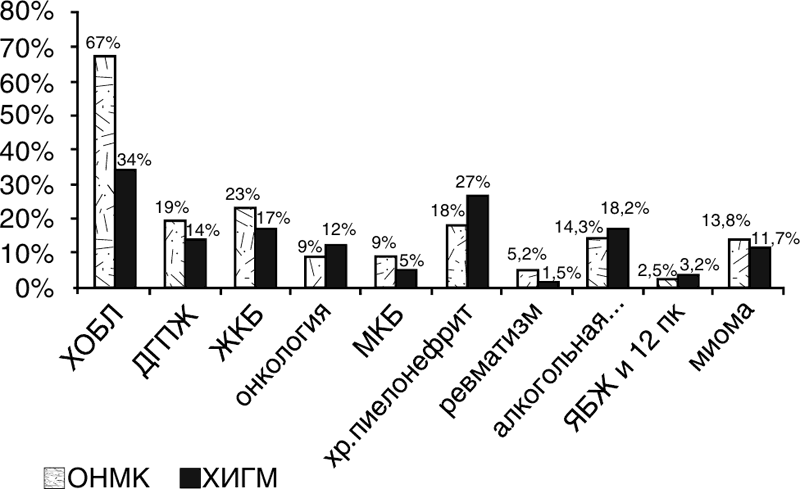
Рисунок 24.
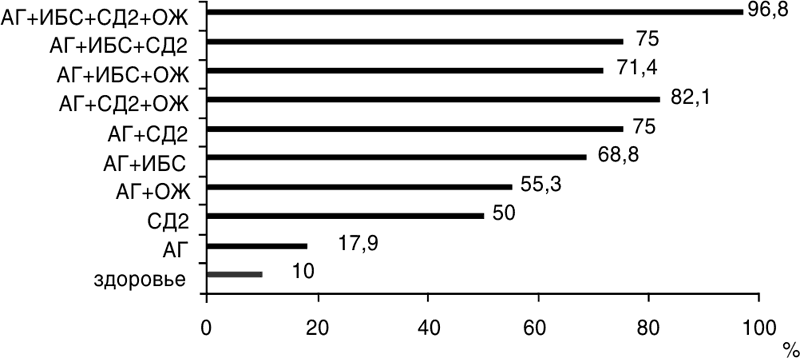
Рисунок 25.
Из рис. 25 видно, что наиболее часто андрогенный дефицит встречается при сочетании ИБС с АГ, СД 2 типа и ожирением (96,8 % против 10 % у пожилых мужчин, не имеющих такой патологии).
А что у женщин? Как известно, эстрогены – главные половые гормоны, защищающие женщин от сосудистых заболеваний. Естественное старение организма обусловливает дефицит эстрогенов, что приводит к дефициту оксида азота, повышению активности ренин-ангиотензинальдостероновой системы, в связи с чем повышается АД, прогрессирует атеросклероз, развивается остеопороз, возникают заболевания щитовидной железы, ЖКБ, т. е. формируется коморбидность.
Итак, сосудистая коморбидность – самая распространенная и прогностически неблагоприятная форма, формирующаяся под воздействием факторов риска, приводящих к локальному воспалению, эндотелиальной дисфункции, что ведет к запуску сердечно-сосудистого континуума, росту осложнений и летальных исходов.






