Интерстициальные болезни легких
Определение. Интерстициальные болезни легких (ИБЛ) – гетерогенная группа болезней, объединенная рентгенологическим синдромом двусторонней диссеминации.
Актуальность. Сегодня можно назвать около 200 заболеваний, имеющих признаки ИБЛ, что составляет около 20 % от всех заболеваний легких, причем половина из них – неясной природы. Поэтому относить ИБЛ к группе редких болезней, как это делалось ранее, уже нельзя. Диагностические ошибки у этих больных составляют 75–80 %, адекватная специализированная помощь оказывается им обычно через 1,5–2 года после возникновения первых признаков заболевания, что отрицательно влияет на эффективность лечения и прогноз. Диагностические ошибки влекут за собой неправильное лечение, причем с использованием достаточно агрессивных методов, глюкокортикостероидов, цитостатиков, антибиотиков.
Летальность при ИБЛ значительно выше, чем при большинстве других заболеваний легких. Причины высокой летальности определяются малой осведомленностью врачей, недостаточной технической оснащенностью медицинских центров, трудностями дифференциальной диагностики в связи с отсутствием патогномоничных признаков, фатальным характером некоторых ИБЛ.
Классификация. Наиболее распространенными терминами для обозначения этой группы болезней являются «диссеминированные заболевания легких», «гранулематозные болезни легких», «интерстициальные болезни легких», «диффузные паренхиматозные болезни легких». Понятие «диссеминированные заболевания легких» учитывает лишь один, хотя и очень важный, признак болезни – рентгенологический синдром легочной диссеминации, не указывая на существо процесса. Термин «гранулематозные болезни легких» основан на формировании гранулем при этих заболеваниях, в то время как наиболее грозные заболевания этой группы, ранее объединяемые термином «идиопатический фиброзирующий альвеолит» (ИФА), вообще не сопровождаются гранулемами. Термин «диффузные паренхиматозные болезни легких» делает акцент на паренхиматозном поражении – альвеолите, который является стержнем и главной ареной развертывания драматических событий.
«Интерстициальные болезни легких» – на сегодняшний день наиболее распространенный в мире термин для обозначения этой группы болезней. Однако это понятие предполагает преимущественное поражение интерстиция, в то время как самые серьезные по своим исходам процессы происходят в паренхиме легких с нередким вовлечением воздухоносных путей.
Главная общая черта этих болезней – альвеолит, причем в большинстве случаев иммунной природы. Основные отличительные признаки: степень и уровень вовлечения в патологический процесс основных структур легкого, а также выраженность и характер прогрессирования дыхательной недостаточности. Так, при саркоидозе, экзогенном аллергическом альвеолите (ЭАА), альвеолярном протеинозе поражаются в первую очередь строма легкого и дольковые структуры. При туберкулезе легких и пневмокониозах – дольковые структуры; при ИФА и ревматических болезнях – внутридольковые структуры.
Этиология. Все ИБЛ по этиологическому признаку можно разделить на заболевания с известной этиологией, неустановленной природы и вторичные при системных заболеваниях.
Ряд авторов предлагают исключить из понятия ИБЛ туберкулез, пневмокониозы, легочные диссеминации опухолевой природы и ряд других заболеваний с известными этиологическими факторами и патогенетическими механизмами и рассматривать их в рамках дифференциальной диагностики с ИБЛ неясной этиологии, которые объединяются в понятие «идиопатический легочной фиброз».
В табл. 17 указаны распространенные ИБЛ известной этиологии.
Таблица 17
Наиболее распространенные ИБЛ известной этиологии

Среди инфекционных ИБЛ первое место по значимости принадлежит туберкулезу. Не всегда легко отличить его от других форм ИБЛ, особенно у пожилых, ослабленных больных. Легочные микозы чаще всего бывают вторичными, их появлению обычно предшествует формирование иммунодефицита. В диагностике паразитарного поражения легких большое значение имеет тщательно собранный эпидемиологический анамнез. Для респираторного дистресс-синдрома характерно наличие септицемии, тяжелой травмы или интоксикации. Для больных СПИДом характерен распространенный инфекционный процесс, вызываемый атипичными микроорганизмами – пневмоцистами, легионеллами, микобактериями и др.
В диагностике неинфекционных ИБЛ важны профессиональный анамнез, знание факторов экологической агрессии, а также сведения об употреблении лекарств (кордарон, нитрофураны, метотрексат, циклофосфамид, блеомицин, препараты золота), которые являются причиной ИБЛ. В неосложненных случаях диагностика заболеваний этой группы не представляет собой больших затруднений.
Около половины всех ИБЛ относятся к категории заболеваний с неустановленной этиологией. Наиболее распространенные ИБЛ неустановленной этиологии:
– обычная интерстициальная пневмония (смерть в течение 2–3 лет смомента диагностики);
– десквамативная интерстициальная пневмония;
– острая интерстициальная пневмония – синдром Хаммена – Рича (летальный исход в течение 1–3 месяцев);
– неспецифическая интерстициальная пневмония;
– саркоидоз;
– гистиоцитоз Х (легочный лангергансоклеточный гистиоцитоз);
– альвеолярный протеиноз;
– идиопатический легочный гемосидероз;
– некротизирующие васкулиты: гранулематоз Вегенера, синдром Черджа – Строс (Churg – Strauss);
– синдром Гудпасчера.
Таблица 18
Предположительная этиология идиопатических интерстициальных пневмоний
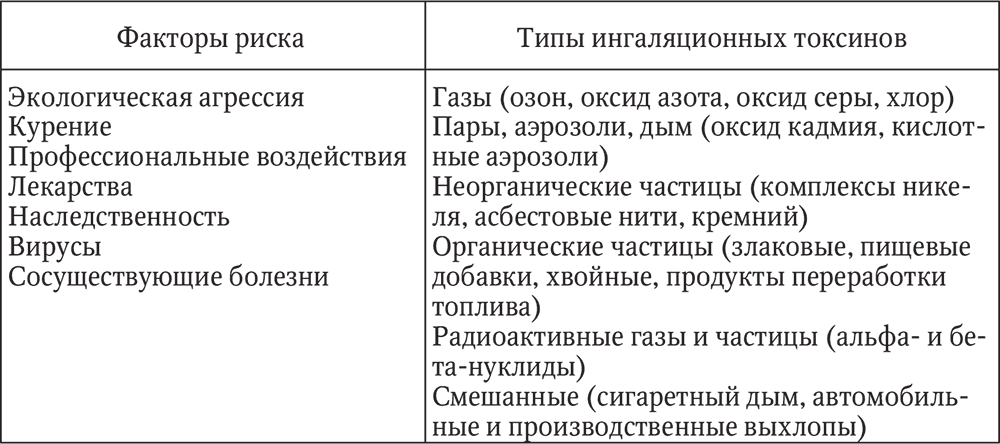
Среди факторов риска поражений легочного интерстиция по типу ИФА обсуждается роль курения, системных заболеваний, лекарств, профессиональных и связанных с внешней средой поллютантов (табл. 18). Особое внимание уделяют роли вирусных инфекций в генезе воспалительных и фибропластических изменений в легких.
Патогенез. Взаимосвязь вирусной инфекции и ИФА не всегда удается подтвердить, но наблюдения показывают, что у больных, инфицированных вирусами Эпштейна – Барр, гепатита В и С, отмечается частое развитие морфологических изменений на территории мелких бронхов, сходных с облитерирующим бронхиолитом, и присоединение клинических признаков бронхиальной обструкции. Эти особенности расцениваются как результат взаимодействий инфекционного агента с иммунной системой, затрагивающих как различные реакции гиперчувствительности, так и прямое действие вируса на эпителий бронхиол.
В поражении легких при вирусном гепатите и циррозе печени имеет значение образование сосудистых печеночно-легочных коллатералей, что приводит к усилению поступления в легкие фиброгенных факторов роста, источником которых являются активированные вирусом иммунокомпетентные клетки печени.
Лекарственные препараты также считаются важной причиной интерстициального повреждения легких. В патогенезе легочной ятрогении особое внимание уделяют свободнорадикальному повреждению из-за высокого кислородного потенциала в легком. Свободные радикалы напрямую и опосредованно участвуют в повреждении легочных структур, прогрессировании пневмосклероза. Помимо того, под воздействием препаратов и их метаболитов (блокаторы кальциевых каналов, цитостатики, антибиотики, наркотические анальгетики и т. д.) в легком нарушаются секреторные функции эпителия, альвеолярных макрофагов, что приводит к морфологическим изменениям по типу фосфолипидоза.
Среди различных вариантов вредных воздействий курение табака считается одним из главных претендентов на роль стимула в развитии ИФА и в особенности облитерирующего бронхиолита. Дериваты табачного дыма активируют систему цитохрома, что приводит к нарушению процессов репликации ДНК, увеличению числа мутаций в эпителиальных клетках.
Курение считается облигатной причиной и другой формы интерстициальных болезней легких – гистиоцитоза Х, характеризующегося тяжелым поражением легких с формированием кистозных полостей и внелегочными поражениями в рамках гранулематозного процесса (несахарный диабет, поражения кожи, остеодеструкция).
У курильщиков, включая и пассивных, увеличивается восприимчивость дыхательных путей к воздействию токсичных агентов. При интерстициальных болезнях легких, в том числе при ИФА, табачный дым можно рассматривать как инициальный повреждающий фактор, стимулирующий воспалительно-склеротические процессы в легких.
В экологически неблагоприятных районах усиливается влияние факторов экологической агрессии: продуктов сгорания автомобильного топлива, переработки нефти, оксида серы, копоти, паров, поллютантов.
Профессиональные воздействия (кремний, асбест, соединения металлов, органические соединения, пыль растительного и животного происхождения) являются причиной пневмокониозов, экзогенного аллергического альвеолита. В эпидемиологических исследованиях была показана связь ИФА при профессиональном контакте с металлической и древесной пылью, продуктами сгорания органических и неорганических соединений (шлифовщики, столяры, пожарные).
Следует отметить, что распространенность изменений в легких, тяжесть течения заболевания во многих случаях не зависят от длительности воздействия и экспозиционной нагрузки токсического фактора. Клинические и экспериментальные данные свидетельствуют, что иммунный ответ при ИФА основан на поляризации лимфоцитарной популяции в сторону Т-хелперов, причем интенсивность процессов воспаления и фиброзирования определяется генетической предрасположенностью. В прогрессировании ИФА большое значение придают провоспалительным и профиброгенным цитокинам, потенцирующим воспалительную реакцию, процессы репарации тканей и связанные с ними процессы фиброзирования в респираторных отделах легочного интерстиция.
Таким образом, риск развития ИФА и его активность обусловлена характерным набором генов, взаимодействующих с внешними факторами и элементами клеточной защиты, определяющих фенотипические особенности фибропролиферативной реакции в легких.
Клиническая картина. Основные клинические признаки ИБЛ весьма ограничены: одышка, кашель, кровохарканье, поражение плевры и внелегочные симптомы. В связи с этим диагностическое значение имеет не только наличие или отсутствие признака, но и его выраженность, изменчивость, а также сочетание с другими, в том числе внелегочными симптомами.
Одышка – главный симптом ИБЛ. При ИФА появляется рано, нередко еще до возникновения рентгенологических признаков болезни, носит инспираторный характер и прогрессирует. У больных саркоидозом одышка является поздним признаком. Нередко у больных саркоидозом наблюдается несоответствие выраженности рентгенологической диссеминации полному отсутствию одышки. У больных ЭАА одышка носит смешанный характер, ее возникновение связано с причинным фактором (аллергеном) и носит волнообразный характер.
Кашель. Поражение изолированных альвеол не сопровождается кашлем из-за отсутствия в них нервных окончаний, потому кашель является признаком раздражения воздухоносных путей. При ЭАА и саркоидозе кашель свидетельствует о бронхоцентрическом процессе. При ИФА кашель – поздний признак, и может быть результатом инфицирования (бактерии, грибы, вирусы) либо формирования тракционных бронхоэктазов.
Кровохарканье – признак деструкции легочной ткани. Наиболее характерно кровохарканье для туберкулеза легких, гранулематоза Вегенера, синдрома Гудпасчера, легочного гемосидероза, фиброзирующих альвеолитов при ревматических болезнях. При ИФА – это поздний признак, проявляющийся в 13 % случаев.
Поражение плевры. Плевральный выпот наиболее часто наблюдается при ревматических болезнях, лекарственном поражении легких, асбестозе, лейомиоматозе. Пневмоторакс характерен для гистиоцитоза Х и лейомиоматоза.
Каждое из заболеваний, входящих в группу ИБЛ, имеет свои наиболее характерные клинические признаки, позволяющие установить диагноз. Оценка последовательности, скорости появления и развития признаков заболевания может иметь решающее значение в диагностике. Так, ИФА обычно начинается с тяжелой прогрессирующей одышки, приносящей максимальные неудобства больному, признаков обструкции нет. При саркоидозе диагностика легочного поражения нередко является случайной находкой при рентгенологическом исследовании грудной клетки; одышка развивается в поздних стадиях болезни. У больных гистиоцитозом Х умеренная одышка сочетается с рецидивирующими пневмотораксами. У больных экзогенным альвеолитом одышка носит смешанный характер (сочетание обструкции с рестрикцией) и нередко зависит от контакта сэтиологическим фактором (легкое фермера, птицевода, голубевода и пр.). Альвеолярный протеиноз характеризуется накоплением в альвеолах белково-липидного вещества, что и определяет клиническую картину. Для легочного гемосидероза характерным симптомом является кровохарканье. У больных некротизирующими васкулитами кровохаркание обычно сочетается с лихорадкой и присоединением вторичной инфекции. Для синдрома Гудпасчера основными признаками являются кровохарканье в сочетании с признаками гломерулонефрита.
Ниже приведен перечень заболеваний, при которых нередко развивается ИБЛ, с формированием диффузного легочного фиброза и дыхательной недостаточностью.
Системные заболевания, при которых возникают ИБЛ
1. Ревматические болезни: ревматоидный полиартрит, системная красная волчанка, дерматомиозит, синдром Шегрена.
2. Болезни печени: первичный билиарный цирроз, хронический аутоиммунный гепатит.
3. Болезни крови: аутоиммунная гемолитическая анемия, идиопатическая тромбоцитопеническая пурпура, хронический лимфолейкоз, эссенциальная криоглобулинемия.
4. Тиреоидит Хашимото.
5. Миастения (Myasthenia gravis).
6. Болезни кишечника: язвенный колит, болезнь Крона, болезнь Уипла.
7. Хронические болезни сердца с левожелудочковой недостаточностью, с шунтированием крови слева направо.
8. Хроническая почечная недостаточность.
9. Системные васкулиты.
Этот перечень не исчерпывает абсолютно всех заболеваний, которые могут вести к ИБЛ, но приводит наиболее часто встречающиеся. Возможность существования так называемых вторичных ИБЛ предполагает в процессе диагностики уделять внимание внелегочной симптоматике, являющейся проявлением основного заболевания, что предполагает знание этих заболеваний, т. е. широкую терапевтическую образованность.
Диагностика
Рентгенодиагностика. Обзорная рентгенограмма, которая остается основным методом диагностики при подозрении на заболевание органов дыхания, при ИБЛ дает до 50 % ошибок. Особенную важность имеет анализ архивных рентгенограмм, позволяющий объективно установить истинное начало заболевания и определить характер его прогрессирования, а также провести клинико-рентгенологические параллели.
Компьютерная томография (КТ) высокого разрешения – главный метод исследования при ИБЛ, который позволяет оценить не только распространенность процесса, но проследить за его динамикой.
В зависимости от диагностических возможностей КТ все ИБЛ делятся на 3 категории (табл. 19).
Исследование функции внешнего дыхания. К основным функциональным признакам ИБЛ относятся:
– уменьшение статических легочных объемов;
– снижение растяжимости легких;
– увеличение частоты дыхания;
– альвеолярная гиповентиляция;
– нарушение вентиляционно-перфузионных отношений;
– снижение диффузионной способности легких;
– гипоксемия, нарастающая при физической нагрузке.
Таблица 19
Категории ИБЛ в зависимости от разрешающих возможностей КТ
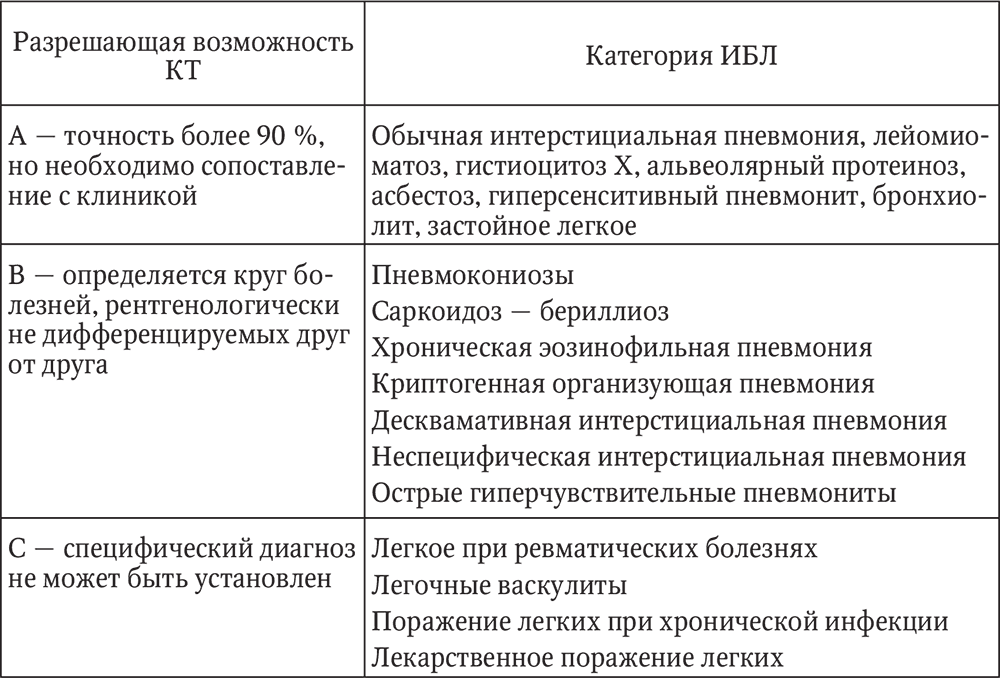
Для некоторых ИБЛ характерно сочетание рестриктивных нарушений с обструкцией. Это относится к ЭАА, гистиоцитозу Х, саркоидозу, при сочетании фиброзирующих альвеолитов с эмфиземой, у больных вторичными ИБЛ при ревматических болезнях, лейомиоматозе.
Иммунологические методы диагностики ИБЛ способствуют установлению этиологии при определении циркулирующих антигенов или антител к ним, позволяют качественно и количественно характеризовать иммунодефицит. Полезны для выявления активности иммунопатологического процесса путем определения маркеров активации иммунокомпетентных клеток, а также для определения циркулирующих иммуноглобулинов и иммунных комплексов.
Микробиологические методы способствуют установлению этиологического диагноза инфекционных ИБЛ путем культуральных исследований и в полимеразно-цепной реакции. Возможна оценка микробной колонизации респираторной системы и определение характера вторичной флоры в стадии сотового легкого.
Бронхологические методы (фибробронхоскопия) позволяют провести осмотр бронхиального дерева, произвести лаваж с подсчетом клеточных элементов, а также различные виды биопсий, в том числе и трансбронхиальную биопсию легких. Исследование клеточного состава бронхоальвеолярного содержимого дает возможность оценить активность альвеолита при относительно свежем патологическом процессе без грубых фиброзных изменений, искажающих результаты исследования. То же относится к трансбронхиальной биопсии, которая наиболее информативна при отсутствии выраженного фиброза.
Ранняя и точная диагностика большинства ИБЛ невозможна без исследования биопсийного материала. Для того чтобы свести до минимума травматизацию больного и получить максимальную информацию о процессе в легких, выбор конкретного метода получения биопсийного материала из четырех наиболее распространенных (трансбронхиальная биопсия, трансторакальная, видеоторакоскопическая и с использованием открытой биопсии) необходимо производить сучастием пульмонолога, рентгенолога, патолога и торакального хирурга.
Особое значение качество биопсии легких имеет при морфологической верификации ряда фиброзирующих альвеолитов, ранее объединяемых под рубрикой ИФА: обычная интерстициальная пневмония, десквамативная интерстициальная пневмония, респираторный бронхиолит, ассоциированный с ИБЛ, неспецифическая интерстициальная пневмония, острая интерстициальная пневмония (синдром Хаммена – Рича), идиопатический бронхиолит с организующейся пневмонией. Общей чертой этих заболеваний является мозаичность морфологических изменений в паренхиме легких.
Приведенные признаки предполагают морфологическую верификацию фиброзирующих альвеолитов при достаточно больших образцах легочной ткани, что невозможно получить спомощью трансбронхиальной биопсии. Так, в США диагностическим стандартом для больных ИБЛ является клиновидная резекция легких. В этом случае всегда надо сравнивать размер ущерба, наносимого больному методом исследования, с ущербом в результате неточной диагностики и, вследствие этого, ошибок в лечении.
Показаниями к инвазивным методам исследования являются:
– невозможность установления диагноза без инвазивных методов;
– необходимость выбора терапии;
– отсутствие признаков сотового легкого – конечной фазы большинства диффузных заболеваний легких.
При ИФА предполагается следующий набор признаков (косвенных), позволяющий верифицировать диагноз без морфологического подтверждения.
Диагностика ИФА без биопсии легких
Большие критерии:
1) исключение известных причин ИБЛ;
2) ФВД – рестрикция с нарушением газообмена;
3) КТ-картина – двусторонние ретикулярные тени в нижних отделах легких сминимальным проявлением «матового стекла»;
4) трансбронхиальная биопсия или бронхоальвеолярный лаваж не обнаружили признаков другого заболевания.
Малые критерии:
1) возраст моложе 50 лет;
2) постепенное начало необъяснимой одышки при нагрузке;
3) продолжительность болезни более 3 мес.;
4) двусторонние инспираторные хрипы в нижних отделах легких (сухие или «целлофановые»).
Диагностический алгоритм при работе сбольными ИБЛ должен состоять из 3 обязательных компонентов:
1) тщательное исследование анамнеза и клинической симптоматики;
2) проведение КТ;
3) исследование биопсийного материала.
Все остальные методы исследования вносят определенный вклад в диагностический процесс и должны использоваться в качестве дополнительных.
Основными компонентами дифференциальной диагностики ИБЛ являются изучение анамнеза, оценка клинической симптоматики, рентгенологическое, функциональное и лабораторное исследование и, наконец, биопсийное исследование. Ключевыми вопросами, подлежащими тщательному изучению при сборе анамнеза у больных ИБЛ, являются:
– факторы экологической агрессии;
– курение;
– наследственность;
– сосуществующие болезни;
– употребление лекарств в связи с сопутствующими болезнями;
– оценка последовательности, скорости появления и развития симптомов;
– установление времени начала болезни – архивные рентгенограммы;
– ответ на начальную терапию.
Изучение влияния факторов экологической агрессии позволяет облегчить диагностику пневмокониозов, экзогенных аллергических альвеолитов и радиационных поражений легких.
Наличие сосуществующей хронической болезни предполагает систематическое применение соответствующих лекарственных средств, некоторые из которых могут вести к формированию легочного фиброза как аллергической, так и токсической природы. Классическим примером является амиодароновый фиброзирующий альвеолит, нередко возникающий при длительном применении известного антиаритмического препарата кордарона (амиодарона).
Поскольку подавляющее большинство больных еще до верификации диагноза подвергаются медикаментозной терапии, важным является оценка ответа на антибактериальные средства и кортикостероиды. Очень демонстративным в этом отношении является экзогенный аллергический альвеолит, особенно его пневмоническая форма. Назначение таким больным антибиотиков обычно не дает выраженного лечебного эффекта, а некоторое смягчение симптоматики, связанное с прекращением контакта с бытовыми или профессиональными аллергенами в связи с госпитализацией, расценивается врачом как недостаточная эффективность антибиотиков. Далее следует наращивание интенсивности антибактериальной терапии, что непременно должно усугубить состояние больного. Подобная картина наблюдается в результате ошибочного назначения глюкокортикостероидов в качестве монотерапии больным диссеминированным туберкулезом, который был принят за саркоидоз легких. Напротив, эффективность глюкокортикоидов обычно предполагает иммунопатологический патогенез заболевания.
Лечение. В современных условиях тактика лечения больных определяется дифференцированно, в зависимости от патоморфологического варианта болезни. Так, десквамативная интерстициальная пневмония и неспецифическая интерстициальная пневмония хорошо отвечают на терапию глюкокортикостероидами. Как правило, иммуносупрессивная терапия при ИФА проводится длительно, в том числе в режиме высоких доз.
Среди препаратов с цитостатическими свойствами, также используемых при разных формах иммуновоспалительных заболеваний, в лечении ИФА особое место занимает колхицин. Основные направления терапии ИФА в современных условиях имеют целью ингибировать легочный фиброз и тем самым увеличить продолжительность жизни больных. Хотя есть сообщения о самопроизвольном излечении от ИФА, но среди больных, не получавших антифиброгенные препараты, показатели смертности выше по сравнению с получавшими терапию.
В литературе последних лет происходит интенсивное накопление новых данных о способах лечения ИФА (гамма-интерферон, цитокины, антиоксиданты, ингибиторы факторов роста, бозентан, эпопростенол, илопрост, пероральный простациклин, трептостинил). Выбор средств, влияющих на функциональную активность медиаторов воспаления и склероза при ИФА, уже сегодня раскрывает новые возможности для замедления темпов прогрессирования легочного фиброза.
Отсутствие доказанных причин заболевания позволяет говорить лишь о его патогенетической терапии, поэтому изучение этиологии, прежде всего инфекционной, следует считать наиболее важным направлением в лечебной стратегии ИФА.






