Глава V. Консервативное лечение хронического панкреатита
Общая оценка методов консервативной терапии хронического панкреатита.
Схема комплексного консервативного лечения заболевания. Применение ингибиторов трипсина.
Лечение панкреатита ветразином
Лечебные мероприятия при панкреатите могут принести успех лишь тогда, когда они основаны на данных патогенеза.
В настоящий момент достаточно достоверно известно, что:
хронический панкреатит чаще всего сочетается с заболеваниями желчных путей и двенадцатиперстной кишки;
в основе возникновения панкреатита лежат нарушения оттока панкреатического сока и желчи (моторные расстройства), вслед за которыми возникают расстройства секреторной деятельности поджелудочной железы;
заболевание поджелудочной железы сопровождается сравнительно рано наступающими расстройствами обмена (углеводного, белкового, водно-солевого);
заболевание поджелудочной железы сопровождается поступлением в кровоток некоторых веществ типа калликреина, нарушающих тонус сосудов;
наиболее вероятными причинами болей при панкреатите является переполнение системы протоков секретом и вовлечение в рубцовый процесс или воспалительный отек нервных окончаний, расположенных в ткани поджелудочной железы.
Таким образом, если в период обострения патологического процесса в поджелудочной железе основной целью
лечения должно быть подавление секреции поджелудочной железы, уменьшение явлений стаза в протоках и двенадцатиперстной кишке и ликвидация болей, то вне периода обострения лечение должно быть направлено на максимальное восстановление функций поджелудочной железы и устранение тех расстройств, которые наступили в результате нарушения ее внешне- и внутрисекреторной функции.
Наблюдения за больными хроническим панкреатитом, которым в клинике проводилось консервативное лечение, показывают, что успех его зависит от того, насколько удалось компенсировать нарушение метаболических процессов, снять болевой синдром, выявить и по возможности устранить ведущее звено в патогенезе страдания.
Под нашим наблюдением находилось 269 больных, которые были выписаны из клиники без операции после только консервативного лечения. Кроме того, всем оперированным больным, как правило, до и после операции назначали консервативное лечение. Наблюдение за этими больными позволяет высказать мнение о том, что консервативное лечение при хроническом панкреатите показано: в начальных стадиях заболевания, когда преобладают функциональные расстройства поджелудочной железы и других органов гепатопанкреатодуоденальной системы; подавляющему большинству больных, которым уже произведено то или иное оперативное вмешательство по поводу хронического панкреатита, необходимо подчеркнуть при этом, что сочетание некоторых консервативных методов с операцией способствует успеху оперативного лечения; в поздних стадиях панкреатита, когда имеются выраженные эндокринно-метаболические расстройства, операцию производят только по жизненным показаниям.
Наблюдение за больными с хроническим панкреатитом показывает, что периоды обострения заболевания чередуются у них с периодами ремиссии, иногда продолжающимися многие месяцы. Важнейшей задачей консервативного лечения хронического панкреатита является не только купирование обострения, но и его предупреждение. Это заставляет периодически повторять консервативное лечение, повторно госпитализируя больных еще до возникновения острых явлений. В таких случаях больные проводят в стационаре меньше времени и избегают тех страданий, которые несет им очередное обострение панкреатита.
Мы старались всем больным, поступающим в стационар, проводить консервативное лечение по разработанной нами схеме.
Принципиальная схема комплексного консервативного лечения больных хроническим панкреатитом
В период рецидива
1. Голодная диета 1—2 дня.
2. Пузырь со льдом на живот 3—4 раза в день по 2 ч.
3. Трасилол капельно на физиологическом растворе от 25 000 до-75 000 ед. 2 раза в сутки 3—5 дней.
4. Эуфиллин в 2,4% растворе внутривенно по 10 мл 1 раз в. день 3—5 дней.
5. Раствор сульфата атропина 0,1% по 1 мл 2 раза в день 3—5 дней.
6. 0,25% раствор новокаина по 100 мл внутривенно 2—3 дня.
7. 1% раствор промедола по 1—2 мл 1—2 раза в день 2—3дня.
8. Папаверин по 0,04 г 2—3 раза в день в течение 5 дней.
9. Плазма, другие белковые жидкости 200—300 мл 1 раз в день внутривенно в течение 2 дней.
10. Антибиотики широкого спектра действия до 1 млн. ед. н
сутки внутримышечно в течение 4—5 дней.
11. И. Антигистаминные препараты (ветразин, шшольфен, димедрол) первые 1—2 дня парентерально, затем по 1 таблетке-2 раза в день в течение последующих 2—3 дней.
12. 5% раствор аскорбиновой кислоты и растворы витаминов группы В по 2—3 мл 1 раз в день внутримышечно в течение 7—10 дней.
13. Щелочные минеральные воды (боржом) по 1 стакану 3 раза в день в течение 10 дней.
14. Паранефральные новокаиновые блокады (по показаниям)
В период ремиссии
1. Белковая диета.
2. Абомин (1 таблетка 3 раза в день в течение 7—10 дней), анаболический препарат, неробол, (0,005 г 2 раза в день в течение 15 дней).
3. Белковые препараты парентерально, переливание крови повторно.
4. Панкреатин, метионин, липокаин по 0,5 г 3 раза в день в течение 10—15 дней.
5. Рентгенотерапия на область солнечного сплетения, УВЧ-терапия.
6. Обезболивающие средства, антиспастические препараты, 0,1% раствор сульфата атропина по 7 капель на прием, но-шпа или никошпан по 1 таблетке 2—3 раза в день.
7. Теплые микроклизмы с антипирином (1,0 г) на настое ромашки (50,0 г) после очистительной клизмы.
8. Курортное лечение (Железноводск, Ессентуки, Дорохове,. Трускавец).
Соблюдение голодной диеты и пузырь со льдом всегда оказывали хороший эффект, особенно в сочетании со щелочными минеральными водами и препаратами атропинового ряда, которые подавляют секрецию и снимают спазм гладкой мускулатуры. Еще в начале века Старлинг показал, что соляная кислота стимулирует панкреатическую секрецию, потому применение щелочных вод и атропина дает, как правило, хороший лечебный эффект. Спустя трое суток после острого приступа больных начинали кормить.
В диетическом лечении больных хроническим панкреатитом мы так же, как и С. А. Тужилин, отдавали предпочтение белковой диете. Эту диету назначают своим больным очень многие авторы: Ф. К. Меньшиков, В. А. Шатерников, А. А. Шелагуров, М. А. Трунин и другие.
Так, больным разрешаются хлеб и хлебные изделия (хлеб белый черствый, сухари из белого хлеба, нежирное печенье), супы протертые, вегетарианские из овощей, круп, фруктов и молочные, мясные блюда из мяса нежирных сортов, курицы, кролика, рыбные блюда в отварном и рубленом виде, овощные блюда (салаты, винегреты, пюре, пудинги, суфле, запеканки), крупяные и мучные изделия в виде каш, пудингов и т. п., фрукты и ягоды натуральные и в виде компотов, киселей, муссов, желе, сахар, мед, варенье, разнообразные молочные продукты и яйца (молоко, творог, кефир, белковый омлет), чай, кофе с молоком, фруктовые и овощные соки.
Запрещаются торты, кондитерские изделия с кремом, сдоба; кислые и жирные щи и супы на крепком мясном или рыбном бульоне; жареное мясо, копченые колбасы, жирные сорта рыбы, консервы; квашеные и соленые овощи, острые маринады; желтки яиц, животные жиры, приправы — хрен, перец, горчица, лук, чеснок; вино и спиртные напитки.
Диета должна удовлетворять следующим требованиям: прием пищи должен быть пятиразовым; пища не должна быть слишком горячей или холодной; при обострении заболевания продукты, входящие в состав пищи, должны быть хорошо измельчены или протерты.
Когда нет обострения хронического панкреатита, калорийность пищи должна соответствовать энергетическим затратам человека; дневной рацион нужно равномерно распределять на пять приемов пищи.
У больных с хроническим панкреатитом значительно нарушается всасывание витаминов в кишечнике. Поэтому мы предпочитаем парентеральное введение витаминов С, Bi, Вб, Bi2, а также включаем их при лечении другими препаратами.
Для устранения внешнесекреторной недостаточности поджелудочной железы назначаем препараты самой железы: панкреатин (0,5 г по 3 раза в день). Это усиливает переваривание жиров, что сказывается на самочувствии больных, повышает аппетит, способствует исчезновению или ослаблению болей, нормализации стула.
Для усиления образования фосфолипидов и задержки перехода углеводов в жиры назначают липокаин по 0,35 г 2 раза в день. Хороший эффект дает систематическое употребление свежего творога, лечение белковыми препаратами (переливание нативной плазмы, белковых гидролизатов) переливания свежей крови. После повторного вливания больным 250 мл крови их самочувствие, как правило, улучшалось.
Если хронический панкреатит сопровождается воспалительными явлениями со стороны желчевыделительной системы и панкреатических протоков, то для предупреждения осложнений необходимо лечение антибиотиками (ауро-мицин, левомицетин, биомицин, тетрациклин и пр.).
Наибольший эффект мы видели от применения препаратов широкого спектра действия — гликоциклина, ауромикаина, сигмамицина, тетраолеана, неомицина, олеоморфоциклина и т. д.
У больных хроническим панкреатитом, сочетающимся с заболеванием холедуоденальной системы, хороший эффект был получен от применения желчегонных (холензим, сернокислая магнезия, холосас, холагол, аллохол, настой бессмертника, кукурузных рылец и т. д.).
В последние годы при хроническом панкреатите стали широко применять антиферментную терапию (трасилол, цалол, инипрол, зимофрен, контрикал).
В результате многолетней работы Верле, Майер, Рингельман в 1952 г. выделили инактиватор трипсина из тканей животных в чистом виде. В 1953 г. Фрей впервые применил инактиватор трипсина при лечении острого панкреатита, а в 1959 г. фирма «Байер» (ФРГ) выпустила препарат трасилол. Мы имеем значительный опыт применения трасилола при остром панкреатите (см. журнал «Хирургия», 1967, № 9, с. 79). Клинические наблюдения показали, что наибольший эффект трасилол дает при его внутривенном введении в среднем по 75 000 ед. в сутки до исчезновения болей и нормализации цифр диастазы мочи.
При обострении хронического панкреатита (эквивалент острого) применялись несколько меньшие дозы трасилола, чем при остром. В этих случаях суточная доза трасилола составляла 30 000—50 000 ед.; на курс лечения требовалось 150 000—250 000 ед. Лечение проводили в комплексе с другими средствами консервативной терапии.
Консервативное лечение без применения трасилола не всегда эффективно. Трасилол инактивирует трипсин и калликреин, в результате чего приостанавливается процесс самопереваривания поджелудочной железы и предупреждается переход отечной формы в некротическую. Трасилол, как правило, эффективен при отечной форме, когда еще нет геморрагического некроза и не произошла активация в крови липазы, вызывающей жировой некроз.
При хроническом панкреатите трасилол был применен 49 раз: 36 раз — при рецидивах заболевания или в послеоперационном периоде и 13 раз — в период ремиссии. Б начале нашей работы мы специально выделили две группы больных по 10 человек в каждой. Одна группа больных получала трасилол в период ремиссии, другая — нет. Сложилось впечатление, что не получавшие трасилол поправлялись быстрее. Этот феномен мы попытались объяснить тем, что трасилол, инактивируя последние дозы ферментов, оставшиеся в склеротически пораженной поджелудочной железе, лишает ее последней возможности участвовать в пищеварении, осуществляя внешнесекреторную функцию. Курс трасилолотерапии, проведенный больным с рецидивом заболевания, как правило, давал выраженный терапевтический эффект.
За последнее время в лечении хронического панкреатита мы довольно широко стали пользоваться ветразином.
Отечественный ингибитор моноаминоксидазы ветразин был синтезирован в 1957 г. А. И. Кост и Р. С. Сагитулиным, его свойства были изучены на кафедре фармакологии фармацевтического факультета I Московского медицинского института им. Сеченова (проф. А. Н. Кудрин),
Согласно гистохимическим исследованиям Г. Ф. Лушяикова, ветразин, угнетая моноаминоксидазу сердца, оказывает избирательное действие на сердечную деятельность С сохранением функции окислительных систем. Однако нас привлекла еще одна важная особенность ветразина: его антигистаминное, антиаллергическое и противовоспалительное действие.
Г. Н. Акжигитов (1967) применил ветразин у 30 больных с отечной формой острого панкреатита и только у двух не было положительного эффекта. Для сравнения проводилось лечение без ветразина у 40 больных. При лечении ветразином скорее прекращались боли, нормализовалась температура, что говорило о стихании острых явлений. Ветразин препятствовал переходу острого панкреатита в хроническую форму. Автор обратил внимание па особо благоприятный эффект от ветразина у больных в тех случаях, когда панкреатит сочетался с заболеванием сердечно-сосудистой системы.
Мы применили ветразин у 24 больных с хроническим панкреатитом в период ремиссии заболевания (8) и в период рецидивов (16). Препарат давали по 1 драже 3 раза в день 4—5 дней либо в инъекциях по 1,0 мл 0,5% раствора два раза в день.
В качестве тестов изучали внешнюю и внутреннюю секрецию поджелудочной железы, гемодинамические показатели, изменения периферической крови и мочи.
Из 24 больных только у одного не было отмечено положительного эффекта. У 19 больных эффект от лечения ветразином был хороший, а у 4 — удовлетворительный.
Применение новокаиновых блокад
При острых и хронических панкреатитах вследствие изменяющихся условий деятельности поджелудочной железы, нарушения ее иннервации, выраженного болевого синдрома, значительной функциональной перегрузки с преобладанием спазматического компонента важное значение приобретает новокаиновая блокада — проверенный временем лечебный фактор, обладающий, как правило, хорошим терапевтическим эффектом. Мы применяли различные виды новокаиновых блокад в лечении больных хроническим панкреатитом как в фазе рецидива, так и в стадии ремиссии.
Ряд хирургов для этой цели рекомендуют поясничную новокаиновую блокаду (Г. М. Новиков, А. Н. Новиков, С. Г. Рукосуев, К. Д. Тоскин, Н. И. Краковский, Ф. В. Мазина и др.); другие видят наибольший эффект рт пенициллин-новокаиновой блокады (Н. П. Шастин, А. М. Трофимов, Ф. Г. Власов и др.), третьи предпочитают вагосимпатическую блокаду (М. И. Коломийченко, Г. Г. Корованов, В. В. Виноградов и др.), четвертые — блокирование только блуждающего нерва (Keith, Bonta, Feriss и др.). Drost, Г. С. Лупенко и др. рекомендуют применение веществ, блокирующих передачу импульсов в симпатической нервной системе.
В 1951 г. В. В. Мосиным была предложена и экспериментально разработана новокаиновая блокада чревных нервов и пограничных симпатических стволов для профилактики и лечения воспалительных заболеваний брюшины и органов брюшной полости. Автор предложил надежный метод охранительного влияния на нервную систему, защищающий кору головного мозга от перераздражения импульсами, поступающими из брюшной полости. Влияя преимущественно на симпатические волокна, эта разновидность новокаиновой блокады оставляет почти интактными парасимпатические нервы, в частности блуждающий нерв. В дальнейшем Д. Ф. Благовидов развил и применил блокаду чревных нервов при лечении перитонитов.
Несколько раньше заплевральная блокада чревных нервов была разработана Лабо.
Мы использовали несколько вариантов новокаиновых блокад для лечения больных хроническим панкреатитом.
Новокаин в 0,25% или 0,5% растворе вводили внутривенно, капельно, в виде вагосимпатической блокады, паранефральной новокаиновой блокады по методике А. В. Вишневского и, наконец, в виде заплевральной новокаиновой блокады по Лабо — Мосину. Методики применения всех упомянутых новокаиновых блокад известны, остановимся на технике выполнения заплевральной новокаиновой блокады. На расстоянии 5—6 см от линии остистых отростков делают «лимонную корочку» по наружному краю длинной мышцы спины (положение больного на правом боку). Иглу длиной 10—20 см продвигают в ткани под углом 45° кнутри и кверху до соприкосновения с поперечным отростком XI грудного позвонка, вернее, с головкой XI ребра. После соприкосновения с костыа направление иглы меняют, ориентируясь на боковую поверхность тела позвонка. Предпосылая движению иглы раствор новокаина, продвигают иглу вперед, медиально и кверху до нового соприкосновения с костью — телом XI грудного позвонка, затем, чуть извлекая иглу, вводят туда 50—100 мл 0,25% раствора новокаина. При этом иногда можно проколоть париетальную плевру, особенно если иглу вкалывать дальше края длинной мышцы спины от линии остистых отростков. У больных в этот момент возникает одышка, появляется кашель и боль, однако скоро все проходит.
Д. Ф. Благовидов (1955) изучал распространение новокаина при его заплевральном введении и выяснил, что новокаин выходит далеко за пределы инъекции, вверх до уровня VI—VII грудных позвонков и спускается ниже диафрагмы вплоть до надпочечников. При этом в зоне действия раствора оказываются не только оба чревных нерва, но и симпатический ствол, его соединительные ветви, нисходящая ветвь грудной аорты, межпозвонковые узлы и межреберные нервы. Это доказывает, что заплевральная блокада чревных нервов действует на многочисленные соматовегетативные образования не только заплевральной, но и забрюшинной области.
Мы применяли различные виды новокаиновых блокад у 114 больных хроническим панкреатитом во время выраженного болевого приступа, исключая вагосимпатическую блокаду, так как считаем ее нецелесообразной. Г. Н. Акжигитов, используя вагосимпатическую блокаду при остром панкреатите, отмечал, что последняя подавляет функцию коры надпочечников, снижает уровень 17-окси-кортикостероидов в периферической крови. Однако и он считает, что для лечения панкреатитов этот вид новокаинового блока мало пригоден. В период обострения заболевания 77 больным внутривенно вводили коктейль: изотонический раствор хлорида натрия 500 мл, 2,4% раствор эуфиллина 10 мл, 0,25% раствор новокаина 100 мл, 5% раствор аскорбиновой кислоты 4 мл, 5% раствор витамина Bi 2 мл, 100 мкг витамина Bi2, трасилол 25 000 ЕД, 0,1% раствор сульфата атропина 2 мл.
Как правило, капельное введение этой смеси постепенно снимало боль, больные успокаивались и засыпали.
У 38 больных хороший эффект наступил после паранефральной блокады по Вишневскому.
Мы обычно делали левостороннюю блокаду, но иногда выполняли ее и с обеих сторон, вводя в околопочечную клетчатку по 80 мл 0,25% раствора новокаина. После блокады у больных, как правило, утихали боли, разрешалась атония кишечника (исчезало мучительное чувство распираний в животе), они переставали страдать от сухости языка и полости рта, проходила одышка, несколько снижалось артериальное давление.
Показателен следующий пример.
Больная А., 26 лет, медицинская сестра, в течение 2 лет страдает хроническим панкреатитом. Год назад был удален желчный пузырь; обнаружены явления индуративного панкреатита.
В клинику больная переведена в связи с периодическими приступами болей такой интенсивности, что она теряла сознание, причем препараты группы пантопона, промедола и т. п. не давали эффекта. Мы 4 раза наблюдали такие приступы, длившиеся от 40 мин до 2 ч. Последний перед операцией приступ был спровоцирован введением 2 мл билигноста с целью проверки чувствительности к йоду. Приступ длился около 3 ч, сопровождался коллапсом и потерей сознания. Трижды больной были проведены двусторонние паранефральные блокады, которые каждый раз давали хороший эффект: боли постепенно стихали, больная успокаивалась и засыпала. На операции у нее был найден индуративный панкреатит, папиллит; наложен билиодигестивный анастомоз. Больная через месяц выписалась без жалоб на боли.
Заплевральную блокаду чревных нервов мы выполнили у 41 больного с болевой формой хронического панкреатита. По нашему мнению, наступающая анестезия чревных нервов надолго (15—30 дней) снимает болевой синдром. У 11 больных введение новокаина сопровождалось кратковременной острой болью, причем, как описывают больные, «несколько минут было нечем дышать». У одной больной 65 лет введение новокаина вызвало падение артериального давления со 170/85 до 100/50 мм рт. ст. и кратковременную потерю сознания. У 36 из 41 больного удалось добиться стойкого обезболивающего эффекта и спустя час — два после блокады — улучшения самочувствия на 2—3 нед.
Таким образом, применение различных новокаиновых блокад при воспалительных процессах в поджелудочной железе вполне оправдано.
В условиях блокады улучшается трофика поджелудочной железы и регуляция ее внешней и внутренней секреции. Это мы видели по изменяющимся углеводным кривым, улучшению аппетита, снижению диспепсических расстройств, снятию болевого синдрома. Вагосимпатическая блокада, видимо, при хронических панкреатитах не показана, так как подавляет функцию коры надпочечников, которая и так истощается при длительном страдании.
Введение новокаина внутривенно в составе различных спазмолитических коктейлей оправдано, так как новокаин, воздействуя на вазорецепторы, нормализует их тонус, находящийся при обострении панкреатита под постоянной угрозой в связи с выработкой и поступлением в кровь кининов (брадикинин, калликреин, каллидин и т. п.). Новокаиновый блок целесообразно применять при обострениях заболевания, в период панкреатического криза.
Паранефральные новокаиновые блокады при панкреатитах, как правило, давали благотворный обезболивающий эффект. Применение этого вида блокад можно рекомендовать как при рецидиве, так и при ремиссии заболевания.
Заплевральную новокаиновую блокаду чревных нервов нельзя применять при остром панкреатите или рецидиве хронического заболевания, когда сосудистый тонус снижен или находится под угрозой снижения. Этот вид блокады может вызвать снижение артериального давления вплоть до коллапса. Заплевральный новокаиновый блок показан у больных хроническим панкреатитом, не имеющих сниженного артериального давления, при сильном болевом синдроме.
Воздействие холинолитиков на моторику двенадцатиперстной кишки
В главе «Диагностика хронического панкреатита» мы приводим данные по исследованию моторно-эвакуаторной функции двенадцатиперстной кишки баллонокимографическим способом. Из этих данных следует, что у 41 больного из 68 обследованных был зарегистрирован гипокинетический или акинетический тип моторики, 28 больных из этой группы страдали хроническим панкреатитом. Иными словами, было установлено, что при хроническом панкреатите двенадцатиперстной кишке присущи гипотонические и даже атонические состояния. В этих случаях явления недостаточности фатерова соска преобладают над явлениями стеноза, давление в двенадцатиперстной кишке превышает давление в желчных протоках, что приводит к хроническому инфицированию кишечным содержимым общего желчного и вирсунгова протоков. Этим состоянием поддерживается хронический панкреатит.
Учитывая благотворное действие нейротропных спазмолитиков при заболеваниях желудочно-кишечного тракта, мы применили эти препараты у больных с заболеваниями панкреатодуоденальной зоны, в частности у больных хроническим панкреатитом.
Как известно, передача нервных импульсов желудочно-кишечному тракту осуществляется через холинореактивные и симпатические системы. Блокада холинореактивных структур с помощью холинолитиков обеспечивает органам,
вовлеченным в патологический процесс, необходимый функциональный лечебный покой.
Действие нейротропных спазмолитиков при различных заболеваниях желудочно-кишечного тракта общеизвестно. Эти средства в лечебных целях используют многие авторы и в комплексной терапии хронических панкреатитов. В главе «Диагностика» мы показали, что применение холинолитиков возможно в диагностических целях, для дифференциации функциональных и органических состояний двенадцатиперстной кишки. Оказалось, что препараты - холинолитики оказывали на моторику двенадцатиперстной кишки различное влияние в зависимости от исходного фона дуоденокинезиограммы. Этот эффект мы и использовали в лечении больных хроническим панкреатитом преимущественно в ранней стадии заболевания.
Препараты группы атропина применяли в сочетании с другими консервативными методами лечения: белковой диетой (150 г белка в сутки), парентеральной белковой терапией (аминопептид, кровь, плазма), витаминами (особенно С и группы В); при рецидивах — трасилол, новокаиновые блокады, седативные, сердечные средства, панкреатин, анаболические гормоны, антибиотики.
Применение нейротропных спазмолитиков мы считаем обязательным как в период обострения заболевания, так и при ремиссии. При рецидивах, сопровождающихся выраженным болевым синдромом, с целью снятия спазма сфинктера Одди назначаем 2,4% раствор эуфиллина (10 мл внутривенно) и 0,1% раствор сульфата атропина (1 мл под кожу, обычно в сочетании с промедолом). В последующие дни заболевания сульфат атропина назначают с целью подавления секреции желудочного сока.
У большинства больных препараты группы атропина были применены в комплексе с другими средствами лечения. Как правило, введение холинолитиков давало выраженный клинический эффект — уменьшались боли, исчезали диспепсические расстройства, улучшался аппетит. У больных с давностью заболевания не более полутора лет введение препаратов группы атропина приводило обычно к нормализации показателей внешней и внутренней секреции поджелудочной железы, к изменению моторной деятельности двенадцатиперстной кишки.
У больной Ж., 35 лет, поступавшей в стационар с обострением панкреатита трижды, рентгенологически был выявлен дуоденальный стаз, отмечалось повышение диастазы в моче и изменение сахарной кривой с двойной нагрузкой. Изучение моторики двенадцатиперстной кишки показало наличие гипокинетического типа дуоденокинезиограммы. Применение 0,1% раствора сульфата атропина у этой больной в течение 7 дней привело к исчезновению болей, диастаза снизилась до 16 ед., сахар крови стал равен 0,9 г/л, рентгенологически скорость пассажа через двенадцатиперстную кишку приблизилась к норме. Повторная запись моторики двенадцатиперстной кишки показала нормализацию кривых, углубление и усиление перистальтических волн.
У 41 больного мы применяли холинолитики и одновременно производили дуоденокинезиографию, что позволило графически регистрировать получаемый эффект (табл. 4).
Таблица 4 Влияние холинолитиков на моторику двенадцатиперстной кишки при подкожном введении

Мы пользовались различными холинолитиками — апролидином, апрофеном, атропином и ацеклидином, что видно из табл. 4. Больным под кожу вводили 0,1—0,2% растворы препаратов (апрофен в 1% растворе) в дозе 1мл.
Латентный период был различным для разных препаратов, в среднем 5—10 мин, продолжительность действия — от 10 до 50 мин.
При исходном нормокинетическом фоне дуоденокинезиограммы эффект от применения холинолитиков был типичен: мы наблюдали угнетение моторной деятельности — феномен, издавна присущий препаратам этой группы. Применение атропина при гиперкинетическом типе моторики также вызвало угнетение моторики. У больных же с хроническим холецистопанкреатитом и с гипокинетическим типом моторики введение холинолитиков вызвало не угнетение, а усиление моторной деятельности, которое продолжалось от 3 до 15 мин.
У больных с акинетическим или гипокинетическим типом моторики двенадцатиперстной кишки, страдавших хроническим панкреатитом или холепанкреатитом, применение холинолитиков не ослабляло, а нормализовало и в ряде случаев усиливало моторную деятельность кишки, давая выраженный терапевтический эффект.
Больная Б., 38 лет, около 4 лет лечится в различных стационарах по поводу хронического панкреатита. При обследовании этой больной наряду с лабораторными данными (снижение триптической и амилолитической активности секрета поджелудочной железы, диабетическая сахарная кривая, стеаторея, креаторея и т. п.) при дуоденокинезиографии был обнаружен акинетический (атонический) тип моторики. Стало ясно, что в основе хронического панкреатита у этой больной лежит атония двенадцатиперстной кишки, что приводит к функциональной недостаточности сфинктера Одди и к хроническому инфицированию вирсунгова протока застойным кишечным содержимым. Введение ацеклидина у этой больной привело к нормализации, а затем и к усилению моторики (рис. 34).
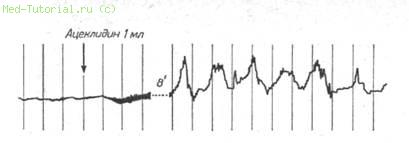
Рис. 34. Дуоденокинезиография. Усиление моторики двенадцатиперстной кишки у больной Б., 38 лет, после введения ацеклидина.
После исследования холинолитики были включены в состав комплексной терапии. Больная получала сульфат атропина по 1,0 мл 0,1% раствора 2 раза в день в течение 3 дней, затем по 0,5 мл 2 раза в день 2 дня и, наконец, по 0,5 мл ежедневно в течение 2 дней. Боли стихли, прошли мучительные диспепсические явления, наладился стул, сон и аппетит, больная была выписана домой с улучшением, хотя углеводная кривая осталась прежней, сохранив диабетический характер.
Таким образом, при хроническом панкреатите и холецистопанкреатите двенадцатиперстной кишке присущи гипотонические и атонические состояния, вызывающие функциональную недостаточность сфинктера Одди и хроническое инфицирование застойным кишечным содержимым желчных протоков и протоков поджелудочной железы.
Нейротропные холинолитики, угнетающие в норме моторику двенадцатиперстной кишки, при подкожном введении больным с гипокинетическим и акинетическим типом моторики нормализуют или усиливают моторную функцию двенадцатиперстной кишки, что целесообразно использовать для лечения больных в ранних стадиях хронического панкреатита.
Благотворный лечебный эффект холинолитиков при хроническом панкреатите связан, вероятно, с блокированием патологических импульсов в ганглиях и коре головного мозга, что приводит к своеобразному торможению в системе мионевральных синапсов желудочно-кишечного тракта, нормализуя их ритм и усиливая моторно-эвакуаторную функцию.
Электростимуляция двенадцатиперстной кишки
Другим не менее эффективным средством усиления моторики двенадцатиперстной кишки при ее гипокинетических состояниях является раздражение кишечной стенки слабым разрядом электрического тока (электростимуляция) .
В главе «Диагностика хронического панкреатита» мы описали анатомо-физиологическую сущность водителя кишечного ритма, расположенного в мышечном слое двенадцатиперстной кишки. Было показано, что при воздействии на него слабыми импульсами электрического тока удается изменить ритм моторики, усиливая его при гипокинетических состояниях кишечной стенки. Это свойство мы использовали для дифференциации ранних и поздних стадий панкреатита, протекающих соответственно при большем или меньшем вовлечении в основной процесс двенадцатиперстной кишки.
Электростимуляция двенадцатиперстной кишки была применена с лечебной целью у 32 больных с ранними стадиями хронического панкреатита и сопутствующими заболеваниями желчных путей.
Больным контрольной группы электростимуляция двенадцатиперстной кишки применялась при нормокинетическом типе дуоденокинезиограмм. У этой группы больных было зарегистрировано некоторое усиление моторики кишки в ответ на поток электроимпульсов, но этот эффект был выражен меньше и поэтому продолжать электростимуляцию мы сочли нецелесообразным.
Из 29 остальных больных (25 женщин и 4 мужчин в возрасте от 26 до 57 лет) давность заболевания хроническим панкреатитом у 7 была до 1 года, у 16 — от 1 года до 5 лет и у 4 — от 5 до 10 лет, двое больных страдали хроническим панкреатитом более 10 лет.
В отечественной литературе нам не встретилось работ, в которых бы электростимуляция двенадцатиперстной кишки применялась в клинике в целях активизации ее моторной деятельности. Поэтому наши данные мы подвергли клиническому анализу для комплексной оценки эффекта электростимуляции с учетом лабораторных данных и операционных находок. Из 29 больных со сниженной моторикой двенадцатиперстной кишки электростимуляция у 7 человек не дала почти никакого результата: акинетический фон кривых под влиянием повторно посылаемых электрических импульсов незначительно изменился у 2 и совсем не изменился у 5 больных.
У 22 больных электростимуляция вызвала значительное усиление моторики с нормализацией характера, силы и ритма перистальтических волн. На рис. 35 приведена дуоденокинезиограмма больной Я., 28 лет, страдающей хроническим панкреатитом 2 года. Исходный фон дуоденокинезиограммы приближался к прямой линии, однако повторная электростимуляция двенадцатиперстной кишки током силой от 5 до 10 |ЛА быстро изменила характер моторики, которая затем оставалась активной в течение нескольких часов.
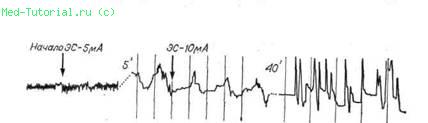
Рис. 35. Дуоденокинезиография. Усиление моторики двенадцатиперстной кишки у больной Я., 28 лет, после электростимуляции.
У части больных электростимуляцию проводили повторно, через 1—2 дня, для более настойчивого навязывания кишечнику адекватного ритма сокращений. У тех больных, у которых ослабленная моторика особенно активно реагировала на электростимуляцию, мы получали и наибольший клинический эффект: уменьшение болей, улучшение аппетита, исчезновение чувства тяжести в подложечной области, отрыжки и метеоризма. У этих больных менялся характер секреции поджелудочной железы, нормализовались эндокринные и метаболические процессы.
Эффект от электростимуляции был особенно разительным, когда хронический панкреатит протекал на фоне хронического колита (рис. 36).
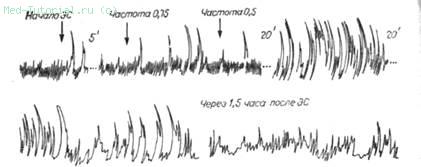
Рис. 36. Дуоденокинезиограмма. Выраженный эффект электростимуляции двенадцатиперстной кишки у больной Ч., страдающей хроническим панкреатитом (гипокинетический тип моторики).
Воздействуя на водитель кишечного ритма у этой группы больных, мы получали не только усиление моторной деятельности двенадцатиперстной и тонкой кишки, но и нормализацию работы толстой кишки в виде самостоятельного стула.
Примером может служить следующее наблюдение.
Больная Ч., 39 лет, страдающая несколько лет хроническим панкреатитом, последние 4 года ни разу не имела стула без клизмы, иногда стула не было по 4—5 сут. Уже при первом сеансе элекгростимуляции больная отметила усиление перистальтики, вечером у нее впервые был самостоятельный стул. После 5 сеансов электростимуляции стул окончательно нормализовался и в течение года больная больше не пользовалась клизмой. Обследование через год выявило улучшение объективных показателей; состояние больной также намного улучшилось.
У части больных, страдающих запорами, мы совместно с В. Ф. Смирновым и М. М. Орешенковым провели одновременную запись моторики двенадцатиперстной кишки и толстой кишки. При этом найдена определенная закономерность между тяжестью хронического панкреатита и длительностью запора. Запоры часто имели место у больных с функциональной, отечной формой хронического панкреатита, когда консервативные методы лечения еще эффективны. Именно в этих случаях стимуляция водителя кишечного ритма в зоне фатерова соска приводила к нормализации деятельности толстого кишечника с изменением многих биохимических и ферментативных показателей.
Влияние холинолитиков и электростимуляции двенадцатиперстной кишки на нормализацию ее моторно-эвакуаторной функции мы представляем в в
