Воспалительный процесс: общий знаменатель
Всем известно, что такое воспаление. Сам термин происходит от латинского глагола inflammare, что означает «воспламенять», «разжигать». Воспаленная ткань «горит» — и далеко не положительным образом. Комплекс воспалительной реакции может включать красноту, жар, опухоль, которые сопровождают укус насекомого или боль, например от воспаленного горла или растянутой лодыжки. Обычно мы признаем, что укус насекомого или царапина на коже доставляют болевые ощущения из-за воспалительного процесса. При этом воспаление — часть гораздо большего количества процессов, чем вы можете себе представить. На самом деле в этом суть лечения — привлечь больше иммунной активности к месту травмы или инфекции. Однако когда воспаление продолжается глубоко внутри организма и по общесистемным траекториям или не имеет определенной цели, оно провоцирует различные заболевания, в том числе ожирение, диабет, рак, депрессию, аутизм, астму, артрит, коронарную недостаточность, рассеянный склероз и даже болезни Альцгеймера и Паркинсона.
Остановимся на болезни Альцгеймера. Воспалительный процесс — это то, что происходит в мозге пациента с этим диагнозом. Я понимаю, что в этом случае может быть очень сложно определить очаг воспаления, потому что привычные симптомы воспалительного процесса, такие как боль и опухоль, не очевидны. В головном мозге, способном воспринимать сигналы о боли во всем организме, нет болевых рецепторов, из-за чего он не в состоянии зафиксировать собственную проблему. Тем не менее на протяжении нескольких последних десятилетий результаты научных исследований вновь и вновь неоспоримо свидетельствуют, что воспаление — фундаментальный процесс, лежащий в основе развития болезни Альцгеймера{61}.
С воспалительным процессом как в головном мозге, так и в организме в целом связаны многие биохимические элементы. У пациентов с болезнью Альцгеймера количество биохимических элементов, указывающих на протекание воспалительного процесса — так называемых биохимических маркеров, — повышено и даже может служить для прогнозирования снижения когнитивных функций мозга и развития деменции. К наиболее известным биохимическим маркерам относятся цитокины — крошечные белки, которые синтезируются клетками, влияют на поведение других клеток и часто становятся важными участниками воспалительного процесса. С-реактивный белок, интерлейкин-шесть (ИЛ-6) и фактор некроза опухолей-альфа (ФНО-альфа, или TNF-?) — все относятся к цитокинам. Сегодня существует возможность получить изображение головного мозга таким образом, чтобы наблюдать эти биохимические маркеры в действии, так что можно определить прямую взаимосвязь между степенью воспалительного процесса и степенью нарушения когнитивных функций мозга.
TNF-? играет особенно важную роль при воспалительных процессах в организме. Его уровень в крови бывает повышенным не только у пациентов с диагнозом «болезнь Альцгеймера», но также при других самых различных воспалительных состояниях, в том числе при псориазе, ревматоидном артрите, заболеваниях сердечно-сосудистой системы, болезни Крона и астме{62},{63}. Роль TNF-? настолько велика, что фармацевтические компании инвестируют огромные средства, пытаясь найти способ снизить уровень этого цитокина. Глобальный рынок для ингибиторов TNF сегодня превышает 20 миллиардов долларов ежегодно{64}.
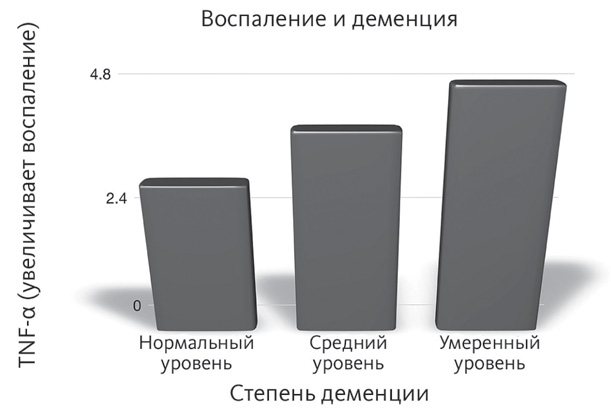
У некоторых людей на естественное усиление воспалительного процесса в организме оказывает влияние генетический фактор, повышающий риск развития заболеваний, в основе которых лежит воспалительный процесс{65}. Однако генетический фактор — это только часть истории. Вы можете сделать очень многое, чтобы повлиять на экспрессию генов: от «отключения» или подавления «плохих» генов до «включения» «полезных», которые помогут поддержать ваше здоровье.
В своей предыдущей книге, «Еда и мозг», я провел глубинный анализ одного из наиболее действенных и фундаментальных способов, с помощью которого можно поддержать экспрессию «полезных» генов и подавить «плохие», а также держать под контролем воспалительный процесс, если в нем нет необходимости для выживания. Этот способ — поддержание здорового уровня сахара в крови. Повышенный уровень сахара провоцирует воспаление в токе крови, поскольку избыток сахара может быть токсичен, если он не используется клетками организма. Он также вызывает реакцию под названием «гликирование» — биологический процесс, при котором сахар связывается с молекулами белков и некоторых жиров, результатом чего становятся деформированные молекулы, не способные выполнять свои функции. Эти связанные сахаром белки технически носят название «конечные продукты усиленного гликозилирования (AGEs)». Организм не воспринимает их как нормальные клетки, поэтому они вызывают воспалительную реакцию. В головном мозге соединение молекул сахара и белков головного мозга приводит к формированию новых летальных структур, вызывающих дегенеративные изменения в функциях головного мозга.
Корреляция между слабым контролем уровня сахара в крови и болезнью Альцгеймера в частности настолько сильна, что сегодня ученые даже называют последнюю диабетом III типа{66}. Хотя научные работы, впервые выявившие это явление, проводились около десяти лет назад, современные исследования внесли еще большую ясность в общую картину. Было обнаружено, что изменение микробиоты кишечника — прямой путь к развитию разных форм диабета и повышению количества AGEs, что, в свою очередь, повышает риск болезни Альцгеймера. Подробнее на деталях этого процесса я остановлюсь в главе 4, а сейчас изложу его суть.
В 2012 году в журнале Nature были опубликованы результаты исследования, согласно которым у пациентов с диагнозом «диабет II типа» также наблюдается бактериальный дисбаланс (дисбактериоз) в кишечнике{67}. Из-за дисбактериоза у них снижен уровень важных побочных продуктов жизнедеятельности кишечных бактерий, необходимых для поддержания здоровья клеток пищеварительной системы. Стоит учесть, что организм пациентов с диабетом II типа испытывает огромный метаболический стресс, так как у них нарушен процесс транспортировки глюкозы из тока крови в клетки. А в областях организма, не имеющих системы транспортировки глюкозы, например в нервах и головном мозге, ученые обнаружили другие формы метаболического стресса, в частности AGEs, которые способны вызывать различные состояния, включая периферическую невропатию (слабость, онемение и боль, вызванную поврежденными нервами), а также разрушать кровеносные сосуды и приводить к нарушениям функций головного мозга.
По моему мнению, это открытие было прорывным. Мне кажется по крайней мере поразительным осознание, что в основе целого каскада событий, ведущих к диабету разного типа и болезням головного мозга, лежит дисбаланс микрофлоры кишечника. Мне очень нравится, как группа китайских исследователей недавно изложила суть дела в отчете, опубликованном в престижном журнале Food Science and Human Wellness{68}:
В последнее время значительный прогресс достигнут в области изучения микробиоты кишечника у пациентов с диабетом II типа. Микробиота кишечника способствует не только возникновению незначительного воспалительного процесса в начале заболевания диабетом II типа, но и последующему развитию этого заболевания из-за воспалительных компонентов. Кроме того, она влияет на развитие различных осложнений, сопутствующих диабету II типа, в том числе диабетической ретинопатии, почечной токсичности, атеросклероза, гипертонии, трофических язв ног, муковисцидоза. В этих исследованиях подчеркивается важнейшая роль микробиоты кишечника в поддержании целостности кишечного барьера, нормального метаболического гомеостаза, обеспечении защиты организма-хозяина от инфекций, вызванных патогенными микроорганизмами, повышении функций защитных систем организма-хозяина и даже в оказании влияния на нервную систему при диабете II типа.
Далее ученые анализируют важнейшую роль рациона питания в улучшении состояния микрофлоры кишечника и снижении риска развития этих осложнений. Они также отмечают, что различные травы и пищевые добавки, известные своими антидиабетическими свойствами, контролируют уровень сахара в крови через микрофлору кишечника. Иными словами, они не обязательно напрямую влияют на инсулин и глюкозу, а скорее оказывают позитивный эффект на микрофлору кишечника. Например, традиционные для китайской медицины компоненты берберин и женьшень, а также элементы, содержащиеся в чае, кофе, вине и шоколаде, обладают антидиабетическими свойствами благодаря эффекту, который они оказывают на кишечные бактерии. Эти компоненты изменяют к лучшему состав кишечных бактерий или же метаболизируют их до того, как они абсорбируются организмом человека. Практики китайской медицины, основанные на травах и применяющиеся уже не одно тысячелетие, наконец начали получать объяснение, которого они заслуживают. В первую очередь травяные компоненты этих средств оказывают положительное влияние на бактерии кишечника, так что от этого получает пользу весь организм.
Доктор Джеймс Хилл, старший научный сотрудник и профессор нейронауки Медицинской школы Университета штата Луизиана, руководит одной из высокотехничных лабораторий, занимающихся изучением взаимосвязи между микрофлорой кишечника и риском развития болезней головного мозга. Недавно доктор Хилл опубликовал научную работу, в которой описал многочисленные способы влияния происходящего в кишечнике человека на функции головного мозга{69}. В своих исследованиях на основании моделей с мышами он изучил, как «полезные» кишечные бактерии способны производить важные химические элементы, такие как белок BDNF, гамма-аминомасляная кислота (ГАМК, или GABA) и глутамат. Уровень этих важных химических элементов напрямую отражает, что происходит в организме с точки зрения микрофлоры кишечника: когда исследователи изменяли состав микрофлоры у мышей, то наблюдали не только изменения в поведении подопытных грызунов, но также фиксировали изменения в уровне этих химических элементов.
Как уже упоминалось ранее, нейротрофический фактор мозга — белок, критически важный для головного мозга. Он участвует в нейрогенезе — процессе образования нейронов. Кроме того, белок BDNF защищает существующие нейроны, обеспечивая их выживание и поддерживая синоптические связи между ними. Качество этих нейронных связей определяет качество мышления, обучения и более высокий уровень функционирования головного мозга. Низкий уровень белка BDNF зафиксирован при целом комплексе неврологических заболеваний, в том числе болезни Альцгеймера, эпилепсии, нервно-психической анорексии, депрессии, шизофрении и обсессивно-компульсивном расстройстве. Сегодня известно, что уровень BDNF можно повысить благодаря аэробной физической нагрузке и потреблению незаменимой полиненасыщенной жирной кислоты класса омега-3 докозагексаеновой кислоты (DHA). Кроме того, появились новые данные о том, что этот критически важный для мозга белок в значительной степени зависит от баланса бактерий, формирующих микрофлору кишечника.
В ноябре 2013 года в журнале Американской медицинской ассоциации JAMA Neurology были опубликованы результаты интереснейшего исследования команды ученых Медицинской школы Бостонского университета, показывающие, как уровень BDNF в крови соотносится с риском развития деменции{70}. Эта научная работа опиралась на данные широко известного Фремингемского исследования[12] — одного из наиболее масштабных эпидемиологических исследований из когда-либо проводившихся, — чтобы получить показатели уровня белка BDNF в группе у 2131 взрослого. У участников группы не проявлялось симптомов деменции в начале исследования. Наблюдение за ними осуществлялось на протяжении десяти лет.
Ученые из Бостонского университета обнаружили, что у участников группы с наиболее высоким уровнем белка BDNF риск развития деменции был в два раза ниже по сравнению с участниками группы с низким уровнем BDNF. Они пришли к выводу, что уровень BDNF «также может быть пониженным у здоровых людей, имеющих предрасположенность к развитию деменции или болезни Альцгеймера». Заключение ученых было очевидным: «Результаты нашего исследования указывают на роль BDNF в возможности предотвращения деменции или болезни Альцгеймера»{71}.
GABA — еще один важный химический элемент, который продуцируют кишечные бактерии. Эта аминокислота, в центральной нервной системе выступающая в качестве нейромедиатора, служит основным химическим «мессенджером» головного мозга, тормозящего нервную активность за счет угнетения передачи и нормализации волн головного мозга. Иными словами, GABA стабилизирует состояние нервной системы, так что организм способен эффективнее справляться со стрессом. В 2012 году исследователи из Бэйлорского медицинского колледжа и Техасской детской больницы обнаружили группу бифидобактерий, производящих большое количество GABA. Они предположили, что эти бактерии могут играть важную роль в профилактике и лечении не только болезней мозга, но и воспалительных заболеваний кишечника (ВЗК), таких как болезнь Крона{72}. Поскольку GABA ингибирует нейронную активность, она помогает контролировать уровень тревожности, а тревожность, в свою очередь, — обычный триггер нарушений работы желудочно-кишечного тракта, в основе которых лежит воспалительный процесс.
Следующий важный нейромедиатор, производимый кишечными бактериями, — глутамат. Он участвует практически во всех функциях головного мозга, включая процессы познания, обучения и запоминания. В здоровом головном мозге это вещество содержится в большом количестве. Массу неврологических расстройств, от тревожности и расстройства поведения до депрессии и болезни Альцгеймера, связывают с недостатком GABA и глутамата в головном мозге.
Один из наиболее важных выводов последнего исследования на тему взаимосвязи между микробами и здоровьем головного мозга заключается в том, что нарушение баланса микрофлоры кишечника — это не просто состояние, в котором «плохие» бактерии имеют численный перевес над «хорошими» и всячески их угнетают, провоцируя воспалительный процесс и лишая организм жизненно важных элементов, ими производимых. У миллионов людей сегодня дисбаланс микрофлоры кишечника обусловлен повышенной кишечной проницаемостью, которая вызывает состояние хронического слабовыраженного воспалительного процесса. Остановимся на этом подробнее.






