Глава 22. Антибактериальные химиотерапевтические средства
К антибактериальным химиотерапевтическим средствам относят следующие группы лекарственных средств:
1. Антибиотики.
2. Синтетические антибактериальные средства.
3. Противосифилитические средства.
4. Противотуберкулезные средства.
После выделения и определения возбудителя заболевания подбирают наиболее эффективные противомикробные средства – препараты выбора (препараты 1-го ряда).
Антибиотики – это химиотерапевтические вещества биологического происхождения, тормозящие рост или вызывающие гибель микроорганизмов.
Таблица 3. Антибактериальные средства выбора при различных возбудителях заболеваний

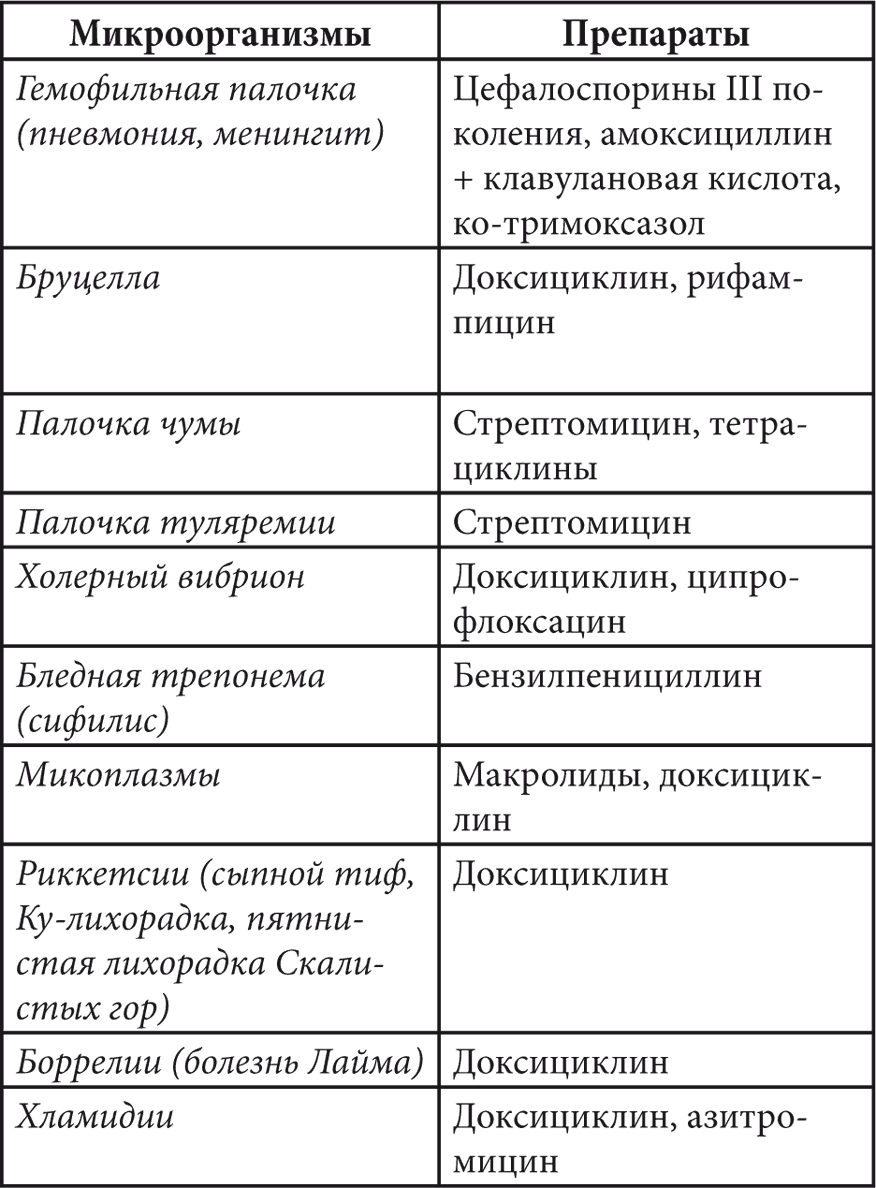
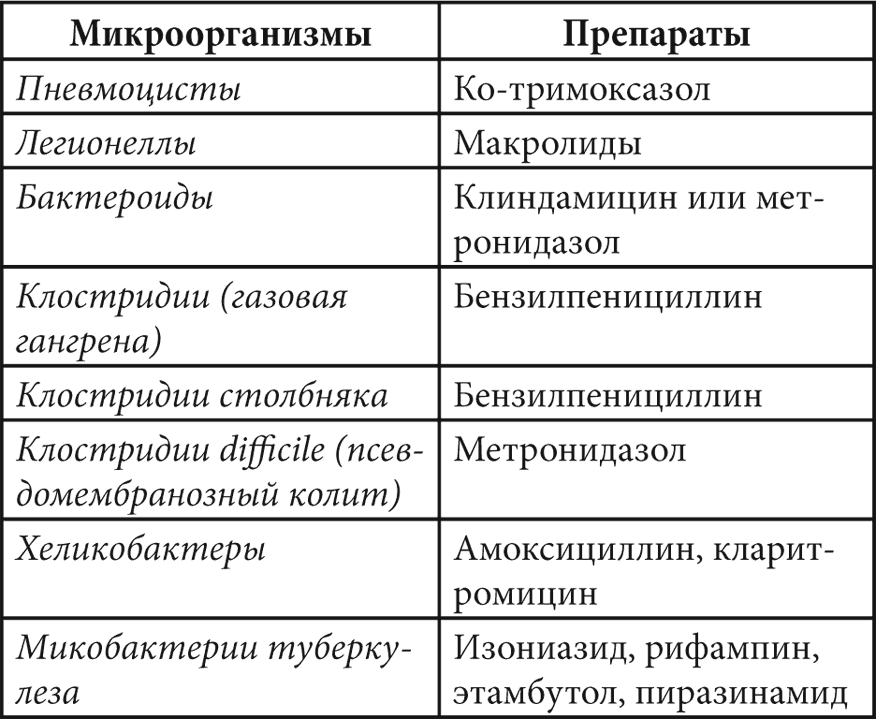
Выделяют различные классификации антибиотиков:
1. В зависимости от источников получения:
– природные (биосинтетические) – вырабатываемые микроорганизмами и низшими грибами;
– полусинтетические (химические аналоги природных антибиотиков) – получаемые искусственным путем.
2. В зависимости от химического строения:
– ?-лактамные антибиотики (пенициллины, цефалоспорины, карбапенемы, монобактамы);
– макролиды и азалиды;
– аминогликозиды;
– тетрациклины;
– полимиксины;
– полиеновые антибиотики;
– препараты хлорамфеникола (левомицетин);
– гликопептидные антибиотики;
– антибиотики разных химических групп.
3. В зависимости от характера действия на бактериальную клетку:
– бактерицидные (вызывающие гибель бактерий);
– бактериостатические (останавливающие рост и деление бактерий).
При применении антибиотиков следует учитывать их характер действия. Совместное назначение бактериостатического средства с бактерицидным может привести к снижению эффективности препаратов. Например, бактериостатический препарат тетрациклин угнетает рост и деление клетки и ослабляет действие бензилпенициллина, действующего только на делящиеся бактерии. Напротив, два бактерицидных препарата могут усиливать действие друг друга. Например, комбинация бензилпенициллина и аминогликозида может приводить к усилению эффектов препаратов, потому что бензилпенициллин нарушает образование клеточной стенки бактерий и облегчает попадание аминогликозида в клетку.
Противомикробное действие антибиотиков заключается в нарушении:
• образования клеточной стенки;
• проницаемости цитоплазматической мембраны;
• образования белка;
• образования РНК.
Бактерицидными называют те антибиотики, которые нарушают образование клеточной стенки бактерий. Бактериостатическими – нарушающие образование белка на рибосомах.
Антибиотики можно разделить по спектру действия на:
1. препараты широкого спектра (действующие как на грамположительные, так и на грамотрицательные бактерии):
• тетрациклины;
• хлорамфеникол;
• аминогликозиды;
• цефалоспорины;
• полусинтетические пенициллины;
2. препараты с преимущественным действием на грамположительные бактерии:
• биосинтетические пенициллины;
• макролиды;
3. препараты с преимущественным действием на грамотрицательные бактерии:
• полимиксины;
• монобактамы.
По применению выделяют:
• основные антибиотики (препараты выбора), с которых начинают лечение;
• резервные антибиотики, которые применяют при неэффективности или непереносимости основных.
Таблица 4. Механизм и характер антимикробного действия антибиотиков
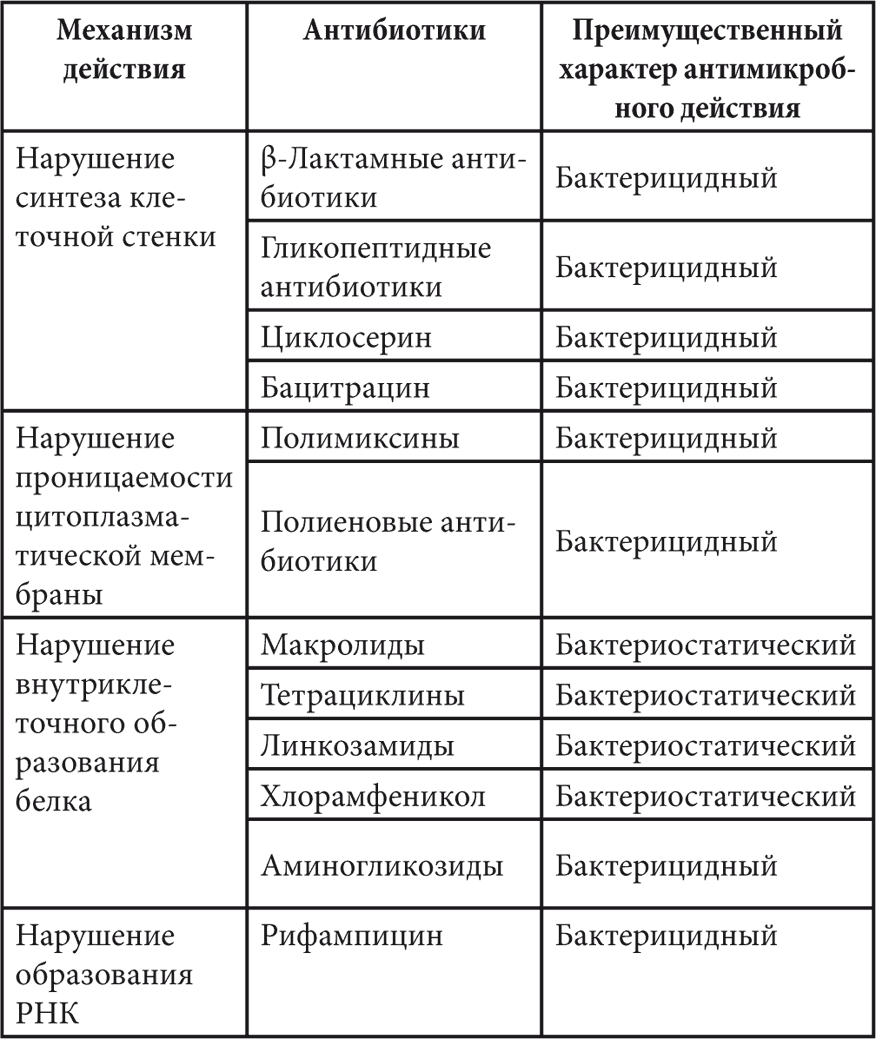
К антибиотикам может развиться устойчивость микроорганизмов – способность микроорганизмов размножаться в присутствии безопасной для них дозы антибиотика.
Устойчивость может быть природной и приобретенной.
Природная устойчивость связана с отсутствием или недоступностью у микроорганизмов «мишени» для действия антибиотика, а также возможно угнетение антибиотика ферментами бактерий. При наличии у бактерий природной устойчивости некоторые антибиотики против них неэффективны. Например, грамотрицательные микроорганизмы устойчивы к действию ванкомицина.
Под приобретенной устойчивостью понимают свойство некоторых бактерий сохранять жизнеспособность при тех количествах антибиотиков, которые подавляют остальную микробную популяцию. Приобретенная устойчивость связана с изменениями в генотипе бактериальной клетки.
Устойчивость может развиваться не только к применяемому препарату, но и к другим препаратам из той же химической группы. Такая устойчивость называется перерестной.
Рациональное применение химиотерапевтических средств не дает возникнуть устойчивости.
Несмотря на то, что действие антибиотиков направлено преимущественно против бактерий, они, тем не менее, вызывают некоторые побочные эффекты у человека.
Антибиотики, нарушающие образование клеточной стенки
Клеточная стенка есть только у клеток бактерий, грибов и растений. Основу клеточной стенки бактерий составляет пептидогликан (также называемый мукопептид, муреин). Пептидогликан представляет собой гигантскую молекулу, покрывающую всю клетку и располагается над цитоплазматической (внутренней) мембраной микробной клетки. У грамотрицательных бактерий пептидогликан сверху «покрыт» наружной мембраной, препятствующей проникновению антибиотиков в клетку.
Пептидогликан образует прочный каркас.
К антибиотикам, нарушающим синтез клеточной стенки бактерий, относят:
– ?-лактамные антибиотики;
– гликопептидные антибиотики;
– циклосерин;
– бацитрацин;
– производные фосфоновой кислоты.
?-лактамные антибиотики
?-Лактамные антибиотики (пенициллины, цефалоспорины, карбапенемы и монобактамы) – это препараты, имеющие в составе молекулы ?-лактамное кольцо, которое необходимо для противомикробного действия. При разрушении ?-лактамного кольца бактериями данные антибиотики перестают действовать.
?-лактамы действуют бактерицидно на активно делящиеся бактерии, так как делящиеся бактерии образуют пептидогликан, который и являются мишенью для действия ?-лактамных антибиотиков.
Пенициллины
Классификация
1. Природные.
2. Полусинтетические.
Природные пенициллины
Природные пенициллины образуются различными видами плесневых грибов рода Penicillium.
Классификация
1. Препараты для парентерального введения (кислотонеустойчивые).
1.1. короткого действия: бензилпенициллина натриевая и калиевая соли;
1.2. длительного действия: бензилпенициллин прокаин; бензатин бензилпенициллин; бензатин бензилпенициллин + бензилпенициллин прокаин.
2. Препараты для энтерального введения (кислотоустойчивые): феноксиметилпенициллин.
Механизм действия
Пенициллины нарушают синтез клеточной стенки бактерий, что вызывает последующую их гибель (бактерицидный эффект).
Эти антибиотики действуют в основном на грамположительные микроорганизмы:
• грамположительные кокки (стрептококки, пневмококки; стафилококки, не образующие ?-лактамазу (фермент, разрушающий ?-лактамное кольцо));
• грамположительные палочки (возбудители дифтерии, сибирской язвы; листерии);
• грамотрицательные кокки (менингококки и гонококки);
• анаэробы (клостридии);
• актиномицеты;
• спирохеты (бледная трепонема, лептоспиры, боррелии).
Показания
Тонзиллофарингит (ангина); скарлатина; рожа; остеомиелит; бактериальный эндокардит; очаговая и крупозная пневмония; абсцесс легких; дифтерия; менингит; газовая гангрена; столбняк; актиномикоз; клещевой боррелиозе (болезни Лайма).
Препараты этой группы – средства выбора при лечении сифилиса и профилактики обострений ревматических заболеваний. Устойчивость чаще всего встречается среди стафилококков, вырабатывающих ?-лактамазы, разрушающие ?-лактамные кольца молекулы бензилпенициллинов. В связи с развитием устойчивости гонококков к бензилпенициллину препарат не следует применять при гонорее.
Бензилпенициллин выпускают в виде натриевой и калиевой солей.
Бензилпенициллина натриевая и калиевая соли – хорошо растворимые препараты бензилпенициллина. В значительной степени разрушаются соляной кислотой желудка, поэтому вводятся внутримышечно.
Бензилпенициллина калиевая сольсодержит большое количество калия, поэтому большие дозы препарата не следует применять больным с почечной недостаточностью, так как содержащийся в препарате калий может вызывать судороги.
К пролонгированным (длительно действующим) пенициллинам относят бензилпенициллин прокаина, или бензилпенициллина новокаиновую соль, которая действует 12–18 часов, бензатина бензилпенициллин, действующий 7-10 дней, и бензатин бензилпенициллин + бензилпенициллин прокаин с продолжительностью действия 1 месяц.
Феноксиметилпенициллин не разрушается соляной кислотой и применяется внутрь.
Природные пенициллины имеют некоторые недостатки:
• разрушение ?-лактамазой;
• разрушение в желудке (за исключением феноксиметилпенициллина);
• относительно узкий спектр действия (эффективны против малого количества микроорганизмов).
Нежелательные реакции
Биосинтетические пенициллины в целом хорошо переносятся, но могут вызвать аллергию. Высокие дозы бензилпенициллина могут вызывать судороги, аллергические реакции.
Лекарственные взаимодействия
Встречаются в практике редко, например, действие варфарина может быть усилено бензилпенициллином.
Полусинтетические пенициллины
В процессе поиска более совершенных антибиотиков группы пенициллина были получены полусинтетические препараты с заданными свойствами: устойчивость к бета-лактамазам, устойчивость к соляной кислоте желудка, обладающие широким спектром действия.
Классификация:
1. Препараты узкого (преимущественно грамположительного) спектра действия, устойчивые к действию ?-лактамазы: изоксазолиловые пенициллины (антистафилококковые пенициллины): оксациллин, нафциллин, клоксациллин, диклоксациллин, флуклоксациллин.
2. Препараты широкого спектра действия, не устойчивые к действию ?-лактамазы:
– аминопенициллины: ампициллин, амоксициллин;
– карбоксипенициллины: карбенициллин, карфециллин, тикарциллин;
– уреидопенициллины: азлоциллин, пиперациллин, мезлоциллин.
Полусинтетические пенициллины, устойчивые к действию ?-лактамазы (изоксазолиловые пенициллины, пенициллиназостабильные, антистафилококковые пенициллины).
Препараты отличаются от природных пенициллинов тем, что они высокоэффективны при инфекциях, вызываемых ?-лактамазообразующими стафилококками, отсюда и название – «антистафилококковые пенициллины», но их эффективность значительно ниже природных. В связи с этим ЛС этой группы показаны только в тех случаях, когда известно, что инфекция вызвана стафилококками, продуцирующими ?-лактамазу.
Первым препаратом данной группы был метициллин. Препарат уступает по эффективности антибиотикам этой группы, поэтому в настоящее время метициллин используют только в лаборатории.
Оксациллин устойчив в кислой среде желудка.
Нафциллин более эффективен, чем оксациллин, в отношении стафилококков, устойчивых к бензилпенициллину.
В настоящий момент некоторые штаммы Staphylococcus aureus выработали устойчивость к оксациллину/метициллину. Такие штаммы стафилококков получили название метициллин-резистентных (MRSA). Препараты выбора при заболеваниях, вызванных MRSA – ванкомицин или линезолид.
Аминопенициллины (ампициллин и амоксициллин) – отличаются от препаратов бензилпенициллина более широким спектром действия, а также устойчивостью к кислоте желудка. Спектр действия аминопенициллинов включает как грамположительные, так и грамотрицательные микроорганизмы.
В отличие от биосинтетических и антистафилококковых пенициллинов аминопенициллины:
• действуют на ряд грамотрицательных бактерий – кишечную палочку, протей (Р. mirabilis), сальмонеллы, шигеллы (последние часто устойчивы), гемофильную палочку;
• для этих бактерий характерен низкий уровень образования ?-лактамаз;
• более активны против энтерококков и листерий;
• менее активны против стрептококков, спирохет, анаэробов, стафилококков, чувствительных к бензилпенициллину.
Аминопенициллины подвержены разрушению всеми ?-лактамазами грамположительных и грамотрицательных бактерий. Не активны против грамотрицательных возбудителей больничных инфекций, таких как синегнойная палочка (P. aeruginosa), клебсиеллы, серрации и многие другие. Аминопенициллины применяют при острых бактериальных инфекциях верхних дыхательных путей и ЛОР-органов, коклюше, сепсисе, бактериальном менингите, кишечных инфекциях, инфекциях желче– и мочевыводящих путей, инфекциях почек, а также против Helicobacter pylori при язвенной болезни желудка. Внутривенно вводимый ампициллин используют чаще всего для лечения инвазивных энтерококковых инфекций и Listeria meningitis; перорально вводимый амоксициллин используют для лечения неосложненных инфекций ушей, носа и горла, в целях предотвращения эндокардита у пациентов с высоким уровнем риска, проходящих стоматологическое лечение и в качестве одного из компонентов комбинированной терапии инфекций, вызванных Helicobacter pylori.
Ампициллин устойчив в кислой среде желудка, более эффективен при кишечных заболеваниях. Прием пищи снижает всасывание препарата в кишечнике. Препарат вводят внутрь и парентерально (внутривенно, внутримышечно). Продолжительность действия – 6 часов.
В качестве антибиотика второго ряда ампициллин используют при брюшном тифе, бациллярной дизентерии, препарат выбора – при листериозе (менингит, эндокардит, сепсис новорожденных).
Амоксициллин по сравнению с ампициллином всасывается в ЖКТ в 2–2,5 раза лучше, чем ампициллин, не зависит от приема пищи. Препарат не применяют при кишечных инфекциях (шигеллез, сальмонеллез). Амоксициллин применяют только внутрь. Более эффективен, чем ампициллин в отношении хеликобактеров, но уступает ампициллину в отношении шигелл. Из всех пероральных (принимаемых внутрь) бета-лактамов амоксициллин обладает наибольшей активностью в отношении Streptococcus pneumoniae, устойчивого к природным пенициллинам.
Ингибиторы ?-лактамаз: клавулановая кислота, сульбактам, тазобактам
Комбинация амоксициллин + клавулановая кислота или ампициллин + сульбактам:
• расширение спектра действия обоих препаратов;
• приобретение устойчивости к гидролизу ?-лактамазами.
Карбоксипенициллины
Карбоксипенициллины так же, как и аминопенициллины, антибиотики широкого спектра действия, но уступают им по эффективности. Карбоксипенициллины эффективны в отношении многих бактерий семейства Enterobacteriaceae (за исключением Klebsiella spp., Proteus vulgaris, C. diversus, Enterococcus faecalis). Эта группа включает карбенициллин, карфециллин и тикарциллин. Препараты применяют также при инфекциях, вызванных синегнойной палочкой.
Карбенициллин – производное 6-аминопенициллановой кислоты, разрушается ?-лактамазами, плохо всасывается в ЖКТ, поэтому его вводят внутримышечно и внутривенно. Применяют 4–6 раз в день.
Карбенициллин вызывает побочные эффекты, характерные для других пенициллинов – реакции гиперчувствительности (анафилактический шок, крапивница, ангионевротический отек и сыпи), в дополнение к ним:
• гипернатриемию (препарат выпускают в виде динатриевой соли), которая может привести к развитию хронической сердечной недостаточности;
• гипокалиемию;
• кровоточивость как результат снижения агрегации тромбоцитов.
Карфециллин – фениловый эфир карбенициллина. В отличие от карбенициллина кислотоустойчив, хорошо всасывается при приеме внутрь, поэтому его принимают внутрь 3 раза в сутки.
Тикарциллин активнее карбенициллина, особенно по воздействию на синегнойную палочку, плохо всасывается в ЖКТ, поэтому его вводят внутримышечно и внутривенно 4–6 раз в день.
Уреидопенициллины
К препаратам этой группы относят азлоциллин, пиперациллин и мезлоциллин. Антимикробная активность карбоксипенициллинов и уреидопенициллинов примерно одинакова (в отношении клебсиел и грамположительных бактерий более активны уреидопенициллины). Разрушаются ?-лактамазами стафилококков и грамотрицательных бактерий. Уреидопенициллины в 4–8 раз превосходят карбоксипенициллины по активности в отношении синегнойной палочки; вводят их парентерально.
Главное достоинство карбокси– и уреидопенициллинов – активность в отношении синегнойной палочки, в связи с чем эти пенициллины получили название «антисинегнойные». Основные показания для препаратов этой группы – инфекции, вызванные синегнойной палочкой, протеем, кишечной палочкой (сепсис, раневые инфекции, пневмонии, инфекции мочевыделительной системы, брюшной полости и малого таза и др.).
По эффективности действия на синегнойную палочку «антисинегнойные» пенициллины располагаются следующим образом: азлоциллин = пиперациллин > мезлоциллин = тикарциллин > карбенициллин.
Комбинированные препараты, содержащие пенициллины и ингибиторы ?-лактамаз
Все полусинтетические пенициллины широкого спектра действия разрушаются бактериальными ?-лактамазами (пенициллиназами), поэтому их целесообразно комбинировать с ингибиторами ?-лактамаз. Ингибиторы ?-лактамаз, такие как клавулановая кислота, сульбактам и тазобактам, в своей структуре содержат ?-лактамное кольцо, но обладают слабыми антибактериальными свойствами. Более того, они связываются с ?-лактамазами и необратимо инактивируют их, тем самым предотвращая гидролиз антибиотиков. Комбинированные препараты получили название ингибиторозащищенных пенициллинов (амоксициллин + клавулановая кислота, ампициллин + сульбактам, иперациллин + тазобактам, тикарциллин + клавулановая кислота). В отличие от монопрепаратов, антимикробный спектр ингибиторозащищенных пенициллинов расширяется в отношении стафилококков, клебсиелл, гемофильной палочки, моракселл, шигелл, сальмонелл, а также анаэробов группы Bacteroides fragilis.
Наиболее широкий спектр антимикробной активности характерен для пиперациллина + тазобактама.
Нежелательные реакции
Крапивница, сыпь, бронхоспазм, отек Квинке, анафилактический шок, боль в животе, тошнота, рвота, диарея, псевдомембранозный колит (потенциально угрожающее жизни осложнение), болезненность и инфильтрат при внутримышечном введении, флебит при внутривенном введении, кандидози др.
Цефалоспорины
Цефалоспорины – группа природных и полусинтетических антибиотиков, имеющих в своей основе 7-аминоцефалоспорановую кислоту. Сходство химической структуры цефалоспоринов с пенициллинами определяет одинаковый механизм и тип антибактериального действия, высокую эффективность, низкую токсичность для макроорганизма, а также перекрестные аллергические реакции с пенициллинами. Отличительные особенности цефалоспоринов – их устойчивость к ?-лактамазам и широкий спектр антимикробного действия.
Механизм действия цефалоспоринов – угнетение транспептидазы, в результате нарушается образование пептидогликана, уменьшается прочность клеточной стенки бактерий, что приводит к гибели бактерий и обусловливает бактерицидный характер действия.
Цефалоспорины классифицируют по поколениям, внутри которых выделяют препараты для парентерального и энтерального введения (табл. 5).
Таблица 5. Классификация цефалоспоринов
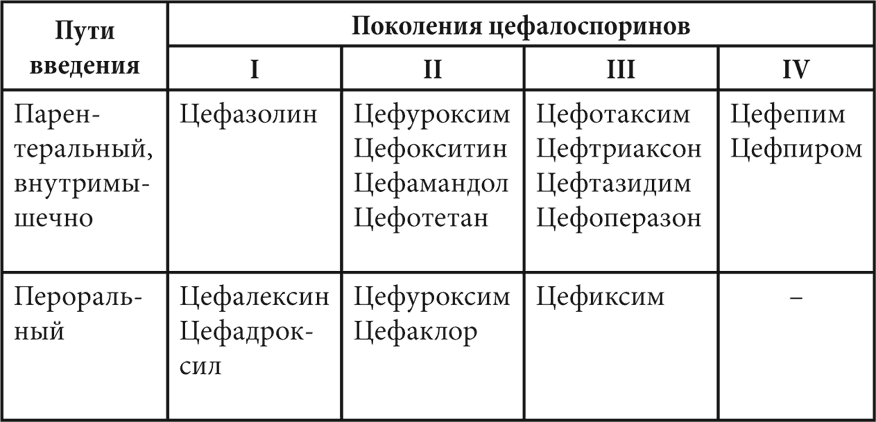
В ряду от I к IV поколению цефалоспоринов спектр действия расширяется, повышается эффективность в отношении грамотрицательных бактерий и наблюдается небольшое понижение активности в отношении грамположительных микроорганизмов. Особенность цефалоспоринов – отсутствие действия на энтерококки.
Цефалоспорины I поколения
Цефалоспорины I поколения обладают широким спектром действия с преимущественным влиянием на грамположительную флору, а также грамотрицательные палочки Proteus mirabilis и E. coli, вызывающие инфекции мочевыводящих путей, а также на Klebsiella pneumoniae, вызывающую пневмонии и инфекции мочевыводящих путей.
Эти препараты чувствительны ко многим ?-лактамазам грамотрицательных микроорганизмов.
Показания
Цефалексин и цефазолин используют для лечения инфекций кожи и мягких тканей, при тонзиллофарингите, при бактериальных инфекциях верхних и нижних дыхательных путей; цефазолин также применяют для профилактики послеоперационных осложнений.
К препаратам I поколения устойчивы синегнойная палочка, листерии, энтерококки и бактероиды.
Цефалоспорины II поколения
Цефалоспорины II поколения отличаются от препаратов I поколения более высокой активностью в отношении грамотрицательных микроорганизмов (кишечной палочки, протея, сальмонелл, шигелл), несколько меньшей эффективностью в отношении грамположительных бактерий. Спектр расширяется за счет трех грамотрицательных микроорганизмов – Haemophilus influenza, некоторых штаммов Enterobacter aerogenes и Neisseria. По спектру антимикробной активности цефалоспорины II поколения могут быть разделены на две группы:
цефуроксим, представляющий первую группу, имеет повышенную активность в отношении H. influenzae по сравнению с первым поколением цефалоспоринов;
цефотетан и цефокситин, составляющие вторую группу, демонстрируют повышенную активность в отношении бактероидов.
II поколение цефалоспоринов обычно более устойчиво к большему количеству ?-лактамаз, чем первое поколение цефалоспоринов; как и цефалоспорины I поколения, не действуют на синегнойную палочку.
Показания
Цефалоспорины II поколения применяют при бактериальных инфекциях верхних и нижних дыхательных путей, инфекциях мочевыводящих путей, инфекциях кожи, мягких тканей, костей и суставов, а также для периоперационной антибиотикопрофилактики в хирургии. Цефуроксим часто используют для лечения внебольничной пневмонии, а цефотетан применяют для лечения интраабдоминальных и воспалительных заболеваний органов малого таза.
Нежелательные реакции
Включают диарею, небольшое повышение уровня печеночных ферментов и реакции гиперчувствительности; редко вызывают агранулоцитоз и интерстициальный нефрит.
Цефалоспорины III поколения
Цефалоспорины III поколения отличаются расширенным спектром в отношении большинства грамотрицательных бактерий, в том числе резистентных к другим антибиотикам. Они активны в отношении бактерий кишечной группы (E. coli, индол-положительные Proteus, Klebsiella, Enterobacter, Serratiau Citrobacter), а также Neisseria и H. influenzae. Цефалоспорины III поколения менее активны в отношении грамположительных организмов в сравнении с I–II поколением препаратов. Некоторые из цефалоспоринов III поколения (цефтазидим, цефоперазон) действуют на синегнойную палочку. По эффективности воздействия на синегнойную палочку препараты располагаются в следующем порядке: цефтазидим > цефоперазон > цефтриаксон > цефотаксим. III поколение цефалоспоринов устойчивы ко многим ?-лактамазам грамотрицательных микроорганизмов.
Показания
Инфекции нижних дыхательных путей, мочевыводящих путей, кожи, мягких тканей, кишечные инфекции, внебольничный менингит, вызванный S. pneumoniae, неосложненную гонококковую инфекцию, эндокардит с отрицательным результатом посева крови и осложненную болезнь Лайма.
Цефалоспорины IV поколения
Цефалоспорины IV поколения обладают еще более широким спектром антимикробного действия, чем препараты III поколения. Они более эффективны в отношении грамположительных кокков. Для них характерны более высокая устойчивость к действию ?-лактамаз микроорганизмов, высокая эффективность в отношении синегнойной палочки.
Показания
Цефалоспорины IV поколения применяют при тяжелых нозокомиальных инфекциях, вызванных полирезистентной микрофлорой, инфекциях нижних дыхательных путей (пневмония, абсцесс легкого, эмпиема плевры), а также для лечения инфекций у пациентов с нейтропенией и иммунодефицитом.
Нежелательные реакции
Аллергические реакции (крапивница, лихорадка, сывороточная болезнь, анафилактический шок). Больным, имеющим в анамнезе аллергические реакции на пенициллины, нельзя назначать цефалоспорины; нарушение функции почек (характерно для цефалоспоринов I поколения); суперинфекция, псевдомембранозный колит; лейкопения; нарушение функции печени; диарея (чаще при применении цефоперазона); судороги; флебиты при внутривенном введении; стоматит, глоссит (кандидоз полости рта).
Комбинированные препараты, содержащие цефалоспорины и ингибиторы ?-лактамаз (цефоперазон+сульбактам)
Сульбактам защищает цефоперазон от гидролиза ?-лактамазами. Спектр действия расширен за счет анаэробных микроорганизмов и штаммов энтеробактерий, продуцирующих ?-лактамазы.
Показания
Применяют при тяжелых нозокомиальных инфекциях, вызванных полирезистентной и смшанной (аэробно-анаэробной) микрофлорой, инфекциях малого таза, ЖКТ, нижних дыхательных путей (пневмония, абсцесс легкого, эмпиема плевры), осложненных инфекциях мочевыводящих путей, сепсисе, а также для лечения инфекций у пациентов с нейтропениеи и иммунодефицитом.
Карбапенемы (имипенем, меропенем, эртапенем)
Карбапенемы – синтетические ?-лактамные антибиотики. В отличие от пенициллинов содержат в тиазолидиновом кольце не атом серы, а метильную группу.
Они характеризуются более высокой устойчивостью к действию ?-лактамаз и обладают сверхшироким спектром антибактериального действия, включая грамположительные и грамотрицательные аэробы и анаэробы, а также штаммы, устойчивые к цефалоспоринам III и IV поколений.
Механизм действия
Нарушают синтез клеточной стенки бактериий (структурное сходство с D-аланин-D-аланином обеспечивает связывание со специфическими пенициллинсвязывающими белками, что приводит к угнетению транспептидазы, нарушению образования поперечных сшивок между цепочками пептидогликана, повышению активности аутолитических ферментов клеточной стенки, что вызывает ее повреждение), поэтому приводят к бактерицидному эффекту.
Показания
Карбапенемы применяют при тяжелых инфекциях (включая нозокомиальные), вызванных полирезистентными штаммами микроорганизмов, чаще как антибиотики резерва. При угрожающих жизни инфекциях могут быть рассмотрены как средства первого ряда при эмпирической терапии. Не активны в отношении метициллин-резистентных стафилококков (MRSA), ванкомицин-резистентных энтерококков (VRE) или легионелл.
Имипенем – производное тиенамицина, продуцируемого Streptomyces cattleya. Препарат инактивируется в почечных канальцах ферментом дегидропептидазой I, при этом не создается терапевтическая концентрация в моче. Имипенем в качестве самостоятельного препарата не применяют. Для медицинского применения выпускают комбинированный препарат, содержащий имипенем и специфический ингибитор дегидропептидазы I почечных канальцев – циластатин. Такое сочетание тормозит метаболизм имипенема в почках и значительно повышает концентрацию неизмененного антибиотика в моче.
Нежелательные реакции
При применении препарата возможны аллергические реакции, тошнота, рвота, судороги, эозинофилия, лейкопения, нейтропения, флебиты в месте внутривенного введения.
Меропенем в отличие от имипенема не разрушается дегидропептидазой почечных канальцев, поэтому применяется самостоятельно. Другие отличия от имипенема: более активен в отношении грамотрицательных бактерий; менее активен в отношении стафилококков и стрептококков; не обладает судорожной активностью; не применяется при инфекциях костей и суставов; может применяться внутривенно в виде инфузий и болюсного введения; нет лекарственной формы для внутримышечного введения.
Эртапенем гораздо менее активен в отношении P. aeruginosa и Acinetobacter spp., чем два других препарата. Преимущество эртапенема – более продолжительное действие, назначается внутривенно или внутримышечно 1 раз в сутки.
Монобактамы
Антибиотики этой группы имеют в своей структуре моноциклическое ?-лактамное кольцо. Единственно применяющийся в медицинской практике монобактам – азтреонам. Выделен из культуры Chromobacterium violaceum. Препарат высоко активен по отношению к грамотрицательным бактериям (кишечной и синегнойной палочке, протею, клебсиеллам, гемофильной палочке, гонококкам, менингококкам, шигеллам, сальмонеллам и др.) и не действует на грамположительные бактерии, анаэробы, включая бактероиды. Ограниченность антимикробного спектра действия азтреонама обусловлена тем, что он устойчив ко многим ?-лактамазам, продуцируемым грамотрицательной флорой, и в то же время разрушается ?-лактамазами грамположительных микроорганизмов и бактероидов.
Показания
Азтреонам – препарат резерва, особенно эффективен у пациентов с выраженной аллергией на пенициллин при инфекциях нижних дыхательных путей (внебольничная и нозокомиальная пневмония), интраабдоминальных инфекциях, тяжелых инфекциях мочевыводящих путей, брюшной полости и малого таза, инфекциях кожи, мягких тканей, костей и суставов; при менингите, сепсисе, при неэффективности других антибактериальных средств.
Нежелательные реакции
Диспепсические нарушения, кожные аллергические реакции, головная боль, флебиты в месте внутривенного введения.
Ингибиторы синтеза муреинового мономера (фосфомицин, фосмидомицин)
Механизм действия
Антибиотики, угнетающие образование мономеров муреина, составляющих пептидогликан клеточной стенки.
Фосфомицин
Антибактериальное средство широкого спектра действия, оказывающее бактерицидное действие. Эффективен в отношении большинства грамположительных (энтерококки, стафилококки, стрептококки) и грамотрицательных возбудителей (кишечная палочка, штаммы Citrobacter, Enterobacter, Serratia, клебсиелла, Morganella morganii, Proteus mirabilis, Proteus vulgaris). Фосфомицин особенно эффективен в отношении грамотрицательных бактерий, вызывающих заболевания мочевыводящих путей, поскольку он выделяется с мочой в неизмененном виде. Однократный пероральный прием 3 г препарата оказался одинаково эффективным, как и многократный прием других ЛС в лечении инфекций мочевыводящих путей.
Показания
Препарат применяют внутрь и парентерально при неосложненных инфекциях мочевыводящих путей, вызываемых чувствительными микроорганизмами (цистит, уретрит, профилактика и лечение инфекции при хирургических вмешательствах и трансуретральных диагностических исследованиях). Фосфомицин можно назначать беременным.
Нежелательные реакции
Головная боль, диарея или тошнота.
Фосмидомицин
Действует аналогично фосфомицину.
Циклосерин
Средство второго ряда при лечении инфекции туберкулеза с множественной лекарственной устойчивостью, а также при инфекциях мочевыводящих путей.
Механизм действия
Нарушение синтеза клеточной стенки.
Нежелательыне реакции
Судороги, неврологические синдромы, в том числе периферическую невропатию и психоз. Алкоголь, изониазид и этионамид потенцируют токсичность циклосерина; пиридоксин может уменьшить симптомы периферической нейропатии, вызванной циклосерином.
Бацитрацин
Вещество впервые выделено из штаммов Bacillus subtilis. Бацитрацин – пептидный антибиотик, нарушающий синтез пептидогликана клеточной стенки. Препарат обладает преимущественным действием на грамположительную флору. Из-за своего значительного токсического действия на почки, костный мозг и нервно-мышечную передачу препарат используют только местно.
Показания
Комбинированный препарат бацитрацина + неомицина применяют при поверхностных кожных (профилактика инфекционно-воспалительных заболеваний при незначительных порезах, царапинах и ожогах, лечение эпидермальной пиодермии) или офтальмологических инфекциях; при наружном отите. Бацитрацин не всасывается при пероральном введении, накапливается в просвете кишечника и поэтому принимается внутрь для лечения колита, вызванного Clostridium difficile, или для эрадикации ванкомицин-резистентных энтерококков (ВРЭ) в ЖКТ.
Нежелательные реакции
Аллергические реакции, реакции на месте нанесения.
Гликопептидные антибиотики
Ванкомицин и тейкопланин обладают бактерицидной активностью в отношении грамположительных палочек и кокков.
Механизм действия ванкомицина обусловлен нарушением синтеза клеточной стенки. Ванкомицин назначают при тяжелых стафилококковых и стрептококковых инфекциях в случаях неэффективности и непереносимости пенициллинов, цефалоспоринов и других антибиотиков.
Показания
Внутривенно вводимый ванкомицин – наиболее широко применяемый препарат для лечения сепсиса и эндокардита, вызванных метициллин-резистентным Staphylococcus aureus (MRSA). Перорально вводимый ванкомицин плохо всасывается, поэтому используется для лечения инфекций ЖКТ, обусловленных C. difficile (возбудитель псевдомембранозного колита). Продолжительность действия препарата составляет 6 часов. Ванкомицин повышает эффективность аминогликозидов, комбинация этих антибиотиков показана при энтерококковом эндокардите.
Нежелательные реакции
Обратимое нарушение функции почек, ототоксическое действие, обратимые лейкопения, нейтропения, эозинофилия, тромбоцитопения; редко – агранулоцитоз, аллергические реакции (сыпь, крапивница, синдром Стивенса-Джонсона, васкулит), местные реакции (тромбофлебит, боль и жжение в месте введения, некроз тканей в месте введения); вследствие высвобождения гистамина – снижение АД, головокружение, тахикардия, бронхоспазм, лихорадка, кожная сыпь, синдром «красного человека» (гиперемия кожи лица и шеи).
Тейкопланин отличается от ванкомицина тем, что: значительно реже вызывает нарушение функции почек; более активен в отношении метициллин-резистентных Staphylococcus aureus (MRSA) и энтерококков; более длительное действие (назначают 1–2 раза в сутки); реже вызывает нежелательные реакции.
Антибиотики, нарушающие синтез белков
Классификация
К антибиотикам, нарушающим синтез белка рибосомами, относят:
• макролиды;
• аминогликозиды;
• тетрациклины;
• хлорамфеникол;
• линкозамиды.
Макролиды и близкие к ним антибиотики
Макролиды – класс антибиотиков, основу химической структуры которых составляет макроциклическое лактонное кольцо, связанное с различными сахарами.
Макролиды классифицируют в зависимости от способов получения и количества атомов углерода в макроциклическом лактоном кольце.
Таблица 6. Классификация макролидов

Механизм действия
Макролиды – бактериостатические антибиотики, блокирующие синтез белка рибосомами, взаимодействуют с 50S субъединицей бактериальных рибосом.
В высоких концентрациях оказывают бактерицидное действие на пневмококки, ?-гемолитический стрептококк группы А, возбудители коклюша и дифтерии. Эффективны в отношении грамположительных кокков (стрептококков, стафилококков), грамотрицательных кокков (гонококков, менингококков), гемофильной палочки, боррелий, бледной трепонемы, Helicobacter pylori. Хорошо проникают внутрь клеток и активны в отношении внутриклеточных возбудителей (хламидий, легионелл, уреаплазм и микоплазм).
Макролиды – наименее токсичные для макроорганизма антибиотики и одни из самых безопасных групп антимикробных средств.
Показания
Макролиды применяют для лечения стрептококкового тонзиллофарингита, пневмонии (в том числе «атипичной», вызванной микоплазмами, хламидиями и легионеллами), коклюша, дифтерии, скарлатины, инфекций кожи и мягких тканей, хламидиоза, микоплазменной инфекции, инфекций полости рта, для эрадикации H. pylori при язвенной болезни желудка и двенадцатиперстной кишки, при остеомиелите, для профилактики и лечения инфекций, обусловленных Mycobacterium avium (кларитромицин, азитромицин), а также с целью круглогодичной профилактики ревматизма (при аллергии на пенициллины).
Эритромицин – природный макролид, продуцируемый Streptomyces erythreus.
Нежелательные реакции эритромицина, как правило, связаны с влиянием на ЖКТ и печень. Желудочно-кишечные расстройства – наиболее частая причина для прекращения приема эритромицина, так как препарат может непосредственно стимулировать моторику ЖКТ, вызывая тошноту, рвоту, иногда отсутствие аппетита, диарею. Проявление этих нежелательных реакций можно уменьшить, применяя препарат после еды. Эритромицин также может приводить к острому холестатическому гепатиту (с лихорадкой, желтухой и нарушением функции печени), вероятно, за счет реакции гиперчувствительности.
Олеандомицин продуцируется Streptomyces antibioticus. По спектру активности близок к эритромицину, но менее активен.
Рокситромицин и кларитромицин – полусинтетические 14-членные макролиды. Кларитромицин используют для терапии и профилактики оппортунистических инфекций при ВИЧ, вызванных атипичными микобактериями Mycobacterium avium, для эрадикации Helicobacter pylori. Более эффективен в отношении легионелл и других внутриклеточных возбудителей (хламидий, микоплазм).
Азитромицин – полусинтетический 15-членный макролид, относится к подклассу азалидов. В отличие от эритромицина менее эффективен в отношении стафилококков и более эффективен в отношении гемофильной палочки, энтеробактерий, легионелл, токсоплазм.
Спирамицин, джозамицин и мидекамицин – природные 16-членные макролиды. Препараты эффективны в отношении некоторых штаммов стрептококков и стафилококков, резистентных к эритромицину. Препараты переносятся лучше, чем эритромицин, реже вызывают нарушения со стороны ЖКТ.
Показания
Спирамицин назначают для лечения периодонтальных инфекций и гингивитов, как средство первого ряда при токсоплазмозе, в том числе у беременных. Мидекамицина ацетат – полусинтетический антибиотик, пролекарство с улучшенной фармакокинетикой: лучше всасывается из ЖКТ, создает более высокие концентрации в тканях.
Нежелательные реакции
Аллергические реакции, диспепсические расстройства (тошнота, тяжесть в эпигастрии); холестатический гепатит, повышение уровня трансаминаз в плазме; нарушение слуха.
Кетолиды
Телитромицин – полусинтетическое производное эритромицина, 14-членный макролид, у которого к лактонному кольцу при 3 атоме углерода присоединена кетогруппа. Телитромицин, более известный как кетолид, чем макролид, имеет сходный с макролидами механизм действия.
Показания
Телитромицин можно использовать при лечении инфекций, вызванных некоторыми бактериальными штаммами, устойчивыми к макролидам (внебольничные пневмонии, обострение ХОБЛ, острый бактериальный риносинусит и тонзиллофарингит). Среди побочных эффектов наиболее часто вызывает диарею, тошноту, рвоту, головные боли. Реже встречаются нарушения зрения, кожная сыпь, также были отмечены редкие случаи скоротечного некроза печени.
Линкозамиды
Механизм действия линкозамидов подобен макролидам – угнетение синтеза белка на этапе транслокации. Препараты обладают бактериостатическим характером действия преимущественно на грамположительные бактерии – стафилококки (в том числе на стафилококки, продуцирующие пенициллиназу и устойчивые к другим антибиотикам), стрептококки, пневмококки, палочки дифтерии, некоторые анаэробы (в том числе на возбудители газовой гангрены и столбняка, Bacteroides fragilis) и микоплазмы. В высоких концентрациях могут действовать бактерицидно.
В группу линкозамидов входят природный антибиотик линкомицин и его полусинтетический аналог – клиндамицин. Препараты не разрушаются соляной кислотой желудка, депонируются в костной ткани и суставах.
Показания
Линкозамиды применяют как антибиотики второго ряда при инфекциях, вызванных грамположительными кокками при тонзиллофарингите, пневмонии, инфекциях кожи и мягких тканей (пиодермия, фурункулез), костей и суставов (остеомиелит, гнойные артриты), при отитах, интраабдоминальных инфекциях и заболеваниях органов малого таза, в том числе обусловленных бактероидами.
Наиболее важные показания к применению клиндамицина – тяжелые анаэробные инфекции, вызванные бактероидами, и лечение смешанных инфекций, связанных с другими анаэробами. Препарат эффективен в отношении возбудителя пневмоцистной пневмонии. В высоких дозах действует на токсоплазмы и плазмодии, поэтому дополнительные показания к применению – хлорохинрезистентная тропическая малярия (в сочетании с хинином) и токсоплазмоз (в сочетании с пириметамином).
Нежелательные реакции
Клиндамицин может вызывать развитие псевдомембранозного колита, разновидность суперинфекции, обусловленной Clostridium difficile. Входящая в состав нормальной микрофлоры кишечника, C. difficile неконтролируемо размножается при применении клиндамицина или других пероральных антибиотиков широкого спектра действия. C. difficile вырабатывает цитотоксин, приводящий к колиту, для которого характерны изъязвление слизистой оболочки, тяжелая диарея и лихорадка. Для лечения колита назначают внутрь ванкомицин или метронидазол (препарат первого ряда), а также проводят дезинтоксикационную терапию. Также при применении линкозамидов могут возникать диспепсические расстройства (боль в животе, тошнота, рвота, диарея), аллергические реакции, транзиторная нейтропения, тромбоцитопения.
Хлорамфеникол
Хлорамфеникол – антибиотик широкого спектра действия, нарушает синтез белков на рибосомах бактерий, в связи с чем оказывает бактериостатическое действие.
Препарат эффективен в отношении как аэробных, так и анаэробных грамположительных и грамотрицательных организмов. Наиболее чувствительные к нему – Haemophilus influenzae, Neisseria meningitidis, пневмококки и некоторые штаммы бактероидов. Тем не менее возможность развития опасных токсических реакций ограничивает системное применение хлорамфеникола.
Показания
Препарат до сих пор используют в некоторых случаях для лечения брюшного тифа, бактериального менингита и риккетсиозов, но только тогда, когда к более безопасному альтернативному средству приобретена устойчивость или эффективный антибиотик вызывает опасную лекарственную аллергию. Наружно в виде спиртового раствора и линимента применяют при бактериальных инфекциях кожи (фурункулез), инфицированных ожогах, трофических язвах, трещинах сосков у кормящих матерей; в виде глазных капель и линимента – при бактериальных инфекциях глаз (конъюнктивит, блефарит, кератит).
Нежелательные реакции
Основной механизм, лежащий в основе токсичности хлорамфеникола, по-видимому, включает угнетение митохондриального синтеза белка. Одно из проявлений этого токсического действия – «серый синдром» новорожденных, возникающий при применении хлорамфеникола в высоких дозах. Вследствие незрелости систем метаболизма у новорожденных, в частности отсутствия механизма эффективной конъюгации с глюкуроновой кислотой для детоксикации хлорамфеникола, препарат может накапливаться в токсичных концентрациях, вызывая этот синдром. Чаще хлорамфеникол приводит к зависимому от концентрации обратимому угнетению эритропоэза и диспепсическим расстройствам (тошноте, рвоте и диарее). Апластическая анемия – редкое, но потенциально смертельное осложнение.
Аминогликозиды
В основе молекулы аминогликозидов лежит циклический спирт – аминоциклитол, к которому посредством гликозидных связей присоединены аминосахара. Группа аминогликозидов представлена природными и полусинтетическими препаратами, которые принято классифицировать по поколениям. Природные аминогликозиды синтезируются грибами родов Actynomyces (неомицин, канамицин, тобрамицин) и Micromonospora (гентамицин). Все аминогликозиды близки по своим свойствам и различаются, главным образом, по активности, спектру действия, выраженности побочных эффектов и устойчивости микроорганизмов.
Классификация
1. Аминогликозиды I поколения: стрептомицин, неомицин, канамицин.
2. Аминогликозиды II поколения: гентамицин, тобрамицин, нетилмицин.
3. Аминогликозиды III поколения: амикацин.
Механизм действия
Аминогликозиды нарушают синтез белка рибосомами бактерий и повышают проницаемость цитоплазматической мембраны микроорганизмов для ионов и белков, что обусловливает бактерицидный характер действия.
Аминогликозиды – антибиотики широкого спектра антибактериального действия с преимущественным влиянием на грамотрицательную флору. Спектр действия аминогликозидов включает некоторые грамположительные и многие грамотрицательные аэробные микроорганизмы (стафилококки, стрептококки, пневмококки, кишечную палочку, сальмонеллы, шигеллы, клебсиеллы, протей, энтеробактерии, синегнойную палочку).
Аминогликозиды I поколения оказывают угнетающее воздействие на микобактерии туберкулеза, возбудителей туляремии и чумы.
К аминогликозидам не чувствительны анаэробы, спирохеты и простейшие. Аминогликозиды этой группы применяют при инфекциях различной локализации, вызванных грамотрицательными микроорганизмами, а также при туберкулезе, чуме, туляремии, бруцеллезе. Аминогликозиды I поколения в настоящее время применяют ограниченно в связи с быстрым развитием устойчивости микрофлоры и высокой ототоксичностью и нефротоксичностью.
Стрептомицин
Показания
Стрептомицин применяют для лечения туберкулеза (в комбинации с другими противотуберулезными средствами), энтерококкового эндокардита и некоторых особо опасных инфекций – чумы (в комбинации с доксициклином), туляремии, бруцеллеза.
Нежелательные реакции
Стрептомицин оказывает выраженные ото– и нефро– токсическое действия.
Неомицин
Самый ототоксичный аминогликозид. Плохо всасывается из кишечника.
Показания
Препарат применяют внутрь для санации кишечника при подготовке к операциям на ЖКТ, для лечения энтерита, вызванного чувствительными к нему бактериями, местно – для лечения гнойных поражений кожи (пиодермии, инфицированные раны, экземы и др.); в офтальмологии – для лечения конъюнктивитов. Наружно неомицин иногда используют в комбинации с глюкокортикоидамиили бацитрациномдля местного лечения инфицированных ран и бактериальных инфекций кожи. Для парентерального введения препарат не используют в связи с высокой токсичностью.
Канамицин применяют внутрь по тем же показаниям, что и неомицин, и парентерально для лечения туберкулеза (как средство II ряда).
Нежелательные реакции
Препарат обладает выраженной ото– и нефротоксичностью.
Аминогликозиды II поколения высокоактивны в отношении синегнойной палочки и некоторых других микроорганизмов, устойчивых к препаратам I поколения и антибиотикам других групп. Устойчивость к аминогликозидам II поколения развивается медленнее, чем к I поколению, но быстрее, чем к III поколению.
Основной представитель аминогликозидов II поколения – гентамицин, высоко эффективный при инфекциях, обусловленных синегнойной палочкой, практически не действует на микобактерии туберкулеза.
Показания
Препарат применяют, главным образом, при тяжелых инфекциях (сепсис, пневмония, эндокардит, осложненные урогенитальных инфекции, абдоминальные инфекции и др.), вызванных грамотрицательными бактериями, устойчивыми к другим антибиотикам. Гентамицин также эффективен при лечении туляремии. Вводят препарат внутримышечно и внутривенно. Гентамицин используют также местно при лечении инфицированных ран кожи, мягких тканей и ожогов. В офтальмологии применяют в виде глазных капель при бактериальных инфекциях глаз, вызванных чувствительной микрофлорой (блефарит, кератит, кератоконъюнктивит, иридоциклит). При инфекциях, обусловленных клебсиеллой, гентамицин комбинируют с антисинегнойными пенициллинами.
Нежелательные реакции
При применении гентамицина возможно развитие осложнений, типичных для всей группы аминогликозидов, однако ототоксическое действие менее выражено.
Тобрамицин и нетилмицин аналогичны по своим характеристикам гентамицину. Тобрамицин обладает высокой эффективностью в отношении синегнойной палочки, особенно в комбинации с антисинегнойными пенициллинами (карбокси– и уреидопенициллинами). Препарат не действует на энтерококки.
Показания
Нетилмицин эффективен в отношении бактерий, устойчивых к гентамицину и тобрамицину. Нетилмицин оказывает менее выраженное ототоксическое действие по сравнению с другими аминогликозидами.
Аминогликозиды III поколения (амикацин)
В отличие от гентамицина амикацин обладает самым широким спектром антимикробной активности, действует на многие штаммы грамотрицательных бактерий, резистентных к аминогликозидам II поколения, поскольку он не инактивируется бактериальными ферментами. Препарат также эффективен в отношении Mycobacterium avium. В настоящее время амикацин относят к препаратам резерва во избежание развития устойчивости.
Показания
Препарат применяют для лечения наиболее тяжелых инфекций, вызванных множественно устойчивой микрофлорой. Вводят внутримышечно и внутривенно.
При парентеральном применении аминогликозидов необходим систематический контроль функций почек, состояния слуха и вестибулярной системы. Аминогликозиды противопоказаны при заболеваниях почек и слухового нерва, беременности, миастении.
Нежелательыне реакции
Диспепсические расстройства (тошнота, рвота, диарея), нефротоксичность, нарушение функций печени, снижение слуха, вестибулярные нарушения, угнетение нервно-мышечной передачи, проявляющееся ослаблением дыхания, снижением мышечного тонуса и двигательной функции.
Аминоциклитолы
Спектиномицин – антибиотик, продуцируемый Streptomycess pectabilis, структурный аналог аминогликозидов.
Механизм действия
Спектиномицин нарушает синтез белка на стадии транслокации. Препарат с бактериостатическим характером действия и преимущественно грамотрицательным спектром антимикробной активности.
Показания
В клинической практике спектиномицин используют в качестве альтернативного средства для лечения гонореи (острый уретрит, простатит, цервицит и проктит) у больных с гиперчувствительностью к пенициллину или при устойчивости гонококков к средствам 1 ряда при гонорее.
Тетрациклины
К группе тетрациклинов относят природные и полусинтетические антибиотики, структурную основу которых составляют четыре конденсированных шестичленных кольца. Тетрациклины классифицируют в зависимости от способа получения:
1. Природные (биосинтетические) антибиотики: тетрациклин, окситетрациклин.
2. Полусинтетические антибиотики: метациклин, доксициклин.
Механизм действия
Тетрациклины угнетают синтез белков на уровне рибосом бактерий. Антибиотики широкого спектра с бактериостатическим характером действия, наиболее активны в отношении размножающихся микроорганизмов. Высокая степень липофильности обеспечивает хорошую всасываемость препаратов в ЖКТ, способность преодолевать биологические барьеры, накапливаться в тканях, проникать внутрь клеток и воздействовать на внутриклеточных возбудителей – хламидий, легионелл, микоплазм, риккетсий. Важная особенность фармакокинетики этой группы антибиотиков – способность связывать в хелатные комплексы двух– и трехвалентные ионы (железа, кальция, магния, цинка, алюминия). Ионы кальция могут содержаться в молочных продуктах, ионы кальция, алюминия – в антацидах. Во избежание нарушения всасывания тетрациклины, как правило, принимают натощак. Взаимодействие антибиотиков с катионами, в частности с кальцием, может привести к секвестрации препаратов в костях и зубах, что потенциально ведет к аномалиям развития и нежелательному прокрашиванию костной ткани и зубов у пациентов детского возраста. По этой причине тетрациклины не следует назначать детям до 8 лет и беременным. Изменение окраски зубов происходит вследствие способности тетрациклинов поглощать волны УФ-спектра. Тетрациклины могут вызвать значительную фотосенсибилизацию кожи.
Показания
В качестве антибиотиков широкого спектра действия тетрациклины применяют при многих инфекционных заболеваниях. В первую очередь тетрациклины показаны при бруцеллезе (совместно с гентамицином или рифампицином), риккетсиозах (сыпной тиф, ку-лихорадка и др.), чуме, холере, туляремии, боррелиозах (возвратный тиф, болезнь Лайма). Тетрациклины назначают при заболеваниях, вызываемых хламидиями (хламидиоз легких, трахома, орнитоз, мочеполовой хламидиоз и др.), микоплазмами (возбудителями атипичной пневмонии), кишечной палочкой (перитониты, холециститы и др.), шигеллой (бациллярная дизентерия), спирохетами (сифилис), гемофильной палочкой и клебсиеллой. Тетрациклины также используют для эрадикации Helicobacter pylori при язвенной болезни желудка и двенадцатиперстной кишки, амебиазе и для профилактики тропической малярии.
Длительность антибактериального действия тетрациклинов неодинакова. По этому признаку среди них следует различать:
• тетрациклины короткого действия (6–8 часов) – тетрациклин и окситетрациклин;
• тетрациклины длительного действия (12–24 часов) – метациклин и доксициклин.
Тетрациклины обычно назначают внутрь (в капсулах или таблетках, покрытых оболочкой), однако, при тяжелых формах гнойно-септических заболеваний растворимые соли тетрациклинов вводят парентерально (внутримышечно, внутривенно, в полости тела). Тетрациклиновую мазь применяют местно при инфекциях кожи и угревой сыпи; глазную мазь закладывают за нижнее веко при бактериальных инфекциях глаз, вызванных чувствительной микрофлорой (блефарит, кератит, кератоконъюнктивит, иридоциклит).
Нежелательные реакции
Кожная сыпь, крапивница, отек Квинке и анафилактический шок; раздражающее действие на слизистые оболочки пищеварительного тракта (тошнота, рвота, боли в животе, метеоризм, диарея) при пероральном применении, а при внутривенном введении – тромбофлебиты; гепатотоксическое действие; нарушение образования скелета, желтое или серо-коричневое окрашивание и повреждение зубов; дисбактериоз и суперинфекция с развитием кандидомикоза и псевдомембранозного энтероколита; фотосенсибилизация и др.
Глицилциклины
Тигециклин – первый представитель нового класса антибиотиков, производное миноциклина. Четыре кольца структуры тигециклина напоминают тетрациклины.
Механизм действия
Препарат нарушает синтез белка на рибосомах. Тигециклин обладает широким спектром и бактериостатическим характером действия.
Показания
Тигециклин был одобрен для внутривенного введения в лечении тяжелых кожных и интраабдоминальных брюшных инфекций, вызванных как метициллиночувствительными, так и метициллинорезистентными штаммами S. aureus, Escherichia coli, Bacteroides fragilis, Enterococcus faecalis (только ванкомициночувствительные штаммы), стрептококками.
Стрептограмины
Стрептограмины – полусинтетические производные природных пристинамицинов, продуцируемых Streptomyces pristinaespiralis.
Механизм действия
Хинупристин (стрептограмин группы В) и дальфопристин (стрептограмин группы А) угнетают синтез белка на рибосомах. По отдельности эти препараты не применяют. Комбинация препаратов оказывает бактерицидное действие преимущественно на грамположительные бактерии, но на энтерококки (Enterococcus faecium) – бактериостатическое действие.
Показания
Хинупристин + дальфопристин эффективны в отношении возбудителей атипичной пневмонии – микоплазм, легионелл и хламидий. Комбинированный препарат был одобрен для лечения инфекций, вызванных ванкомицин-резистентными штаммами энтерококков (Enterococcus faecium), осложненных и угрожающих жизни инфекций кожи и мягких тканей, обусловленных стрептококками, стафилококками, метициллин-резистентными стафилококками.
Нежелательные реакции
Болезненность и воспаление в месте инъекции (флебиты); диспепсические расстройства; гипербилирубинемия; артралгия; миалгия; головная боль.
Антибиотики, нарушающие проницаемость цитоплазматической мембраны
Полимиксины – группа циклических пептидных антибиотиков, продуцируемых Bacillus polymyxa, впервые были выделены в 1947 г. Их относят к катионным детергентам. Представляют собой поверхностно-активные вещества.
Механизм действия полимиксинов связан с прямым взаимодействием с фосфолипидами цитоплазматической мембраны микроорганизмов и нарушением ее структуры. В результате повышается проницаемость бактериальной мембраны, что способствует выходу из клетки жизненно важных элементов цитоплазмы, в частности ионов Na+ и K+. Полимиксины оказывают бактерицидное действие, эффективны преимущественно в отношении грамотрицательных бактерий – кишечной палочки, сальмонелл, шигелл, клебсиелл, гемофильной палочки, синегнойной палочки.
При назначении внутрь полимиксины не всасываются и плохо абсорбируются со слизистых оболочек и больших ожоговых поверхностей.
Показания
Препараты применяют в основном местно при инфекционных заболеваниях глаз, ушей, кожи, слизистых оболочек. Внутрь назначают при инфекционных заболеваниях кишечника, для санации перед хирургическими операциями (препараты плохо всасываются, и их действие ограничивается кишечником).
Полимиксин В назначают внутрь при инфекциях, вызванных синегнойной палочкой (при условии развития ее устойчивости к уреидопенициллинам, цефалоспоринам, аминогликозидам, фторхинолонам), при инфекционных заболеваниях ЖКТ, вызванных грамотрицательными бактериями. В виде глазных капель применяют при бактериальных инфекциях глаз (конъюнктивит, блефарит, кератит), местно – при наружном отите, синусите, гайморите, ожогах, пролежнях, остеомиелите. Внутримышечно, внутривенно применяют при пневмонии, абсцессе легкого, сепсисе, эндокардите, менингите.
Нежелательные реакции
Нефротоксическое действие (альбуминурия, азотемия); поражение нервной системы (головокружение, нарушения сознания, зрения, сонливость, атаксия, периферические парестезии); нарушение нервно-мышечной передачи (блок натриевых каналов приводит к параличу дыхания, апноэ); суперинфекция (кандидоз); аллергические реакции (кожная сыпь, зуд, крапивница, эозинофилия); диспепсические расстройства (тошнота, боли в эпигастрии, снижение аппетита) при приеме внутрь; тромбофлебит и болезненность в месте инъекции при парентеральном введении.
Полимиксин М
Препарат назначается местно в виде раствора и линимента при медленно заживающих ранах, инфицированных ожогах, язвах, пролежнях, воспалительных болезнях глаз и уха. Внутрь полимиксин М принимают при инфекциях ЖКТ (колиты, энтероколиты), при острой и хронической дизентерии (если другие антибиотики неэффективны), для санации кишечника при подготовке больных к операциям на ЖКТ.
Антибиотики, нарушающие синтез РНК
Рифамицины представлены полусинтетическими производными – рифампицином и рифабутином.
Механизм действия
Рифампицин оказывает бактерицидное действие благодаря образованию стабильного комплекса с бактериальной ДНК-зависимой РНК-полимеразой, тем самым угнетая синтез РНК.
Показания
Препарат обладает широким спектром действия. Особенно эффективен в отношении бактерий, обитающих в фагосомах, поскольку оказывает бактерицидное действие как на вне-, так и на внутриклеточные возбудители, особенно быстро размножающиеся – микобактерии туберкулеза и лепры, бруцеллы, хламидии, легионеллы, риккетсии, стафилококки, стрептококки, кишечная палочка, менингококки и гонококки. Хотя рифампицин можно использовать для профилактики менингококковой инфекции и для лечения некоторых других бактериальных инфекций (бруцеллез), его основное применение – лечение туберкулеза и других микобактериальных инфекций (лепра, атипичные микобактериозы при ВИЧ).
Поскольку быстрое появление резистентности делает терапию туберкулеза одним ЛС не только неэффективной, но и непродуктивной, рифампицин применяют в сочетании с другими противотуберкулезными препаратами.
Нежелательные реакции
Нарушение зрения; понижение АД (при быстром внутривенном введении); флебит (при внутривенном введении); тромбоцитопеническая пурпура; тромбо– и лейкопения, острая гемолитическая анемия; кандидоз ротовой полости; диспепсические расстройства (уменьшение аппетита, тошнота, рвота, боль в животе, диарея); псевдомембранозный колит; гепатотоксическое действие (повышение уровня печеночных трансаминаз и билирубина в крови, желтуха, гепатит); нефротоксическое действие (канальцевый некроз, интерстициальный нефрит, острая почечная недостаточность); аллергические реакции – кожная сыпь, зуд, крапивница, отек Квинке, эозинофилия; артралгия; гриппоподобный синдром; красно-оранжевое окрашивание жидкостей организма (слезной, потовой, мочи).
Рифампицин
Препарат, характерной особенностью которого является способность стимулировать работу микросомальных ферментов печени системы цитохрома Р-450 (индуктор). Он ускоряет метаболизм и укорачивает действие непрямых антикоагулянтов (варфарина), глюкокортикоидов, пероральных контрацептивов, гипогликемических средств для приема внутрь.
Показания
Лечение туберкулеза.
Рифабутин используют как средство II ряда для лечения туберкулеза, по основным характеристикам подобен рифампицину.
Отличия от рифампицина: эффективен в отношении некоторых штаммов микобактерий туберкулеза, устойчивых к рифампицину; более слабый индуктор микросомальных ферментов печени системы CYP3A; более активен в отношении атипичных микобактерий (M. avium).
Нежелательные реакции, характерные для антибиотиков
Нежелательные реакции, характерные для антибиотиков можно разделить на 4 группы:
1. Связанные с действием на иммунную систему.
2. Связанные с химиотерапевтическим действием антибиотиков.
3. Органотропные.
4. Смешанные.
Действие антибиотиков на иммунную систему может проявляться в виде: реакций гиперчувствительности немедленного типа (сыпь, крапивница, зуд, отек Квинке, анафилактический шок); реакций гиперчувствительности замедленного типа (контактный дерматит); снижения активности макрофагов и Т-лифоцитов (иммунодепрессивное действие обусловлено применением антибиотиков широкого спектра действия).
Химиотерапевтическое действие антибиотиков проявляется в виде: реакции обострения или дисбиоза (дисбактериоз, суперинфекция).
Реакция обострения, или реакция Яриша – Герсгеймера, – это интоксикация организма при действии бактерицидных антибиотиков. Под влиянием препаратов в кровь поступают эндотоксины и продукты распада микробных тел, выделяющиеся при массовой гибели и разрушении клеток микроорганизма; в результате повышается температура тела и увеличиваются лимфатические узлы. Реакция обострения – диагностический признак в некоторых сомнительных случаях и показывает эффективность применяемых антибиотиков.
Дисбиоз развивается вследствие гибели значительной части представителей нормальной (защитной) микрофлоры, чувствительных к препарату, и размножения устойчивых к препарату микроорганизмов, включая патогенных и условно-патогенных.
Кандидамикоз полости рта, кишечника, урогенитальный кандидоз – побочный эффект практически любого антибиотика с широким спектром действия. Для коррекции кандидамикоза можно использовать противогрибковый препарат, например, нистатин. Диарея с примесью крови – диагностический признак псевдомембранозного колита, обусловленного размножением Clostridium difficile; как правило, возникает во время приема антибиотиков из группы пенициллинов, цефалоспоринов, линкозамидов и др.
Органотропные нежелательные реакции обусловлены действием антибиотиков на различные органы и ткани: гепатотоксичные антибиотики (макролиды, гликопептиды, рифампицин, тетрациклины и др.); нефротоксичные антибиотики (аминогликозиды, цефалоспорины (цефамандол), полимиксины, гликопептиды и др.); гематологические нарушения, такие как гемолитическая анемия, апластическая анемия, агранулоцитоз, которые могут наблюдаться при приеме хлорамфеникола.






