Диагностика аллергических болезней
Специфическая диагностика
Диагностические аллергены
Диагноз аллергического заболевания устанавливается на основании аллергологического анамнеза, клинических проявлений, тестирования с предполагаемым аллергеном.
Аллергены как диагностические препараты применяются при условии соблюдения общепринятой стандартизации и сертификации, при наличии разрешения к их использованию Фармакологического комитета Соответствующие этим требованиям пыльцовые аллергены производятся Ставропольским институтом вакцин и сывороток, бытовые и пищевые аллергены — Центральным НИИ вакцин и сывороток (г. Москва), грибковые и бактериальные — Казанским НИИ эпидемиологии и микробиологии.
Главным структурным подразделением, в котором проводится комплексная диагностика аллергических заболеваний, является аллергологический кабинет, где работает врач-аллерголог, имеющий сертификат, разрешающий осуществлять аллергологическое тестирование с учетом показаний и противопоказаний для каждого больного.
Перед аллергологическим тестированием пациент проходит осмотр и получает заключение о состоянии здоровья у оториноларинголога и по показаниям у невропатолога, окулиста, дерматолога, женщины также у гинеколога; кроме того, проводятся рентгенологическое обследование органов дыхания и придаточных пазух носа, клинический анализ крови и мочи, ЭКГ.
Общепринятым методом специфической диагностики неинфекционной аллергии являются кожные пробы (скарификационные, внутрикожные) и провокационные аллергологические тесты. Противопоказания к их проведению:
— обострение аллергического заболевания;
— острый инфекционный процесс (ангина, грипп, ОРИ);
— обострение общесоматического заболевания;
— туберкулезный процесс любой локализации в периоде обострения;
— беременность;
— декомпенсированные (или субкомпенсированные) болезни сердечно-сосудистой системы, печени и почек, крови;
— психические заболевания в периоде обострения;
— длительная терапия ппококортикоидами.
Тестирование также не проводится на фоне приема антигистаминных препаратов и после 60 лет.
Специфическая диагностика при сенсибилизации к пыльцовым аллергенам осуществляется за 3–4 месяца до начала цветения растений, к бытовым аллергенам — лучше в летний период, к эпидермальным — после устранения контакта с животными, т. е. в периоды наименьшего контакта с сенсибилизатором.
Кожные пробы
Скарификационные кожные пробы. Для скарификационных проб используются аллергены, содержащие 10 000 PNU. Одновременно можно поставить до 10 кожных проб с различными аллергенами. Проба проводится на волярной поверхности предплечья по средней линии после предварительной обработки кожных покровов 70 % раствором спирта. Насечки на поверхность кожи наносят на расстоянии 5 см (в строгом соответствии с маркировкой) стерильными скарификаторами, отдельными для каждого маркера (нижний с 0,01 % свежеприготовленным раствором гистамина, отступив на 5 см от линии лучезапястного сустава). С помощью положительной пробы с гистамином оценивается нормальная реактивность кожных покровов. На S см выше проводится тест с контрольной жидкостью (контроль отрицательной реакции). Аллергены наносятся в соответствии с маркировкой на расстоянии 5 см. Капли испытуемых растворов наносят на кожу и в капле стерильными скарификаторами, отдельными для каждого аллергена, делают две параллельные царапины длиной до 5 мм. Реакцию немедленного типа определяют через 20 мин (табл. 2).
Проба уколом (prick-test)
Внутрикожные пробы. Проводятся при положительном аллергологическом анамнезе, указании на предполагаемую сенсибилизацию в случае отрицательных или сомнительных результатов скарификационной пробы.
Места проведения внутрикожной пробы, способы подготовки и условия выполнения такие же, как скарификационной пробы. Первоначальное разведение аллергена —1:10 000 (1PNU), и лишь при отрицательном результате с последним разведением оно может быть 1:1000 (10 PNU), 1:100(100 PNU), 1:10(1000 PNU).
В нижнюю треть волярной поверхности предплечья на расстоянии 5 см от лучезапястного сустава вводят тест-контрольную жидкость в количестве 0,02 мл, затем отдельными стерильными шприцами туберкулинового типа вводят каждый аллерген в объеме 0,02 мл на расстоянии 5 см один от другого. Результаты реакции немедленного типа регистрируют через 20 мин (табл. 3).

Провокационные аллергические тесты
В отдельных случаях при проведении кожных проб реакция может быть ложноположительной из-за крайне высокой чувствительности капилляров кожи к механическому раздражению или к консерванту (фенолу). В связи с этим прибегают к высокоспецифичным провокационным аллергическим тестам — назальному капельному или ингаляционному.
Следует помнить, что при проведении провокационных тестов возможны анафилактоидные реакции, которые требуют своевременной неотложной квалифицированной помощи. Поэтому в аллергологическом кабинете, стационаре, где подобное тестирование проводится, должен быть противошоковый набор. Однако при квалифицированном проведении аллергологического тестирования и правильной оценке полученных результатов на всех этапах подобных осложнений удается избежать.
Назальный капельный тест. Может использоваться при сезонном рините в случаях сенсибилизации к пыльце растений, при круглогодичном рините с подозрением на аллергию к бытовой пыли. Проводят в период ремиссии.
Вначале в одну половину носа гашеткой капают 3 капли тестконтрольной жидкости. Если в течение 15 мин отсутствует реакция со стороны слизистой оболочки носа, можно приступить к назальному провокационному тесту с предполагаемым аллергеном. Тест проводят с аллергеном в концентрации, при которой была получена сомнительная реакция в ответ на внутрикожное тестирование, объем аллергена — 3 капли. Если через 10–15 мин получена отрицательная реакция, концентрацию аллергена увеличивают. Тест считается положительным, если после закапывания аллергена в полость носа появляется заложенность носа, ринорея, чиханье.
Провокационная ингаляционная проба проводится в фазе ремиссии заболевания в условиях стационара, чаще при отрицательных результатах скарификационных тестов с аллергенами в диагностике профессиональной бронхиальной астмы.
При испытании небактериальных аллергенов животного или растительного происхождения, содержащих 10 000 PNU, готовят разведения 1:2,1:4,1:8 и т. д. (чаще до 2048), при использовании химических аллергенов применяют специально подобранные концентрации аллергенов, исключающие неспецифические реакции, связанные с запахом вещества или раздражающим действием. Так, по данным В.Н. Ожигановой, М.З. Нариманова, концентрация используемых для ингаляционных провокационных проб бихромата калия составляет 0,01—0,001 %, формальдегида — 0,05—0,01 %, хлористого никеля — 0,01—0,001 %, азотистого кобальта — 0,5–0,005 %, урсола — 0,001—0,0001 %.
Вначале проба проводится с тест-жидкостью — дистиллированной водой в течение 3 мин. При отрицательном результате приступают к провокационной пробе с испытуемым аллергеном в течение 3 мин (время проведения пробы может быть сокращено при положительных результатах). Проба считается положительной при изменении аускультативной картины — удлинении выдоха, появлении сухих свистящих хрипов на выдохе, снижении ЖЕЛ на 10 %, ФОВ1 — на 15–20 %.
Ингаляционная провокационная проба может сочетаться с лабораторными методами аллергодиагностики. По нашим данным, проведение до ингаляционной и через 24 ч после ингаляционной провокационной пробы исследования с помощью иммуноферментного анализа IgE или теста деструкции тучных клеток с тем же профессиональным аллергеном имеет важное практическое значение. Увеличение уровня IgE и процента дегрануляции тучных клеток через 24 ч после ингаляционной провокационной пробы в значительной мере повышает достоверность полученных положительных результатов.
Лабораторные методы специфической аллергодиагностики
Эти методы могут широко использоваться при аллергических заболеваниях в фазе обострения, в периоды массивного контакта с аллергеном, при высокой чувствительности заболевших к аллергену, при наличии противопоказаний, у детей, при идентификации профессиональных аллергических заболеваний, так как исключают возможность появления неспецифических, ложноаллергических реакций.
Среди различных способов специфической аллергодиагностики при реагиновом IgE-зависимом типе более предпочтительно определение моноклональных IgE. Существуют непрямые методы определения IgE и наиболее распространенные прямые методы выявления специфических IgE, основанные на новых технологиях и использовании диагностикумов в виде стандартизованных и сертифицированных аллергенов к ним.
Реакция пассивного переноса по Праустнитцу — Кюстнеру (непрямой метод постановки кожной пробы) чаще используется в детской практике при идентификации пищевой аллергии. Сущность метода заключается в реакции пассивного переноса реципиенту сенсибилизации с помощью внутрикожного введения 0,1 мл сыворотки крови больного с наличием в ней предполагаемых специфических IgE. Спустя 24 ч в этот же участок вводят 0,02 мл предполагаемого аллергена. Реакцию регистрируют через 20 мин. Однако угроза переноса СПИДа, вирусного гепатита и других инфекций не позволяв! широко использовать данный метод.
Определение специфических IgE. Исследование общего IgE осуществляется с помощью бумажного радиоиммуносорбентного теста (метод PRJST), определение аллергоспецифического IgE — радиоаллергосорбентного теста (метод RAST). Наряду с ними в настоящее время для определения аллергоспецифических IgE все шире используется способ иммуноферментного анализа (ИФА).
Метод RAST наиболее специфичен и точен, так как основан на использовании радиоактивной метки. Сущность его заключается в связи специфического IgE исследуемой сыворотки с аллергеном, размешенным на бумажной пластинке. После отмывания неспецифического (общего) IgE в содержимое добавляются меченые 125I антитела против IgE. Образовавшийся радиоактивный комплекс считывается на сцинтилляционном счетчике.
Метод ИФА. Сыворотка обследуемого, содержащая специфические IgE, наслаивается на полистирольную поверхность микропланшет с адсорбированным набором аллергенов, с которыми связываются только определенные специфические IgE.
При точечном иммуноанализе аллергены наносятся в виде точек на нитроцеллюлозные диски.
Для определения концентрации специфических IgE, связанных с аллергеном, добавляются антиантитела (меченные ферментом) к IgE. На следующем этапе с помощью специальных реагентов, воспроизводящих цветную реакцию, интенсивность которой зависит от концентрации специфических IgF в комплексе с аллергеном, определяют содержание специфических IgE фотометрически в вертикальном луче в системе «Унискан» или «Мультискан». В норме она не превышает 210 МЕ/ед.
Наряду с выявлением специфических IgE используются и другие лабораторные тесты для диагностики как антителозависимых реакций (определение показателей специфического повреждения базофилов, аллергических антител в реакции пассивной гемагглютинации, реакция связывания комплемента и др.), так и реакций замедленного (клеточного) типа (реакция торможения миграции лейкоцитов крови — РТМЛ, тест розеткообразующих клеток — РОК, тест повреждения нейтрофилов и др.).
Их применение в аллергологической практике не потеряло своего значения — идентификация повышенной чувствительности к аллергенам, аутоантигенам позволяет осуществлять более целенаправленное лечение и реабилитацию больных.
Реакция прямого специфического повреждения базофилов крови. Базофилы крови, тучные клетки — клетки-мишени в реализации аллергических реакций немедленного типа. IgE с помощью Fc-фрагмента фиксируются на рецепторах мембран этих клеток, а с помощью Fab-фрагмента специфически реагируют с аллергеном. Это сопровождается резкой активацией (дегрануляцией) клеток-мишеней, что и используется в качестве маркера аллергической реакции.
Для постановки реакции 5 мл исследуемой крови добавляют в центрифужную пробирку с 5 каплями 6 % водного раствора трилона Б и инкубируют в течение часа при 37 °C. Образовавшуюся взвесь лейкоцитов с помощью пастеровской пипетки переносят в чистую пробирку, а затем разливают в две центрифужные пробирки по 0,3 мл. В первую пробирку (опытную) добавляют 0,1 мл изотонического раствора хлорида натрия, в котором растворена рабочая доза аллергена, во вторую (контрольную) — 0,1 мл изотонического раствора хлорида натрия без аллергена. Обе пробирки инкубируют в течение 10 мин при 37 °C, затем центрифугируют в течение 10 мин при 1500 об/мин. После чего сливают надосадочную жидкость, а лейкоцитарную массу, оставшуюся на дне пробирки, осторожно встряхивая, разбивают в остатке жидкости, стекающей со стенок. С помощью пастеровской пипетки содержимое каждой пробирки переносят на отдельные предметные стекла (в виде капли на край) и шлифованным краем другого стекла готовят тонкие лейкоцитарные мазки. Мазки окрашивают озин-метиленовым синим по Май — Грюнвальду в течение 1–2 мин после просушивания на воздухе. После промывания препарата в метиловом спирте мазки-препараты микроскопируют с иммерсией (увеличение 10х80). Просчитывают 50 базофилов по краям мазка и число поврежденных средних клеток. Показатель поврежденных клеток в опытном и контрольных препаратах определяют по формуле:

Реакция считается положительной при показателе 1,4 и выше.
Л.A. Дуева с соавт. (1986) подобрали рабочие концентрации и дозы химических аллергенов и антибиотиков для реакции прямого специфического повреждения базофилов крови (табл. 4).
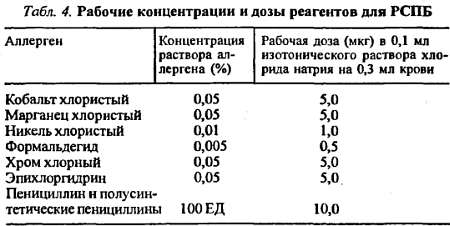
Тест деструкции тучных клеток
Суспензию тучных клеток (0,02 мл) и сыворотку больного (0,02 мл) инкубируют 15 мин при 37 °C, затем вносят 0,02 мл аллергена в предварительно подобранной концентрации и снова инкубируют 15 мин при 37 °C. Одномоментно готовят три контроля: тучные клетки без сыворотки и без аллергена; тучные клетки с сывороткой без аллергена; тучные клетки с аллергеном без сыворотки.
После окраски образцов 0,025 % раствором толуидинового синего или 0,3 % раствором нейтральной краски заполняют суспензией тучных клеток камеры Горяева и подсчитывают окрашенные клетки, сравнивая число гранулированных клеток в контроле и опыте. Наблюдаемая дегрануляция тучных клеток в испытуемом образце считается слабоположительной при наличии 10–20 % дегрануляции, положительной — при 21–40 %1 резкоположительной — при дегрануляции более 40 % клеток по сравнению с контролем. Концентрация аллергенов, не вызывающая спонтанной дегрануляции, для антибиотиков—100—1000 ЕД/мл, калия бихромата и йодида, натрия хромата, никеля сульфата — 0,01—0,1 % раствора, формальдегида—0,2–0,4 %. Бытовые аллергены используются в дозе от 10 цо 100 PNU.
Реакция пассивной гемагглютинации (РПГА) позволяет обнаруживать антитела к водорастворимым и водонерастворимым аллергенам.
Реакция основана на феномене агглютинации эритроцитов, сенсибилизированных in vitro к химическим аллергенам, при добавлении сыворотки пациента, содержащей антигаптенные антитела.
Реакция торможения миграции лейкоцитов крови (РТМЛ) основана на способности сенсибилизированных Т-лимфоцитов (например, к гаптенам) выделять лимфокин — фактор, ингибирующий миграцию лейкоцитов. С помощью PTMЛ раскрывается реакция клеточного типа (неантителозависимая) к различным антигенам.
Перекрестная сенсибилизация и ложноаллергические реакции
Аллергологическое тестирование в сопоставлении с аллергологическим анамнезом и клиническими проявлениями заболевания позволяет идентифицировать наличие сенсибилизации к аллергенам, веществам, содержащим аллергены, установить наличие возможной перекрестной сенсибилизации к ряду продуктов и веществ.
Однако некоторые потенциально существующие аллергены могут вызывать ложноаллергические реакции, клинические признаки которых весьма схожи с проявлениями истинных аллергических реакций; дифференциальная же диагностика часто может быть затруднена без идентификации специфических иммуноглобулинов к тому или иному аллергену.
Как известно, механизм развития аллергических реакций, несмотря на их многообразие, участие в их реализации различных клеток и биологически активных веществ, включает: иммунологическую, патохимическую и патофизиологическую фазы (А.Д. Адо, 1978).
Запуск иммунологической фазы чаще осуществляется при повторной встрече с аллергеном (через 7—14 дней) посредством презентации его макрофагами (неспецифическая форма реагирования) Т-хелперам-2 (Тх2). Тх2 через систему интерлейкинов обеспечивают специфический ответ, опосредованный В-лимфоцитами, трансформирующимися в плазмоциты, экспрессирующими IgE, специфические по отношению к аллергену (специфическая форма реагирования).
Патохимическая фаза характеризуется выбросом тучной клеткой (индуцированной комплексом специфического IgE с аллергеном) ряда биологически активных веществ. Последние весьма многообразны: гистамин и гистаминоподобные вещества уже через несколько минут вызывают немедленную раннюю реакцию; лейкотриены, хемотаксические факторы эозинофилов, нейтрофилов провоцируют позднюю, отсроченно-воспалительную реакцию.
Патофизиологическая фаза аллергической реакции на одни и те же биологически активные вещества, в зависимости от локализации «шокового» органа, проявляется весьма пестрой клинической картиной — ринитом, бронхиальной астмой, альвеолитом, крапивницей, отеком Квинке, анафилактическим шоком (при реагиновом типе реакции).
Однако следует отметить, что ряд потенциальных аллергенов из числа пищевых веществ, гаптенов наряду с истинными аллергическими способны индуцировать ложноаллергические реакции (рис. 2).
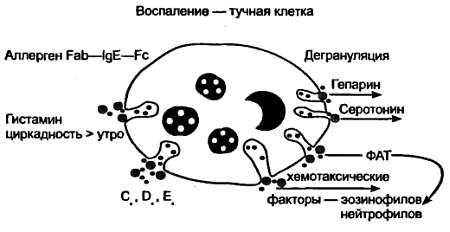
Рис. 2.
Это может быть обусловлено способностью некоторых веществ вызывать высвобождение гистамина из тучных клеток, базофилов неспецифическим путем на холинергической основе с проявлением только патохимической и патофизиологической фазы (при отсутствии иммунологической). Как отмечает Л.В. Лусс (1988), йодсодержащие и рентгеноконтрастные вещества, например, могут осуществлять либерацию медиаторов на неспецифической основе из тучных клеток, базофилов, нейтрофилов и тромбоцитов путем неспецифической активации комплемента.
Стимуляторы высвобождения гистамина, как отмечает Ф.С. Зарудий (1985), весьма разнообразны: свободные высокоокислительные радикалы, ионы кальция, катионный белок эозинофилов, маннитол, хлортетрациклин, декстран, кодеин, препараты сывороточного альбумина, индометацин, карбахолин, морфин, промедол, рентгеноконтрастные вещества и др.
Ложноаллергические реакции в значительной мере провоцируются на фоне ряда заболеваний желудочно-кишечного тракта, гепатобилиарной системы, нейроэндокринопатий, приема продуктов с высоким содержанием гистамина или тирамина. Предрасположенность к ложноаллергическим реакциям при аллергических заболеваниях и без них высока при снижении дезинтоксикационной функции по отношению к гистамину и гистаминоподобным продуктам в связи со снижением активности гистаминазы, гистаминопексической способности тканевых белков (Л.В. Лусс, 1998; В.И. Пыцкий с соавт., 1999). Ложноаллергические реакции возникают при нарушении метаболизма арахидоновой кислоты. Например, нестероидные противовоспалительные средства (препараты салициловой кислоты), анальгетики угнетают активность циклоксигеназы и индуцируют липоксигеназный путь обмена простагландинов, сдвигают баланс в сторону преимущественного образования лейкотриенов и тем самым провоцируют патохимическую фазу ложноаллергической реакции.
В связи с этим приводим обобщенные перечни аллергенов, изделий, содержащих аллергены, и компоненты, обладающие перекрестной сенсибилизацией, в сопоставлении с веществами, вызывающими ложноаллергические реакции (табл. 5,6), что позволит в ряде случаев осуществлять более углубленную дифференциальную диагностику наблюдаемых в общеклинической практике истинных аллергических и ложноаллергических реакций.














