2.8. Экологическая патология детского возраста
Состояние здоровья детей – один из наиболее чувствительных показателей, отражающих изменения качества окружающей среды. Многочисленные данные свидетельствуют о том, что в экологически неблагополучных регионах регистрируется повышенная заболеваемость как взрослых, так и детей.
В зонах экологического кризиса достоверно превышены показатели как младенческой, так и детской смертности, частоты невынашивания беременности сравнительно со средним значением по России. Существенно повышена региональная частота врожденных пороков развития. Она достигает в отдельных регионах 13–14 %. Показано, что в 12 наиболее индустриально развитых регионах России, которые могут быть отнесены к зонам экологического кризиса, уровень младенческой смертности на 25 % выше по сравнению с благополучными областями. Более того, темпы снижения этого показателя в зонах экологического напряжения значительно отстают от его динамики в относительно «чистых» районах.
В структуре причин младенческой смертности в городах с развитой промышленностью врожденные пороки развития и опухоли составляют 36–40 % и занимают первое место. В крупных промышленных городах с загрязнением атмосферного воздуха оксидом углерода, оксидами азота, сернистым газом, пылью основными причинами ранней детской смертности являются асфиксия, родовая травма, врожденные пороки развития, при этом перинатальная смертность в 2 раза превышает таковую в «чистых» зонах. Наиболее высокие показатели детской смертности установлены в возрастной группе детей старше 1 мес. вследствие врожденных пороков, чаще всего – нервной системы, а после года жизни на первое место выходят онкологические заболевания.
В городах России с повышенным уровнем загрязнения атмосферного воздуха сероводородом, углеводородами, фенолом, аммиаком, фтористыми соединениями наблюдается отставание детей в физическом и нервно-психическом развитии; распространенность хронических заболеваний органов дыхания в 1,5–2 раза превышает аналогичные показатели в «чистых» районах (Ревич Б. А., 1993).
Сегодня общепринятыми гигиеническими нормативами, регламентирующими безопасное для человека загрязнение биосферы, являются ПДК химических объектов. Проблема, однако, заключается в том, что безопасного загрязнение окружающей среды не бывает. Кроме того, гигиенические нормативы ПДК вредных веществ в биосфере разработаны на основе изучения реакций взрослых людей и даже экспериментальных животных. Они не предусматривают существование возрастных вариаций чувствительности. Более того, не установлено дозовой зависимости действия антропогенов окружающей среды (в диапазоне допороговых нетоксических концентраций) на здоровье детей с учетом превышения ПДК.
Поэтому для детей и беременных женщин ПДК экопатогенов не известны. Экопатогенные воздействия обусловили появление новых, неизвестных ранее заболеваний, среди которых должны быть названы химическая астма (сульфитная, изотиоцианатная), киширский синдром (астма у детей, сенсибилизированных выбросами заводов по производству полусинтетических кормов для животных), черновицкий синдром, диоксиновый синдром, синдром тотальной аллергии, синдром нездоровых зданий, синдром напряжения – утомления, болезнь Минамата, болезнь Юшо и др.
В первую очередь, на загрязнение окружающей среды реагирует наиболее чувствительное детское население.
Рассматривая различные клинические эффекты, возникающие под действием химических агентов у детей, следует подчеркнуть, что они определяются прежде всего классом опасности вещества, продолжительностью воздействия, а также возрастной и индивидуальной чувствительностью.
При длительном воздействии низких концентраций ксенобиотиков возможно возникновение следующих неоднородных эффектов (Вельтищев Ю. Е., 1998):
– генотоксического эффекта, проявляющегося в нарушении структуры и процессов репарации ДНК. Под генотоксическим эффектом понимают прежде всего способность агентов индуцировать мутации генов соматических клеток (стволовых клеток костного мозга, лимфоцитов, нейтрофилов, фибробластов, эпителия и др.). Такие мутации могут стать причиной серьезных отклонений в состоянии здоровья ребенка, но не наследуются. В постнатальном периоде мутации генов соматических клеток могут быть основой развития аутоиммунных, воспалительных, фибропластических, дегенеративных процессов в различных органах либо вести к злокачественной трансформации клеток. Низкие концентрации химических агентов могут вызывать мутации генов половых клеток, хотя это относится в основном к сильным мутагенам (тиофосфамид);
– ферментопатического действия ксенобиотиков в виде угнетения или активации ферментных систем, распространяется на многие жизненно важные ферменты тканевого дыхания, биоэнергетики, детоксикации, антиоксидантной защиты. Для защитных реакций организма особое значение имеет высокополиморфная система цитохром – Р-450-оксидаз, а также целый ряд других ферментов, которые обеспечивают окисление и конъюгацию ксенобиотиков с глюкуроновой, серной кислотами, глутатионом. Не менее важную защитную роль играют ферменты антиоксидантной защиты, повреждение которых ведет к патологическим реакциям в тканях при контакте с токсичными радикалами. Многие ксенобиотики и в первую очередь тяжелые металлы инактивируют ферменты в результате прямого связывания с белковыми структурами, SH-группами аминокислот. Повреждение ферментов антиоксидантной защиты ведет к патологическим реакциям в тканях при контакте с токсичными радикалами;
– мембранопатологическое действие химических поллютантов, проявляется прежде всего в повреждении мембранных рецепторов для нейромедиаторов, гормонов, интерлейкинов, других молекулярных сигналов межклеточного взаимодействия. Более сильные воздействия ведут к нарушению структуры клеточных, митохондриальных и лизосомальных мембран. Большинство ксенобиотиков с прооксидантными свойствами вызывает деструкцию липидов клеточных мембран с последующим высвобождением медиаторов воспаления и аллергии (простагландины, лейкотриены, липоксины и т. п.). Этот механизм лежит в основе псевдоаллергических реакций (неиммунная – либераторная аллергия);
– метаболических нарушений, их следует отнести к наиболее частым эффектам действия поллютантов. Эти эффекты многообразны и, как правило, неспецифичны, затрагивают самые различные нарушения биоэнергетики, снижение синтеза белков, порфиринов и гемма, нарушение окислительно-восстановительных процессов и метаболизма жирных кислот, аминокислот. Этими свойствами обладает множество ксенобиотиков независимо от класса их токсичности (тяжелые металлы, диоксины, полициклические ароматические углеводороды, фенол, сероводород, кислоты и др.). Ксенобиотики могут связываться с клеточными рецепторами, медиаторами, гормонами либо проявлять действие антивитаминов или гормоноподобных веществ. Многие ксенобиотики действуют как ирританты, вызывая раздражение слизистых оболочек дыхательных путей и приводя к угнетению системы местного иммунитета (твердые частицы, сернистый ангидрид, формальдегид и др.). Дети часто болеют ОРВИ;
– канцерогенного эффекта, проявляющегося через 15–20 лет после начала контакта с вредным фактором.
Экологическая патология детского возраста, по определению академика Ю. Е. Вельтищева (1998), – это прежде всего врожденные пороки развития, аллергические заболевания, хронические нервно-психические заболевания, соматические и онкологические заболевания. Экологическую патологию определяют также: появление необычных заболеваний, атипичность течения известных болезней у детей, а также «омоложение» ряда нозологических форм (язвенная болезнь, гипертоническая болезнь, сахарный диабет, ишемическая болезнь сердца, инфаркт миокарда).
Дети обладают гиперчувствительностью к воздействию неблагоприятных факторов окружающей среды, особенно в критические периоды развития и роста. Наиболее высокая чувствительность к неблагоприятным факторам внешней среды у эмбриона, новорожденного и у детей раннего возраста.
Основными причинами повышенной возрастной чувствительности, по Ю. Е. Вельтищеву (1998), являются:
– высокая интенсивность пролиферативных процессов и дифференцирование клеток в процессе роста (вероятность мутагенных влияний неблагоприятных факторов возрастает в интенсивно пролиферирующих клетках);
– особенности обмена веществ растущего организма, напряженность основного обмена, незрелость ряда ферментных систем, систем детоксикации в раннем возрасте;
– ограничение функциональных возможностей печени и почек, направленных на очищение организма и выведение загрязняющих веществ;
– интенсивные процессы формирования межнейрональных связей в мозге и миелинизации нейронов, повреждение которых тяжелыми металлами, токсичными радикалами или нейротропными пестицидами влечет за собой задержку нервно-психического развития;
– свойственный развивающимся организмам феномен импринтинга – запечатлевания, в том числе метаболического или ферментативного импринтинга, стойкого изменения активности ферментативных реакций трансформации ксенобиотиков. Способностью индуцировать импринтинг обладает большое количество химических соединений. Их воздействие в критический период влечет стойкое изменение ферментативной активности, не свойственное периоду развития. Например, ранняя индукция диоксинами системы оксигеназ или цитохром-Р-450-оксидаз повышает в дальнейшие периоды жизни чувствительность организма к полициклическим углеводородам.
Отдельного рассмотрения заслуживает феномен гормезиса – стимуляция физиологических функций. Некоторые авторы полагают, что очень низкие уровни радиации или концентрации химических веществ могут быть полезными для организма (Luckey Th., 1991). На этой предпосылке основаны методы гомеопатии. В эксперименте на животных было показано, что действие химических агентов в крайне малых дозах на эмбриональной стадии развития повышает резистентность организма к тем же самым агентам в постнатальном периоде жизни. Это считается результатом ферментативного импринтинга.
Однако феномен гормезиса не всегда означает положительное влияние на организм ребенка. С ним могут быть связаны преждевременное половое созревание, раннее проявление аллергии, аутоиммунной патологии, «омоложение» некоторых форм заболеваний, гетерохрония развития органов и систем.
Несмотря на гиперчувствительность детей к факторам окружающей среды, не у всех детей, находящихся в неблагоприятных экологических условиях, развиваются эколого-зависимые нарушения здоровья. Это объясняется неоднородностью (индивидуальной гиперчувствительностью) детской популяции (наследственный полиморфизм человеческой популяции, полиморфизм белков, ферментов, антигенов и т. д.).
Дети с различными проявлениями диатезов (аллергического, лимфатического, дисметаболического, сомато– и нейродиатезов) составляют контингент наивысшего риска развития экопатологии.
Наследственный полиморфизм системы глютатионтрансфераз лежит в основе значительных вариаций чувствительности организмов к действию множества ксенобиотиков. Спектр этих ферментов изменяется также с возрастом ребенка.
Полиморфная система трансферрина определяет разную чувствительность людей к действию токсичных радикалов кислорода. Нетипичные варианты трансферрина крови ассоциируются с повышенной частотой спонтанных абортов, недонашивания беременности, хроническими воспалительными процессами, артропатиями (Beckman L., 1989).
Соотношение людей с сильными, средними и слабыми характеристиками антиоксидантных систем защиты в европейской популяции составляет 5:4:1 (Calabrese E. J., 1986), то есть примерно 10 % людей конституционально слабо защищены от воздействия токсичных радикалов кислорода, азота, серы, постоянно образующихся в атмосфере. Гетерозиготность по ряду мутантных рецессивных генов может резко повышать чувствительность организма к химическим агентам. Так, гетерозиготные носители мутантных аллелей синдромов хромосомной нестабильности (атаксия – телеангиэктазия, анемия Фанкони и др.) составляют контингент очень высокого риска по повреждению ДНК клеток. При этом частота гетерозиготного носительства составляет 4–5 % популяции. У гетерозигот чаще наблюдаются состояния хромосомной нестабильности – ранимость иммунной и нервной систем.
Известны не только возрастные и индивидуальные различия реакций на ксенобиотики, но также этнические вариации. Они могут быть обусловлены этническими особенностями антигенов тканевой совместимости HLA, которые генетически предопределяют подверженность или устойчивость человека по отношению к определенным заболеваниям, прежде всего аутоиммунным.
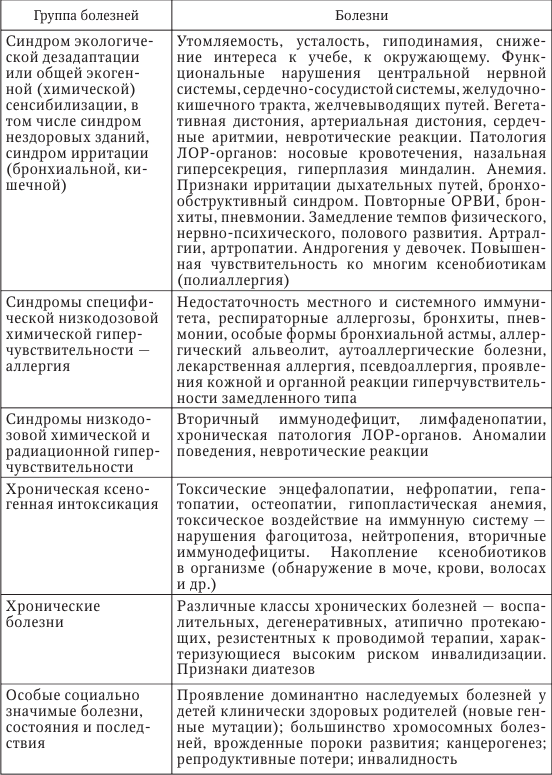
На основании изучения различных форм проявлений экопатологических состояний у детей академиком Вельтищевым Ю. Е. (1998) предложена рабочая классификация этой патологии (табл. 15).
Вопросы экопатологии детского возраста в последние годы стали предметом многих исследований и широко обсуждаются на съездах педиатров России. Этим вопросам посвящен целый ряд монографий: «Экопатология детского возраста» (под ред. Ярыгина В. Н. [и др]., 1995); «Профилактические мероприятия по охране здоровья детей и женщин» (под ред. Алексеева С. В., Янушанец О. И., 1997); «Экология и здоровье детей» (под ред. Студеникина М. Я., Ефимовой А. А., 1998); обзоры Ревича Б. А. (1993, 2001).
Таблица 15
Основные клинические формы экопатологии у детей
(Вельтищев Ю. Е., 1998)

В табл. 16 представлены обобщенные сведения о распространенности хронических форм патологии на экологически неблагополучных территориях по сравнению со средним уровнем по России. Приведенные данные свидетельствуют о том, что в зонах экологического неблагополучия особенно широко распространены пищевая аллергия у детей раннего возраста, аллергические заболевания, болезни ЛОР-органов, гастриты и гастродуодениты, вегетососудистая дистония, врожденные пороки развития, отставание детей в умственном развитии. Указывалось также на задержку физического развития детей, значительную распространенность сколиозов. Несомненно также существование региональных вариаций и этнических различий частоты экологической патологии (Вельтищев Ю. Е., 1998).
На сегодняшний день уже не вызывает сомнения тот факт, что бронхиальная астма является чувствительным маркером загрязнения атмосферного воздуха. Ю. Л. Мизерницкий (1999) указывает, что существуют различные пути реализации действия загрязняющих веществ при бронхиальной астме, которые могут выступать в качестве ирритантов, провоцирующих развитие бронхиальной гиперреактивности, сенсибилизаторов или иммунодепрессоров, ведущих к снижению резистентности организма вследствие угнетения фагоцитарной функции нейтрофилов, снижения факторов местного иммунитета. Основные факторы риска развития бронхиальной астмы представлены в табл. 17.
В зонах экологического неблагополучия достоверно повышена распространенность бронхиальной астмы (БА) (в 1,7–2 раза). По данным Студеникина М. Я. (1994), заболеваемость всеми формами аллергической патологии у детей Москвы достигает 449: 1000. В экологически благополучных регионах она составляет 129: 1000.
Таблица 16
Распространенность хронических форм патологии в среднем по России и на ее экологически неблагополучных территориях (на 1 000 детей)
(Вельтищев Ю. Е., 1998)

Примечание: В таблице использованы данные Баранова А. А. [и др.], 1994; Гресь Н. А., Авдеенко Н. В. [и др.], 1992; Ефимовой А. В. [и др.], 1990; Ревич Б. А. [и др.], 1993, 2001; Игнатовой М. С. [и др.], 1994; Каганова С. Ю. [и др.], 1994; Касаткиной Э. П. [и др.], 1995, и ряда других исследователей.
Таблица 17
Факторы риска развития бронхиальной астмы у детей
(Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика», 1997)

Интенсивный рост распространенности БА отмечается в последние десятилетия во всех развитых странах мира (кроме скандинавских), причем причины такого роста не совсем ясны.
БА в США и Западной Европе страдает от 3 до 7 % детей. В России также отмечено повышение распространенности болезней аллергической природы, но она не достигает такого высокого уровня, как в странах Европы и США: распространенность БА среди детей России в 7—10 раз ниже. Однако не исключено, что в странах Западной Европы имеет место гипердиагностика БА.
Одно из объяснений различия распространенности аллергических болезней в России и в Европе связывает их с различными химико-физическими свойствами атмосферных поллютантов: в Восточной Европе преобладают ирританты, раздражающие дыхательные пути (сернистый газ, крупные пылевые частицы – свыше 10 мкм), которые ответственны за частую заболеваемость детей назофарингитами, ОРВИ, бронхитами (в том числе за формирование групп часто и длительно болеющих детей).
В Западной Европе доминируют оксиды азота, летучие органические соединения, озон и мелкодисперсные пылевые частицы (менее 2,5 мкм) – все они представляют собой сильные адъюванты аллергической сенсибилизации и глубоко проникают в дыхательные пути.
Химические ирританты, почти все тяжелые металлы, диоксины, полихлорированные и полициклические углеводороды оказывают угнетающее влияния на местный, а позднее и системный иммунитет ребенка. Поэтому в зонах экологического неблагополучия распространены признаки вторичного иммунодефицита. Однако выраженность иммунологической недостаточности не достигает крайне тяжелых степеней, которые характерны для первичных наследственных иммунодефицитов. Наиболее информативными проявлениями вторичного иммунодефицита у детей являются не частая их заболеваемость ОРВИ и не спорные отклонения в содержании иммуноглобулинов в крови или снижение Т– или В-лимфоцитов, а частота хронических бронхолегочных заболеваний и поражения ЛОР-органов.
Значительные различия в частоте заболеваемости хроническим тонзиллитом между загрязненными и контрольными зонами также свидетельствуют о недостаточности системного и местного иммунитета. Это полигенное заболевание развивается у детей с лимфатическим диатезом, который по распространенности уступает место лишь аллергическому диатезу (включая атопию и аутоаллергию).
Отражением гипоиммунного состояния у детей служит сниженная напряженность противоинфекционного иммунитета после вакцинации. Н. А. Агаджанян, Л. Г. Кузьменко (1995) приводят следующие данные: при использовании стандартной противокоревой вакцины защитные титры противокоревых антител у детей из экологически неблагополучных регионов выявлены в 32 % наблюдений, а у детей контрольных регионов – в 86 %. Напряженность противодифтерийного иммунитета составила соответственно 36 и 75 %.
Многие ксенобиотики служат причиной серьезных реакций и поражения ЦНС.
Таким образом, здоровье ребенка в значительной степени зависит от здоровья родителей, и в то же время здоровье взрослого населения закладывается в детском возрасте. С медицинской точки зрения, в понятие образа жизни, кроме социально-экономических характеристик, входят и вполне управляемые факторы: санитарная культура, отказ от бесконтрольного приема лекарственных средств, вредных привычек, оздоровление условий труда, быта, адекватная двигательная активность и т. д.