Особенности условий взятия образцов биоматериалов

В соответствии с Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», правилами применения национальных стандартов Российской Федерации – ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения» при взятии образцов для бактериологических исследований особенное внимание должно быть уделено предотвращению загрязнения. Содержимое абсцесса следует набирать через кожу, если это возможно, поскольку ее легче дезинфицировать, чем слизистые оболочки.
Жидкий материал предпочтительнее образцов на тампонах. Секрет, содержащий интерферирующие вторичные микроорганизмы, должен быть удален с поверхности открытой раны, затем образец собирают бактериологическим тампоном круговыми вращательными движениями от центра к периферии раны.
Объем пробы должен быть насколько возможно большим. Образцы для культуры крови, если возможно, следует собирать в период повышения температуры тела. При подозрении на инфекционный эндокардит следует брать не менее десяти культур крови.
Образцы для выделения и идентификации вирусов обычно собирают немедленно после появления симптомов (если возможно – в первые три дня). Для анализа используют образцы на тампонах (из носа, гортани, глаз), смывы из глотки, жидкость из пузырьков при кожных поражениях, кал, мочу и спинномозговую жидкость.
При взятии кожных образцов для микологических исследований соскобы с зон активного поражения берут с помощью скальпеля после тщательной дезинфекции участка кожи. При отложениях на волосах их образцы берут с помощью эпиляционной пипетки или остригают. При поражении ногтей берут их срезы и соскобы с нижней части ногтей.
Для обнаружения дрожжей в моче используют случайный образец мочи, для детекции дрожжей или грибков в мокроте предпочтительнее использовать ее утренний образец.
При диагностике паразитарных заболеваний исследуют кровь (для обнаружения плазмодиев, трипаносомы, лейшмании, микрофилярии), кал (для обнаружения лямблии, гельминтов), образцы тканей пораженных органов (для обнаружения Trichinella spiralis larvae, Echinococcus) или самих паразитов (артроподы: клещи, насекомые), мочу (при мочеполовом шистозомозе).
ПЦР-анализ может быть проведен в образцах: крови с ЭДТУК и цитратом, высушенной крови (на фильтровальной бумаге), костного мозга, мокроты, жидкости из полости рта, бронхиальной лаважной жидкости, спинномозговой жидкости, мочи, кала, биопсийного материала, культуре клеток, фиксированной или покрытой (парафинированной) ткани и т. д.
Важным условием получения достоверных результатов является предотвращение загрязнения образцов экзогенной дезоксирибонуклеиновой кислотой (ДНК), обычными источниками которой являются волосы и кожа людей, дверные ручки, лабораторная мебель, порошки, реагенты, термоциклер и наконечники пипеток. Идеальным средством создания чистой беспылевой среды служат настольные шкафы с ламинарным потоком профильтрованного воздуха.
Взятие образцов для молекулярно-биологических исследований лучше всего проводить в закрытые одноразовые системы, которые должны быть свободны от нуклеаз, для чего подвергаются автоклавированию в токе горячего воздуха. При использовании незакрытых систем для взятия проб следует, по меньшей мере, надевать одноразовые перчатки.
Стеклянная посуда должна обрабатываться 1 %-ным раствором диэтилпирокарбоната, который тормозит РНКазы. Оставшийся препарат следует тщательно удалить путем автоклавирования посуды и последующей ее обработки жаром при температуре 250 °C в течение 4 ч.
Правила первичной обработки образца биоматериала
Важнейшей процедурой первичной обработки образцов биоматериалов после взятия их у пациентов является их кодирование с целью последующей надежной их идентификации. Кодирование видов образцов по характеру внесенных в них добавок закреплено с помощью разного цвета крышек пробирок, содержащих соответствующие добавки: красный/ белый – без добавок, для сыворотки, клинико-химические исследования, серология; зеленый – гепарин, для плазмы, клинико-химические исследования; фиолетовый – ЭДТА, для плазмы, гематологические исследования; голубой – цитрат натрия, для коагулологических исследований; серый – фторид натрия, для исследования глюкозы, лактата. Идентификация образцов от определенных пациентов наиболее рациональна с помощью штрих-кодов, в которых отражены идентификационные признаки пациентов: фамилия, клиническое отделение, фамилия лечащего врача и т. п. Штрих-коды изготавливают в месте взятия образца (при доставке проб из другой лаборатории маркировку допускается проводить в лаборатории, выполняющей анализ) и считывают с помощью специального устройства в клинической лаборатории. В небольших учреждениях возможно ручное кодирование пробирок нанесением на них карандашом по стеклу или фломастером условных знаков, цифр.
Другие процедуры первичной обработки образцов биоматериалов по месту их взятия зависят от общей организации лабораторного обеспечения в данном учреждении. Если процедурные кабинеты расположены в том же здании, что и лаборатория, то контейнеры с образцами следует как можно скорее доставлять в лабораторию, где и будут осуществляться все дальнейшие действия.
Пробы, содержащие инфекционные агенты, следует обрабатывать иначе, чем пробы с относительно небольшим риском инфицирования (подобно большинству проб крови, сыворотки, мочи, кала, тампонам, мазкам и фильтровальным бумажкам).
Биологический материал – кровь
При необходимости более длительного транспортирования в лабораторию образцы свернувшейся крови (обычно свертывание происходит в течение 30 мин), предназначенные для получения сыворотки, должны быть отцентрифугированы на месте не позднее, чем через 1 ч после взятия образца. Кровь для получения сыворотки или плазмы центрифугируют в течение 10–15 мин при ускорении 1000–1200 g (оборотов в минуту). Цитратную плазму для исследований системы свертывания крови центрифугируют в течение 15 мин при 2000 g; для получения плазмы, свободной от тромбоцитов, центрифугирование длится 15–30 мин при 2000–3000 g. Центрифугирование пробирок с капиллярной кровью выполняется при 6000–15000 g в течение 90 с. Обычно центрифугирование проводят при температуре 20 °C – 22 °C. Для отдельных аналитов может требоваться центрифугирование при температуре 4 °C, 6 °C. Мазки крови для дифференциального подсчета лейкоцитов должны быть подготовлены не позднее, чем через 3 ч после взятия образца.
Поскольку нуклеиновые кислоты быстро распадаются, образцы для молекулярно-биологических исследований следует быстро подвергать стабилизации путем инактивации ДНКаз и РНКаз с помощью хаотропных веществ (гуанидин-изотиоцианат-ГИТЦ) и органического растворителя, например, фенола. Конечная концентрация ГИТЦ в стабилизированной пробе должна быть не ниже чем 4 моль/л. Стабилизированный таким способом материал не должен охлаждаться во избежание кристаллизации ГИТЦ. Кровь с ЭДТА для экстракции ДНК из лейкоцитов не требует стабилизации.
Биологический материал – кал
Вегетативные формы паразитов можно обнаружить только в свежих образцах кала в течение 40 мин после испражнения при условии его хранения при температуре 4 °C. Цисты стабильны. Для концентрации паразитов и их сохранения в образцах кала обычно применяют растворы мертиолят-йод-формалин и ацетат натрия-формалин.
Требования к условиям хранения и транспортирования образцов биоматериалов в клиническую лабораторию
Условия хранения образцов биоматериалов, взятых у пациентов, определяются стабильностью в этих условиях искомых аналитов. Максимально допускаемая нестабильность, выраженная в процентном отклонении результата после хранения от исходного уровня, не должна превышать половины размера общей ошибки определения, рассчитываемой из суммы биологической и аналитической вариации данного аналита. Максимально допускаемое время хранения измеряется периодом времени, в течение которого в 95 % образцов содержание аналита сохраняется на исходном уровне.
Стабильность аналитов в различных видах образцов (крови, мочи, спинномозговой жидкости) и проб (сыворотке, плазме, осадке, мазке крови) неодинакова. Данные о стабильности проб следует учитывать и при их хранении после поступления в лабораторию. В отношении аналитов, нестабильных на свету, должны быть соблюдены соответствующие предосторожности (сбор материала в темную посуду, защита образца от прямого света).
Биологический материал – кровь
Содержание электролитов, субстратов, некоторых ферментов может не изменяться при хранении образцов сыворотки крови при температуре холодильника 4 °C в течение до четырех дней. Гемоглобин, эритроциты стабильны в течение одного дня при хранении в закрытой пробирке. Хранение образцов плазмы крови, предназначенной для исследований свертывающей системы, в условиях комнатной температуры более 4 ч не рекомендуется.
Исследование газов крови следует проводить немедленно; при невозможности неотложного исследования – образцы в закрытых стеклянных контейнерах могут храниться в бане с ледяной водой до 2 ч.
При транспортировании в лабораторию контейнеры с образцами крови следует предохранять от тряски во избежание развития гемолиза. Температура ниже 4 °C и выше 30 °C может существенно изменить содержание в образце многих аналитов. Образцы цельной крови пересылке не подлежат.
Биологический материал – моча
Собранную мочу как можно быстрее доставляют в лабораторию. Длительное хранение мочи при комнатной температуре приводит к изменению физических свойств, разрушению клеток и размножению бактерий. Моча, собранная для общего анализа, может храниться не более 1,5–2,0 ч обязательно в холодильнике, применение консервантов нежелательно, но допускается, если между мочеиспусканием и исследованием проходит более 2 ч. Наиболее приемлемый способ сохранения мочи – охлаждение (можно хранить в холодильнике, но не замораживать). При охлаждении не разрушаются форменные элементы, но возможно влияние на результаты определения относительной плотности.
Биологический материал – спинномозговая жидкость
При исследовании в пределах 1 ч пробу не охлаждают. Для транспортирования проб СМЖ используют закрытые пробирки. При исследовании в пределах трех часов – хранить на льду, не замораживать, не фиксировать, не добавлять консерванты. Транспортирование следует осуществлять как можно скорее в связи с нестабильностью клеток. Для цитологических исследований следует отсылать препараты, полученные путем цитоцентрифугирования пробы СМЖ (20 мин при 180 г), которые стабильны в течение 4–6 дней при комнатной температуре. Для длительного хранения после отделения клеток с помощью центрифугирования пробу следует быстро заморозить до минус 70 °C в тщательно закупоренном полипропиленовом сосуде.
Доставка в лабораторию биоматериалов для микробиологического исследования
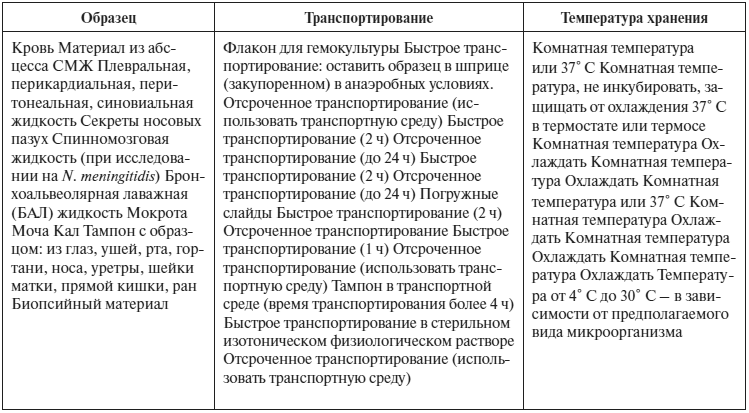
Доставка в лабораторию образца биоматериала должна длиться не более двух часов после взятия материала. Требования к транспортированию и хранению бактериологических проб приведены в таблице. Если соблюдение этих условий не может быть обеспечено, рекомендуется инокуляция во флакон для культур крови или в гемофлакон или, например, для проб мочи, использование погружных слайдов.
Таблица 50
Условия транспортирования и хранения образцов различных биоматериалов для бактериологических исследований
Образцы для обнаружения и идентификации вирусов должны быть доставлены в лабораторию быстро при температуре 4 °C в отдельном контейнере. В этих условиях вирусы обычно остаются стабильными в течение 2–3 дней.
Образцы кожи, волосы и срезы ногтей для микологических исследований отсылают в лабораторию сухими в стерильных контейнерах. Случайный образец мочи для обнаружения дрожжей немедленно отсылают в лабораторию в стерильном контейнере. Также поступают с утренним образцом мокроты для обнаружения в ней дрожжеподобных и плесневых грибов.
Образцы тканей для микологических исследований, помещенные в изотонический раствор, немедленно пересылают в лабораторию. Образцы материала из влагалища, верхних дыхательных путей или кала для микологических исследований (по два тампона с каждым образцом) рекомендуется пересылать в стерильных контейнерах.
При коротком сроке транспортирования образцов для микологических исследований комнатная температура не влияет отрицательно на результаты. При транспортировании на значительные расстояния рекомендуется охлаждение образцов (для образцов на тампонах это не обязательно), чтобы предотвратить подавление бактериями медленно растущих грибов. При подозрении на заражение фикомицетами (например, Mucor) необходимо быстрое транспортирование образца без охлаждения.
В отношении большинства образцов биоматериалов для паразитологических исследований специальные условия транспортировки не обязательны. Артроподы пересылают в лабораторию в 70 %-ном спирте. В таблице приведен перечень преаналитических факторов, которые имеют значение при паразитологических исследованиях.
Таблица 51
Условия хранения и транспортирования образцов для паразитологических исследований

При пересылке образцов должна быть обеспечена их целостность, чтобы результат анализа был правильным и были соблюдены все требования биологической безопасности.
Нормы, регулирующие транспортировку по почте, определяются соответствующими документами. Образцы, пересылаемые по почте, должны «противостоять протеканию содержимого, ударам, изменениям давления и другим воздействиям, которые могут произойти при обычном транспортировании».
Не разрешается использовать стекло в качестве упаковочного материала при транспортировании проб во избежание поломки и возможного вреда для лиц, участвующих в транспортировании.
Рекомендуется следующая структура упаковки для биологического материала:
• внутренняя упаковка для материала пробы;
• абсорбирующий материал;
• наружная упаковка, с информацией об образце и лабораторными формами назначений анализов: коробка, сумка.
Несколько контейнеров с образцами объемом до 500 мл могут быть упакованы в один ящик из картона, дерева, подходящего пластика или металла в соответствии с правилами транспортирования биоопасных материалов. Диагностические образцы, если они не испаряются через упаковку, могут пересылаться в бандеролях.
Упаковки с инфекционными материалами должны быть помечены надписью: ДИАГНОСТИЧЕСКАЯ ПРОБА/ИНФЕКЦИОННАЯ ОПАСНОСТЬ. Ответственность за пересылку по почте инфекционных материалов несет отправитель. Оптимальные сроки доставки проб биоматериала в лабораторию приведены в табл.
При наличии в транспортной упаковке инфекционного материала необходим дополнительный вторичный контейнер для предотвращения любого протекания материала при каком-либо механическом повреждении.