Глава 13. БОЛЕЗНИ ОРГАНОВ ПИЩЕВАРЕНИЯ
АЛИМЕНТАРНАЯ ДИСТРОФИЯ (голодная болезнь, безбелковый отек и др.) – болезнь длительного недостаточного питания, характеризующаяся общим истощением, расстройством всех видов обмена веществ, дистрофией тканей и органов с нарушением их функций.
Этиология, патогенез. Недостаточное поступление в организм и всасывание питательных веществ, обусловленное экзогенными, а также эндогенными причинами (опухолевое, рубцовое сужение пищевода, привратника, синдромы недостаточности пищеварения, всасывания). Имеют значение не только абсолютное, но и относительное (непропорциональное выполняемой физической работе) снижение калорийности пищи, качественные изменения пищевого рациона, особенно дефицит белков (главным образом животных), жиров; недостаток незаменимых аминокислот, жирных кислот и витаминов (в первую очередь жирорастворимых). При продолжительном недостатке питания возникают гипопротеинемия, дистрофические изменения в различных органах и тканях, нарушается функция многих органов, возникает полигландулярная недостаточность. Дистрофические изменения в стенке пищеварительного тракта и пищеварительных железах сопровождаются прогрессирующими нарушениями их функций и еще более усугубляют изменения обмена в организме.
Симптомы, течение. Выделяют 3 стадии алиментарной дистрофии. Стадия I характеризуется понижением питания, поллакиурией, усилением аппетита, жажды, стремлением к повышенному потреблению поваренной соли. Общее состояние больных резко не страдает. Во II стадии наряду с отчетливым похуданием ухудшается общее состояние больных, возникает мышечная слабость, теряется трудоспособность, появляются гипопротеинемические отеки на ногах, умеренная гипотермия тела. Наблюдаются повышенный аппетит и жажда, поли– и поллакиурия, начальные дистрофические изменения в различных органах, изменения психики. Для III стадии характерны кахексия, полное исчезновение подкожной жировой клетчатки, атрофия мышц, резкая слабость (до полной невозможности совершать самостоятельные движения), апатия, выраженные изменения психики, парестезии, полигиповитаминоз, признаки сердечной, печеночной недостаточности, анемия, мучительные запоры, нередко пролежни. Затем развивается выраженная гипотермия (температура тела снижается в отдельных случаях до 30 °C), гипотензия, ацидоз; во многих случаях развивается голодная кома или наступает внезапная смерть.
Течение болезни при отсутствии экстренных мер прогрессирующее вплоть до развития голодной комы. Гибель больных в III стадии алиментарной дистрофии наступает в виде или медленного постепенного умирания, или так называемой ускоренной смерти (в течение суток), вызванной присоединением инфекционной болезни, а также внезапной смерти в момент даже небольшого физического напряжения. Осложнения: присоединение инфекционных заболеваний (пневмония, туберкулез, кишечные инфекции и др.).
Лечение. Соблюдение полного физического и психического покоя в первые дни, полноценное, богатое витаминами и белком питание с постепенным расширением диеты. Одновременно в/в введение плазмы, белковых гидролизатов, витаминов. Симптоматическая терапия: борьба с ацидозом, сердечной и сосудистой недостаточностью, мочегонные средства (при выраженных отеках), анаболические стероидные гормоны. Постепенное расширение режима, лечебная физкультура.
При голодной коме – в/в введение 50 мл 40 %-ного раствора глюкозы каждые 2 ч, кровезаменителей, плазмы, белковых гидролизатов, согревание больного; при выведении из комы – горячий сладкий чай, затем частое дробное кормление больного (небольшими порциями) с использованием наиболее легко усваиваемой пищи.
При алиментарной дистрофии, вызванной нарушением проходимости верхних отделов пищеварительного тракта, в первую очередь – устранение причины (опухолевого или рубцового стеноза пищевода, ахалазии кардии) или паллиативные операции (гастростомия и др.).
АМЕБИАЗ – см. Инфекционные болезни.
АМИЛОИДОЗ – системное заболевание с поражением многих органов и различных тканевых структур, характеризующееся нарушением белкового обмена и внеклеточным отложением в них сложного белковополисахаридного комплекса. Различают следующие основные формы амилоидоза: 1) первичный, по-видимому представляющий собой врожденную ферментопатию, наследуемую аутосомно-доминантным путем (возможно, имеется несколько форм врожденного амилоидоза); 2) вторичный, возникающий на фоне длительных хронических заболеваний, характеризующихся распадом тканей и всасыванием продуктов распада (при туберкулезе легких и других органов, бронхоэктатической болезни, хроническом остеомиелите и др.) или значительными иммунопатологическими нарушениями (неспецифический язвенный колит, сывороточная болезнь и т. д.); 3) идиопатический; 4) старческий.
Поражение пищеварительной системы встречается при любой форме амилоидоза, особенно некоторых ее отделов (языка – макроглоссия, кишечника, печени). В большинстве случаев поражение пищеварительной системы представляет лишь одну из многих локализаций процесса (одновременно имеет место амилоидоз почек, кожи, скелетной мускулатуры, нервной системы и других органов и тканей).
Амилоидоз пищевода встречается чаще одновременно с поражениями других отделов пищеварительной системы. Характерны дисфагия при проглатывании плотной и сухой пищи, особенно при еде лежа, отрыжка. При рентгенологическом исследовании пищевод гипотоничен, перистальтика ослаблена, при исследовании больного в горизонтальном положении взвесь сульфата бария долго задерживается в пищеводе. Осложнения: амилоидные язвы пищевода и пищеводные кровотечения.
Амилоидоз желудка обычно сочетается с амилоидозом кишечника и других органов. Клиническая картина: ощущение тяжести в эпигастральной области после еды, диспептические расстройства; при рентгенологическом исследовании – сглаженность складок слизистой оболочки, ослаб-ление перистальтики и эвакуации содержимого из желудка. Осложнения: амилоидные язвы желудка, желудочные кровотечения, перфорация язв. Дифференциальный диагноз проводят с хроническим гастритом, язвенной болезнью желудка, реже – с опухолью. Решающее значение имеют данные биопсии (выявление амилоидоза).
Амилоидоз кишечника – частая локализация этого заболевания. Проявляется ощущением дискомфорта, тяжести, реже умеренными тупыми или спастическими болями в животе, запорами или упорными поносами. Копрологическое исследование выявляет выраженную стеаторею, амилорею, креаторею. В крови анемия, лейкоцитоз, повышение СОЭ, гипопротеинемия (за счет гипоальбуминемии), гиперглобулинемия, гипонатриемия, гипопротромбинемия, гипокальциемия. Специальные методы исследования обнаруживают нарушение пристеночного пищеварения и всасывания в кишечнике (см. Недостаточности всасывания синдром). При рентгенологическом исследовании характерна развернутость («вздыбленность») кишечных петель, утолщение складок и сглаженность рельефа слизистой оболочки кишки, замедление или ускорение пассажа взвеси сульфата бария по кишечнику. Биопсия слизистой оболочки тонкой и толстой кишок подтверждает диагноз и позволяет провести дифференциальный диагноз с энтеритами и колитами, особенно с неспецифическим язвенным колитом. Изолированный опухолевидный амилоидоз кишечника протекает под маской опухоли (боль, непроходимость кишечника) и обычно обнаруживается уже на операционном столе. Осложнение: тяжелая гипопротеинемия вследствие нарушения процессов всасывания в кишечнике, полигиповитаминозы, стенозирование кишечника, амилоидные язвы, кишечные кровотечения, перфорации.
Амилоидоз печени встречается сравнительно часто. Характерны увеличение и уплотнение печени, при пальпации край ее ровный, безболезнен. Нередок синдром портальной гипертензии, асцит. Реже встречаются боль в правом подреберье, диспептические явления, спленомегалия, желтуха, геморрагический синдром. Лабораторные исследования определяют изменение белково-осадочных проб, гиперглобулинемию, гиперхолестеринемию, в ряде случаев – гипербилирубинемию, повышение активности щелочной фосфатазы, аминотрансфераз сыворотки крови; положительная проба с бромсульфалеином. Решающее значение в диагностике имеет пункционная биопсия печени. Осложнения: печеночная недостаточность.
Амилоидоз поджелудочной железы диагностируется редко (протекает под маской хронического панкреатита); характерны тупая боль в левом подреберье, диспептические явления, панкреатогенные поносы, стеаторея. Исследование дуоденального содержимого выявляет внешнесекреторную недостаточность поджелудочной железы. В тяжелых случаях развивается вторичный сахарный диабет.
Диагноз амилоидоза органов системы пищеварения. Большое значение имеет выявление поражения других органов и систем: почек, сердца, кожи, селезенки и пр.; наиболее достоверным методом диагностики амилоидоза является биопсия органов, в пунктатах которых обнаруживают глыбки амилоида при окраске срезов конго красным, метиленовым или генциановым фиолетовым. При вторичной форме этой болезни важно выявление хронического заболевания, которое обычно осложняется амилоидозом (туберкулез, бронхоэктатическая болезнь, эмпиема плевры и др.). Применяют также функциональные клинические пробы: с конго красным и метиленовым синим (быстрое исчезновение красок при в/в введении из сыворотки крови вследствие фиксации амилоидом и резкое снижение выделения их почками с мочой). Однако при первичном амилоидозе они дают непостоянный результат. Диагноз первичного амилоидоза основан на тщательном генетическом анализе (выявление амилоидоза у родственников). Лабораторные исследования крови обнаруживают диспротеинемию (гипоальбуминемия, гипергаммаглобулинемия; в поздней стадии – увеличение содержания ?2– и ?-глобулинов в сыворотке крови), повышение СОЭ, в ряде случаев – гиперфибриногенемию, повышение содержания холестерина и беталииидов крови. Однако эти изменения неспецифичны для амилоидоза. Течение прогрессирующее. По мере прогрессирования заболевания больные инвалидизируются.
Прогноз неблагоприятный. Смерть больных наступает от истощения, почечной, сердечной недостаточности.
Лечение. При вторичном амилоидозе в первую очередь – лечение основного заболевания (туберкулез, остеомиелит, хроническая эмпиема плевры и др.), после излечения которого нередко исчезают и симптомы амилоидоза. Из специфических средств лечения амилоидоза используют иммунодепрессанты, кортикостероиды. При раннем лечении возможно обратное развитие амилоидоза. Симптоматическая терапия: поливитамины (парентерально), диуретические средства (при выраженных отеках), переливания плазмы. При печеночной недостаточности – соответствующая симптоматическая терапия. При амилоидозе кишечника, протекающем с упорными поносами, – вяжущие средства (нитрат висмута основного, адсорбенты). При изолированном опухолевидном амилоидозе желудочнокишечного тракта – хирургическое лечение.
АХАЛАЗИЯ КАРДИИ (кардиоспазм, ахалазия пищевода, мегаэзофагус, идиопатическое расширение пищевода и др.) – сравнительно редкое хроническое нервно-мышечное заболевание пищевода, характеризующееся нарушением рефлекторного раскрытия кардии при глотании и сопровождающееся нарушением перистальтики и снижением тонуса грудного отдела пищевода.
Этиология изучена недостаточно. Предполагается важная роль вирусной инфекции, генетической предрасположенности; нередко признаки заболевания возникают после психической травмы. В основе патогенеза ахалазии пищевода лежит нарушение деятельности интрамурального нервно-мышечного аппарата пищевода, связанное с дефицитом нейротрансмиттера – окиси азота. Нарушение расслабления нижнего пищеводного сфинктера приводит к тому, что он раскрывается только при механическом воздействии на него накопившейся в пищеводе пищи. При потере тонуса стенок пищевода развивается вторичная его дилатация, если же тонус сохранен – гиперкинетические нарушения перистальтики.
Симптомы, течение. Характерны загрудинная боль, нарушение проглатывания (дисфагия) и пищеводная рвота (регургитация). Загрудинная боль проявляется в виде болевых кризов, часто возникающих ночью; иногда боль возникает при пустом или, наоборот, переполненном пищеводе. Дисфагия вначале эпизодическая, в выраженных случаях наблюдается при каждом приеме пищи и, особенно при проглатывании сухой или плохо прожеванной пищи, усиливается при волнении. Для облегчения прохождения пищи больные выпивают залпом стакан воды или заглатывают воздух, делают глубокие вдохи, выгибают туловище назад и т. д., что в ряде случаев помогает. По мере прогрессирования заболевания появляется дисфагия при приеме жидкостей. Облегчение дисфагии воспринимается больным как «проваливание» пищи в желудок. В противном случае возникает регургитация, проявляющаяся срыгиванием скопившихся в пищеводе слюны, слизи и пищевых остатков. Срыгивание возникает при переполнении пищевода на высоте загрудинного дискомфорта, а также при наклоне туловища вперед или ночью, во время сна. В последнем случае возможна аспирация срыгиваемых масс, что нередко является причиной аспирационных пневмоний. Загрудинная боль возникает чаще ночью, может иррадиировать в шею, нижнюю челюсть, межлопаточное пространство, длится от нескольких минут до нескольких часов, иногда снимается инъекциями анальгетиков и спазмолитиков.
Диагноз подтверждается рентгенологическим исследованием, которое обнаруживает различной степени расширение и удлинение пищевода, в ряде случаев сочетающиеся с его S-образным искривлением, нарушение перистальтики, скопление в пищеводе жидкости натощак. Взвесь сульфата бария длительно задерживается в пищеводе, верхний уровень ее нередко достигает уровня ключиц, после чего она внезапно как бы «проваливается» в желудок. Кардиальный сегмент пищевода сужен, имеет ровные контуры и вид «кончика морковки» или «мышиного хвоста», не раскрывается при глотании, задерживая поступление контраста в желудок; газовый пузырь желудка отсутствует (патогномоничный признак). Прием 1–2 таблеток нитроглицерина расслабляет кардиальный сфинктер, вследствие чего содержимое пищевода легче проходит в желудок и временно устраняется дисфагия. Эта фармакологическая проба облегчает дифференциальную диагностику ахалазии кардии и органических стенозов пищевода. Эзофагогастроскопия помогает в дифференциальной диагностике этих заболеваний. Отсутствие раскрытия кардии при глотании подтверждается при эзофагоманометрии.
Течение обычно прогрессирующее с усилением дисфагии и других симптомов заболевания, нарастающим истощением. Осложнения: хронический застойный эзофагит, сдавление расширенным пищеводом возвратного и блуждающего нервов, правого бронха, верхней полой вены, повторные аспирационные пневмонии и хронические бронхиты. В отдельных случаях могут развиваться дивертикулы пищевода и небольшие аксиальные грыжи пищеводного отверстия диафрагмы. У этих больных отмечено более частое возникновение рака пищевода.
Лечение. Наиболее эффективна эндоскопическая дилатация кардии. При возобновлении спастических сокращений дистальной части пищевода применяют антагонисты кальция (верапамил по 80 мг 3 раза в сутки, нифедипин по 10 мг 4 раза в сутки) и пролонгированные нитраты (например, нитросорбид 20 мг 3–4 раза в сутки), при атонии грудной части пищевода – прокинетики (домперидон, цизаприд), при сопутствующем эзофагите – обволакивающие средства. При неэффективности повторных эндоскопических дилатаций проводится хирургическое лечение – кардиотомия.
Прогноз при своевременном лечении благоприятный.
Профилактика. Больным противопоказана работа, связанная с большой физической нагрузкой и нерегулярным питанием. Диспансерному учету подлежат все больные, не реже 1 раза в год показано рентгенологическое и эндоскопическое исследования.
БРОНЗОВЫЙ ДИАБЕТ – см. Гемохроматоз.
БУЛЬБИТ – см. Дуоденит.
ГАСТРИТ – группа острых и хронических заболеваний, характеризующихся воспалительными или воспалительно-дистрофическими изменениями слизистой оболочки желудка. Диагностика основана, главным образом, на гистологических критериях. Различают гастрит острый (характеризуется нейтрофильной инфильтрацией) и хронический (в инфильтрате определяются нейтрофильные лейкоциты, плазматические клетки и лимфоциты).
Гастрит острый. Этиология, патогенез. Острый гастрит – полиэтиологическое заболевание, обусловленное химическими, механическими, термическими и бактериальными причинами. Патогенез сводится к дистрофически-некробиотическому повреждению поверхностного эпителия и железистого аппарата слизистой оболочки желудка и развитию в ней воспалительных изменений. Воспалительный процесс может ограничиваться поверхностным эпителием слизистой оболочки или распространяться на всю толщу слизистой оболочки, интерстициальную ткань и даже мышечный слой стенки желудка. Острый гастрит часто протекает как острый гастроэнтерит или острый гастроэнтероколит. Различают простой (банальный, катаральный), коррозивный и флегмонозный гастрит; наибольшей клинической значимостью обладает острый стрессорный гастрит.
Гастрит простой встречается наиболее часто. Причиной экзогенного гастрита являются погрешности в питании (употребление перца, горчицы, уксуса, алкоголя и его суррогатов), раздражающее действие некоторых лекарств (например, салицилаты), пищевая аллергия (на землянику, грибы и др.), различные инфекции и т. д.
Симптомы, течение. Симптомы острого гастрита проявляются обычно через 4–8 ч после воздействия этиологического фактора. Появляются тошнота, слюнотечение, неприятный вкус во рту, отрыжка, затем присоединяются схваткообразные боли в подложечной области, рвота не приносящая облегчения, иногда с примесью желчи. Кожные покровы и видимые слизистые оболочки бледные, язык обложен серовато-белым налетом, слюнотечение или, наоборот, сильная сухость во рту. При пальпации выявляется болезненность в эпигастральной области. При эндоскопическом исследовании слизистая оболочка утолщена, гиперемирована, отечна, выявляются геморрагии и эрозии, микроскопически определяется инфильтрация лейкоцитами поверхностного, местами дистрофически, некробиотически измененного эпителия. Длительность заболевания – 2–6 дней.
Лечение. Постельный режим в первые дни, лечебное питание: первые 1–2 дня рекомендуется воздерживаться от приема пищи, но разрешается питье небольшими порциями крепкого чая, боржома; на 2-3-й день разрешают нежирный бульон, слизистый суп, манную и протертую рисовую кашу, кисели. Затем больного переводят на диету № 1, а через несколько дней – на обычное питание. Промывание желудка теплой водой, физиологическим или 0,5 %-ным солевым раствором. При инфекционной этиологии гастрита пока-зано назначение антибактериальных препаратов (энтеросептол по 0,25-0,5 г 3 раза в день, левомицетин по 2 г/сут и др.) и абсорбирующих веществ (активированный уголь и др.). При остром аллергическом гастрите показаны антигистаминные средства. При выраженном болевом синдроме – холинолитические препараты (платифиллина гидротартрат – 1 мл 0,2 %-ного раствора п/к), спазмолитики (папаверина гидрохлорид 1 мл 2%-ного раствора п/к). При обезвоживании – парентеральное введение изотонического раствора хлорида натрия и 5 %-ного раствора глюкозы.
Профилактика простого гастрита сводится к рациональному питанию, строгому санитарно-гигиеническому надзору на предприятиях общественного питания, санитарно-просветительной работе с населением.
Гастрит коррозивный развивается вследствие попадания в желудок крепких кислот, щелочей, солей тяжелых металлов.
Симптомы, течение. Сразу после приема токсичного вещества появляется сильная жгучая боль, часто нестерпимая во рту, за грудиной и в эпигастральной области. Повторная мучительная рвота не приносит облегчения; в рвотных массах – кровь, слизь, иногда фрагменты тканей. На губах, слизистой оболочке рта, зева и гортани – следы химического ожога: отек, гиперемия, изъязвления (от серной и хлористоводородной кислоты появляются серовато-белые пятна, от азотной – желтые и зеленовато-желтые струпья, от хромовой – коричневато-красные, от карболовой – ярко-белые, напоминающие налет извести, от уксусной – поверхностные беловатосерые ожоги). При поражении гортани появляются охриплость голоса и стридорозное дыхание. В тяжелых случаях развивается шок. Живот обычно вздут, болезнен при пальпации в подложечной области; иногда выявляются признаки раздражения брюшины. Острая перфорация наступает у 10–15 % больных в первые часы после отравления (реже – позднее).
Прогноз зависит от тяжести воспалительно-деструктивных изменений и терапевтической тактики в первые часы и дни заболевания. Угрожающий жизни период болезни продолжается 2–3 дня, смерть может наступить от шока или перитонита. Исходом коррозивного гастрита могут быть рубцовые изменения, особенно в пилорическом и кардиальном отделах желудка.
Лечение начинают с промывания желудка большим количеством воды через зонд, смазанный растительным маслом (противопоказаниями к введению зонда являются коллапс и деструкция пищевода). При отравлении кислотами к воде добавляют молоко, оксид магния, известковую воду, при поражении щелочами – разведенную лимонную или уксусную кислоту. Перед промыванием, особенно при болевом синдроме, показаны наркотические анальгетики (морфина гидрохлорид, промедол), фентанил с дроперидолом. При падении АД, кроме того, допамин, норадреналин (п/к или в/в с кровезаменителями, глюкозой, изотоническим раствором хлорида натрия). В течение первых дней – голодание, парентеральное введение изотонического раствора хлорида натрия, 5 %-ного раствора глюкозы. При невозможности в течение ближайших дней питания через рот – парентеральное введение плазмы, белковых гидролизатов. При перфорации желудка, отеке гортани – срочное оперативное лечение. Для предупреждения сужения пищевода производят бужирование в период заживления; при неэффективности последнего – оперативное лечение стеноза.
Гастрит флегмонозный (флегмона желудка) встречается крайне редко, характеризуется флегмонозным воспалением стенки желудка с диффузным или ограниченным распространением гноя преимущественно в подслизистом слое; распознается обычно при хирургическом вмешательстве. Обычно сопровождается развитием перигастрита и нередко перитонита. Возникает чаще первично; вызывается стрептококками, в том числе в сочетании с кишечной палочкой, реже стафилококком, пневмококком, протеем и др. Иногда развивается как осложнение язвы или распадающегося рака желудка, повреждения слизистой оболочки желудка при травме живота. Вторичная форма развивается при общих инфекциях (сепсис, брюшной тиф и др.).
Симптомы, течение. Характерно острое развитие с ознобом, повышением температуры тела, резкой адинамией, болью в верхней половине живота, тошнотой и повторной рвотой, иногда – с кровью, гноем. Язык сухой, живот вздут. Общее состояние резко ухудшается. Больные отказываются от еды и питья, быстро истощаются, изменяются черты лица (так называемое лицо Гиппократа). В подложечной области при пальпации – болезненность. В крови высокий нейтрофильный лейкоцитоз с токсической зернистостью, повышенная СОЭ, изменения белковых фракций и другие признаки воспаления. При эндоскопическом исследовании – складки слизистой оболочки грубые, покрыты фибринозными наложениями; микроскопически выявляют лейкоцитарную инфильтрацию всех слоев стенки желудка. Возможны осложнения (гнойный медиастинит, плеврит, поддиафрагмальный и печеночный абсцессы, тромбофлебит крупных сосудов брюшной полости, сепсис и др.). Прогноз во многих случаях неблагоприятный.
Лечение проводят в основном в хирургических стационарах. Парентерально вводят антибиотики широкого спектра действия в больших дозах. При неэффективности консервативной терапии – хирургическое лечение.
Острый стрессорный гастрит (острый эрозивный гастрит, острая язва желудка, острый геморрагический гастрит) развивается после хирургической операции, при ожогах с поражением 20–40 % кожного покрова, на фоне тяжелой травмы (особенно в сочетании с шоком, гиповолемией, гипоксией) или болезни (при почечной, печеночной, дыхательной, сердечной недостаточности и др.). Секреция соляной кислоты значительно возрастает при черепно-мозговой травме, что может приводить к повреждениям слизистой оболочки не только желудка, но и двенадцатиперстной кишки (язвы Кушнера).
Симптомы, течение. Первым признаком острого стрессорного гастрита, как правило, служит желудочно-кишечное кровотечение, поскольку пациенты в тяжелом состоянии, как правило, не обращают внимание на симптомы диспепсии. При эндоскопическом исследовании выявляют гиперемию и кровоточивость слизистой оболочки желудка, множественные эрозии и изъязвления. Прогноз во многих случаях неблагоприятный.
Лечение включает применение антисекреторных средств – 100 мг ранитидина (зантака) однократно, затем внутрь по 150 мг 2 раза в сутки, или 40 мг фамотидина (кваматела) в/в однократно, затем внутрь по 20 мг 2 раза в сутки, или омепразола (лосека) 40 мг в/в однократно, затем внутрь по 20 мг 2 раза в сутки. Применяется эндоскопическая коагуляция, по строгим показаниям проводится хирургическое лечение (послеоперационная летальность достигает 50 %).
Профилактика острого стрессорного гастрита – адекватная терапия критических состояний. Больным с высоким риском развития стрессорного гастрита показано профилактическое назначение антацидных и антисекреторных препаратов.
Гастрит хронический характеризуется хроническим воспалением слизистой оболочки (в ряде случаев и более глубоких слоев) стенки желудка.
Этиология, патогенез. В происхождении гастрита типа А (аутоиммунного атрофического гастрита) важную роль играет наследственность, заболевание носит семейный характер. В основе его патогенеза лежит аутоиммунный механизм, о чем свидетельствует обнаружение антител к париетальным клеткам слизистой оболочки желудка у этих пациентов. Гастрит протекает с поражением тела и дна желудка, сопровождается снижением кислотности желудочного сока. Со временем атрофия слизистой оболочки желудка приводит к нарушению всасывания витамина B12 и развитию B12-дефицитной анемии.
При неатрофическом гастрите (тип В, хеликобактерный гастрит) в большинстве случаев обнаруживают инфицирование слизистой оболочки желудка Helicobacter pylori, с чем и связывают его происхождение. Воспалительный процесс на начальных этапах локализуется в антральном отделе желудка, характерно сохранение или повышение кислотообразующей функции желудка (гиперсекреторный гастрит). По мере прогрессирования гастрита различия между типом В и типом А стираются – воспаление охватывает все отделы желудка (возникает пангастрит), развивается диффузная атрофия и метаплазия его слизистой оболочки, секреция соляной кислоты уменьшается.
Между активностью хронического гастрита и выявляемостью Helicobacter pylori в слизистой оболочке желудка отмечена четкая зависимость. Однако хеликобактерная теория возникновения хронического гастрита встретила ряд возражений. Как было установлено, эти микроорганизмы обнаруживаются преимущественно при поверхностных формах хронического гастрита, тогда как при прогрессировании атрофических изменений с уменьшением секреции соляной кислоты выявляемость их снижается, а в ряде случаев (например, при B12-дефицитной анемии) они вообще не определяются.
Более редкие особые формы гастрита: химический (рефлюкс-гастрит, тип С, развивается под воздействием химических раздражителей – при раздражении слизистой оболочки желудка кишечным содержимым после резекции желудка, дуоденогастральном рефлюксе желчи, злоупотреблении алкоголем, под влиянием нестероидных противовоспалительных средств); радиационный (при лучевых поражениях); лимфоцитарный (ассоциированный с целиакией); неинфекционный гранулематозный (при болезни Крона, гранулематозе Вегенера, инородных телах); эозинофильный (аллергический).
Симптомы, течение. Заболевание часто протекает бессимптомно. При аутоиммунном гастрите (тип А), сопровождающемся секреторной недостаточностью, могут наблюдаться желудочная диспепсия (тупые боли, чувство тяжести, распирания в подложечной области после еды), неприятный вкус во рту, отрыжка воздухом и пищей, анорексия, тошнота, а также метеоризм, диарея. При развитии В12-дефицитной анемии больных начинают беспокоить быстрая утомляемость, жжение языка, парестезии, при осмотре выявляют «лакированный» язык, бледность кожи, субиктеричность склер и др. При исследовании желудочного содержимого определяется гипоацидность. Эндоскопическое исследование выявляет бледность слизистой оболочки, просвечивание сосудов; преимущественная локализация изменений – дно и тело желудка.
При неатрофическом гастрите (тип В) симптомы могут напоминать клиническую картину язвенной болезни – голодные и ночные боли в подложечной области, тошнота и рвота, отрыжка кислым и изжога, а также запоры. При эндоскопическом исследовании в антральном отделе желудка на фоне гиперемии и отека слизистой оболочки нередко выявляют подслизистые кровоизлияния и эрозии. Проявлениями рефлюкс-гастрита (тип С) могут быть боль в подложечной области после приема пищи, рвота желчью, приносящая облегчение, похудание.
Диагноз гастрита подтверждается при гистологическом исследовании. Точная картина может быть получена при исследовании пяти биоптатов – двух из антрального, двух из дна желудка и одного из области угла желудка. При оценке тяжести гастрита учитывают степень обсеменения Helicobacter pylori, выраженность нейтрофильной и мононуклеарной инфильтрации, стадии атрофии и кишечной метаплазии. Инфицирование Helicobacter pylori выявляется с помощью ряда тестов – бактериологического, гистологического, цитологического, дыхательного и уреазного.
Гастрит с сохраненной и повышенной желудочной секрецией, часто проявляющийся болями, следует дифференцировать с язвенной болезнью. При гастрите отсутствует сезонность обострений, на высоте обострения не выявляется изъязвление слизистой оболочки желудка. Диспепсия требует исключения других заболеваний со сходной клинической картиной, в частности, рака желудка.
Все формы хронического гастрита характеризуются обычно многолетним течением, нередко с чередованием периодов обострения и ремиссии. С годами хронический гастрит приобретает, как правило, прогрессирующее течение.
Лечение. При отсутствии клинических проявлений гастрита в медикаментозном лечении нет необходимости. При появлении клинической симптоматики терапию обычно проводят в амбулаторных условиях, при обострениях целесообразна госпитализация. Важную роль играет лечебное питание. В период обострения болезни питание должно быть дробным, 5–6 раз в сутки; при рефлюкс-гастрите целесообразен прием пищи в положении лежа. Диетотерапия строится с учетом характера секреторных нарушений. При хроническом гастрите с секреторной недостаточностью (тип А) назначают диету № 2 (механическое щажение желудка со стимуляцией секреторной активности), при хроническом гастрите с повышенной секрецией (тип В) – диету № 1. В период стихающего обострения диета должна быть полноценной, ограничиваются лишь поваренная соль, углеводы и экстрактивные вещества, особенно при повышенной кислотности желудочного сока.
При симптомах диспепсии используют прокинетики (домперидон – мотилиум по 10 мг 3–4 раза в сутки, цизаприд – координакс по 5 мг 3–4 раза в сутки) и антациды (маалокс, альмагель, фосфалюгель и т. п. по 15 мл через 1,5–2 ч после еды и перед сном).
При выявлении Helicobacter pylori эрадикационная терапия (направленная на полное его уничтожение в желудке и двенадцатиперстной кишке) считается показанной при эрозивном гастрите, в случае выраженной атрофии слизистой оболочки желудка и кишечной метаплазии. Рекомендуют следующие схемы эрадикационной терапии: 1) пилорид (ранитидин/висмут цитрат) 400 мг 2 раза в сутки в течение 4 нед + кларитромицин 250 мг 2 раза в сутки, или тетрациклин 1 г 2 раза в сутки, или амоксициллин 1 г 2 раза в сутки + метронидазол (трихопол) 0,5 г 2 раза в сутки или фуразалидон 0,2 г 2 раза в сутки, продолжительность антимикробной терапии 7 дней; 2) ранитидин 150 мг 2 раза в сутки или фамотидин 20 мг 2 раза в сутки в течение 7 дней, далее доза уменьшается вдвое и лечение продолжается еще 3 нед + де-нол 240 мг 2 раза в сутки, или вентрисол 120 мг 4 раза в сутки, или бисмофальк 150 мг 4 раза в сутки, или викалин по 1 таблетке 4 раза в сутки + кларитромицин, или тетрациклин, или амоксициллин (продолжительность терапии препаратами висмута и антимикробными средствами – 7 дней).
При аутоиммунном гастрите повысить секреторную функцию желудка помогают сок подорожника, плантаглюцид, различные горечи. Заместительная терапия ахлоргидрии проводится натуральным желудочным соком. При доказанной пернициозной анемии в/м вводят оксикобаламин или цианокобаламин в дозе 1000 мкг в сутки в течение 6 дней, затем в течение месяца ту же дозу вводят 1 раз в неделю, в дальнейшем пожизненно 1 раз в 2 мес.
При рефлюкс-гастрите для улучшения опорожнения желудка применяют прокинетики – домперидон (мотилиум) или цизаприд (координакс), для нейтрализации раздражающего действия желчи на слизистую оболочку желудка – антациды.
Санаторно-курортное лечение хронического гастрита проводится вне обострения болезни на курортах Боржоми, Дорохово, Ессентуки, Железноводск, Пятигорск, Трускавец и др. Целесообразно применение минеральных вод: при пониженной кислотности предпочтительно употребление вод соляно-щелочных источников (например, Ессентуки № 17) за 15–20 мин до приема пищи, а при сохраненной и повышенной секреторной функции – гидрокарбонатных (Боржоми, Ессентуки № 4, Славянская, Смирновская и др.) за 1 ч до приема пищи и во время изжоги.
Прогноз в отношении жизни благоприятный: под влиянием лечения в большинстве случаев сравнительно быстро улучшается самочувствие больных, но основные морфологические изменения хронического гастрита и нарушения секреторной функции желудка, как правило, остаются. При хроническом гастрите, по-видимому, увеличивается риск развития язвенной болезни. Кроме того, хронический гастрит нередко рассматривают как предопухолевое заболевание.
Профилактика хронического гастрита – соблюдение режима питания, отказ от курения и злоупотребления алкоголем, санация полости рта, выявление и лечение других заболеваний органов пищеварения. Больные остаются под диспансерным наблюдением пожизненно, лечение и обследование проводится «по требованию» – при появлении клинической симптоматики.
ГАСТРИТ ГИПЕРТРОФИЧЕСКИЙ (болезнь Менетрие) – особая форма гастрита, характеризующаяся резкой гипертрофией слизистой оболочки желудка с развитием в ней множественных аденом и кист.
Этиология, патогенез. В происхождении гипертрофического гастрита могут играть роль хроническая интоксикация (свинцом, алкоголем), алиментарные погрешности, недостаточное употребление витаминов, курение, перенесенные инфекционные заболевания (брюшной тиф, вирусный гепатит, дизентерия), нейрогенные и наследственные факторы, метаболические нарушения, пищевая аллергия. Существующие теории рассматривают гипертрофический гастрит как результат аномалии развития, следствие воспалительных изменений слизистой оболочки желудка, вариант доброкачественного опухолевого процесса.
Симптомы, течение. Клиническая картина характеризуется болями в эпигастрии, тошнотой, диареей; наличием в слизистой оболочке желудка множественных или единичных аденом и кист, вследствие чего ее складки приобретают резко утолщенный грубый вид; повышенной потерей белка с желудочным соком, гипопротеинемией (в тяжелых случаях). Дифференциальный диагноз с опухолью желудка основан на рентгенологическом и эндоскопическом исследовании с прицельной биопсией (из-за глубокого залегания аденоматозная ткань не всегда попадает в биоптат). Дозированное раздувание желудка при проведении этих исследований облегчает диагноз, вызывая сглаживание желудочных складок (в отличие от опухолевой инфильтрации).
Течение заболевания может быть длительным, многолетним с наличием периодов продолжительной ремиссии заболевания; иногда наблюдают трансформацию гипертрофического гастрита в хронический атрофический гастрит. Возможное осложнение – желудочные кровотечения.
Лечение. Щадящая диета с повышенным содержанием белка, применение обволакивающих и вяжущих средств, антихолинергических препаратов (гастроцепин по 25 мг 4 раза в сутки).
ГАСТРОЭЗОФАГЕАЛЬНАЯ РЕФЛЮКСНАЯ БОЛЕЗНЬ хроническое рецидивирующее заболевание, обусловленное спонтанным, регулярно повторяющимся забрасыванием желудочного и (или) дуоденального содержимого в пищевод. Если у пациента с типичной клинической картиной гастроэзофагеальной рефлюксной болезни (ГЭРБ) при эндоскопии вы-является воспалительное повреждение слизистой оболочки пищевода, диагностируется рефлюкс-эзофагит; если повреждения отсутствуют, говорят об «эндоскопически негативной» ГЭРБ.
Этиология, патогенез. Желудочно-пищеводный рефлюкс развивается главным образом при недостаточности нижнего пищеводного сфинктера. Относительная недостаточность кардии возникает при повышении внутрижелудочного давления, абсолютная недостаточность может быть обусловлена органическими изменениями гладкомышечных волокон пищевода (например, вследствие хирургического вмешательства, бужирования пищевода, при системной склеродермии) или нарушением его нервной регуляции. Тонус нижнего пищеводного сфинктера снижается при употреблении некоторых продуктов питания (шоколада, кофе, цитрусовых, томатов), под влиянием алкоголя, никотина, некоторых лекарственных средств (антагонистов кальция, нитратов, бета-адреноблокаторов, холинолитиков, теофиллина и др.). Кроме того, к возникновению заболевания предрасполагают вынужденное положение тела с наклоном туловища, ожирение, беременность. Определенную роль может играть наличие грыжи пищеводного отверстия диафрагмы.
Симптомы, течение. Основные проявления ГЭРБ – изжога, кислая отрыжка, ощущение жжения или боль за грудиной, возникающие после еды (особенно, жирной), при наклоне туловища вперед, нередко – ночью, а также отрыжка воздухом, дисфагия.
Диагноз уточняется при рентгенологическом исследовании, выявляющем грыжу пищеводного отверстия диафрагмы, суточном мониторировании пищеводного рН (при кислотном рефлюксе рН снижается до 4 и менее) и при эндоскопии, позволяющей подтвердить воспаление и изъязвление слизистой оболочки пищевода. Различают 4 степени рефлюксэзофагита: I – единичные несливающиеся эрозии; II – сливающиеся эрозии, не захватывающие всю поверхность слизистой оболочки дистального отдела пищевода; III – язвенные поражения нижней трети пищевода, сливающиеся и охватывающие всю поверхность слизистой оболочки дистального отдела пищевода; IV – хроническая язва, стеноз пищевода, пищевод Баррета.
Дифференциальный диагноз проводят с ишемической болезнью сердца, стенокардией; однако в отличие от ангинозных приступов, боль при гастроэзофагеальной рефлюксной болезни возникает не при нагрузке, а в горизонтальном положении, связана с приемом пищи, купируется не нитратами, а антацидами.
В большинстве случаев заболевание протекает без существенного прогрессирования; периоды ремиссии могут достигать нескольких лет; частые рецидивы могут наблюдаться при выраженном эрозивном рефлюксэзофагите. Возможные осложнения – пептические язвы пищевода, пищеводно-желудочные кровотечения, стенозирование пищевода, развитие пищевода Баррета (характеризуется обнаружением в биоптатах цилиндрического эпителия, значительно увеличивает риск возникновения рака пищевода). Попадание желудочного содержимого в дыхательные пути может приводить к развитию у этих больных ларингита, фарингита, бронхообструктивных заболеваний, аспирационных пневмоний и др.
Лечение. Диетотерапия: частое, дробное питание; прием пищи, не позднее чем за 3–4 ч до сна; отказ от употребления продуктов, снижающих тонус нижнего пищеводного сфинктера, прекращение приема алкоголя и курения. Целесообразно избегать приема лекарств, способствующих рефлюксу. Снижение массы тела при ожирении; с целью предотвращения желудочнопищеводного рефлюкса запрещают физическую работу, связанную с наклоном туловища и напряжением брюшного пресса, ношение тесной одежды, тугих поясов. Спать рекомендуется с приподнятой верхней половиной туловища.
Медикаментозная терапия: при отсутствии видимых повреждений пищевода применяют комбинацию про кинетика (домперидон – мотилиум, или цизаприд – координакс) и антацида (маалокс, ренни и т. п. 3 раза в сутки за 1 ч до еды), продолжительность курса – 10 дней. При рефлюкс-эзофагите к терапии добавляют препараты, подавляющие желудочную секрецию (блокатор Н2-гистаминовых рецепторов – ранитидин или фамотидин, либо ингибитор протонного насоса – омепрозол, или рабепразол, или лансопразол). Дозы препаратов и продолжительность терапии зависят от выраженности эндоскопических изменений. При рефрактерных формах заболевания используют также сукральфат (вентер, сукратгель) по 1 г 4 раза в сутки за 30 мин до еды. При развитии осложнений (стриктур пищевода, повторных кровотечений, пищевода Баррета, аспирационных пневмоний) возможно хирургическое восстановление функции нижнего пищеводного сфинктера.
Профилактика. Больные подлежат пожизненному диспансерному наблюдению, обследование (осмотр, общий анализ крови, мочи) проводится один раз в год, контрольное эндоскопическое исследование показано больным, у которых не достигнута ремиссия либо выявлен пищевод Баррета.
ГАСТРОЭНТЕРИТ– см. Гастрит; Энтерит.
ГАСТРОЭНТЕРОКОЛИТ– см. Гастрит; Энтерит; Колит.
ГЕМОХРОМАТОЗ (пигментный цирроз печени, бронзовый диабет, синдром Труазье – Ано – Шоффара, сидерофилия и др.) – общее заболевание, характеризующееся нарушением обмена железа, повышенным его содержанием в сыворотке крови и накоплением в тканях и внутренних органах. Встречается сравнительно редко, преимущественно у мужчин.
Этиология, патогенез. Первичный («идиопатический») гемохроматоз относят к ферментопатиям и рассматривают как врожденное заболевание с аутосомно-рецессивным типом наследования, при котором в тонком кишечнике человека всасывается значительно больше железа, чем в норме, и оно избыточно депонируется в тканях – в печени, поджелудочной железе, миокарде, коже и т. д. в основном в виде нерастворимого гемосидорина. Возникает вторичная воспалительно-склеротическая реакция тканей пораженных органов. В гладких мышцах также избыточно откладывается липофусцин, в эпидермисе – меланин. Вторичный гемохроматоз возникает при избыточном поступлении в организм железа (длительном неконтролируемом лечении препаратами железа, при повторных частых переливаниях крови и т. д.).
Симптомы, течение. Характерны гиперпигментация кожи (особенно открытых частей тела, подмышечных впадин, ладоней, половых органов и старых кожных рубцов), принимающей серо-бурый или коричневатый цвет, увеличенная и плотная печень и сахарный диабет (чаще – инсулинозависимый). Нередки явления гипофизарной недостаточности с утратой либидо и атрофией половых желез. Гемосидероз миокарда проявляется кардиомегалией, нарушениями сердечного ритма и проводимости, сердечной недостаточностью, изменениями на ЭКГ (низкий вольтаж, уплощение или инверсия зубца T).
Повышена концентрация сывороточного железа (до 50–70 мкмоль/л), насыщенность железом трансферрина достигает 90 % (в норме 30 %). Гиперферремия выявляется еще до того, как возникают гиперпигментация кожи и увеличение печени. Исследование окрашенных голубым нитропруссидом гистологических препаратов, приготовленных из биоптатов печени больного, позволяет обнаружить большое количество внутриклеточного железа. Отмечается повышенное выделение с мочой железа после инъекции дефероксамина. Биохимические сдвиги, характерные для цирроза печени, появляются в более позднем периоде заболевания по сравнению с гиперпигментацией и увеличением печени. Как правило, выявляется гипергликемия и глюкозурия.
Течение постепенно прогрессирующее.
Прогноз без лечения неблагоприятный. Средняя продолжительность жизни больных после установления диагноза (при отсутствии лечения) не превышает 4–5 лет. Причиной гибели больных могут быть печеночная или диабетическая кома, острое кровотечение из варикозно-расширенных вен пищевода и желудка, сердечная недостаточность; у пожилых больных с длительным течением заболевания в 15–20 % случаев развивается рак печени.
Лечение. Назначают систематические кровопускания (приблизительно раз в неделю по 400–500 мл крови), повторные курсы инъекций дефероксамина (по 10 мл 10 % раствора в/м или в/в). При развитии диабета, появлении признаков поражения печени, сердца проводится соответствующая терапия.
ГЕПАТИТ – группа острых и хронических воспалительных заболеваний печени, характеризующихся некрозом ее клеток.
Гепатит острый. Этиология. Различают гепатиты инфекционные, токсические, лекарственные и др. Возможные возбудители инфекционного гепатита – вирусы гепатита, а также цитомегаловирус, вирусы инфекционного мононуклеоза (Эпштейна – Барр), желтой лихорадки, краснухи, кори, простого герпеса, Коксаки, эховирусы, лептоспиры, микоплазмы, риккетсии. Токсические гепатиты вызываются алкоголем и некоторыми другими химическими веществами (например, четыреххлористым углеродом), токсинами бледной поганки, сморчков (мускарин, афалотоксин и др.). Лекарственный гепатит вызывают изониазид, метилдофа, ингибиторы МАО, индометацин и другие лекарственные средства.
Патогенез острого гепатита заключается либо в непосредственном действии повреждающего фактора на печеночную паренхиму, либо в иммунологических нарушениях, возникающих в ответ на первичное поражение печени, с последующим цитолизом пораженных и интактных гепатоцитов. В некоторых случаях дополнительное значение имеют нарушение микроциркуляции в печени и внутрипеченочный холестаз.
Симптомы, течение. В легких случаях острый гепатит протекает практически бессимптомно, выявляясь лишь при случайном либо целенаправленном обследовании (например, на производстве среди лиц, контактирующих с гепатотропными ядами). В более тяжелых случаях клинические симптомы заболевания развиваются быстро, часто в сочетании с признаками общей интоксикации и токсического поражения других органов и систем. В разгар болезни характерны желтушное окрашивание кожи и слизистых оболочек, беловато-глинистого цвета стул, насыщенно-темного цвета («цвета пива») моча, геморрагические явления. Цвет кожных покровов бывает оранжевым или шафранным. Однако в легких случаях желтуха видна только при дневном освещении, наиболее рано появляется желтушное окрашивание склер и слизистой оболочки мягкого неба. Нередки носовые кровотечения, петехии; больных беспокоит кожный зуд, отмечаются брадикардия, угнетенное психическое состояние, повышенная раздражительность больных, бессонница и другие признаки поражения центральной нервной системы. Печень и селезенка несколько увеличены и слабо болезненны. При особо тяжелых поражениях и преобладании некротических изменений в печени (острой дистрофии) ее размеры могут уменьшаться.
Лабораторные исследования обнаруживают гипербилирубинемию (100–300 мкмоль/л и более); повышение активности ряда сывороточных ферментов – альдолазы, аспартатаминотрансферазы и особенно аланин-аминотрансферазы (значительно выше 40 ед.), лактатдегидрогеназы; гипоальбуминемию, гиперглобулинемию (преимущественно повышается содержание ?2– и реже гамма-глобулинов). Отклонены от нормы показатели белковоосадочных проб (тимоловая, сулемовая и др.). Нарушена выработка печенью фибриногена, протромбина, VII, V факторов свертывания, вследствие чего возникают геморрагические явления.
Течение, осложнение, прогноз. При своевременном лечении часто наступает полное выздоровление. В части случаев острый гепатит переходит в хронический, а затем в цирроз печени. В отдельных случаях развивается острая дистрофия печени с клиникой острой печеночной или печеночнопочечной недостаточности, от которой больные могут погибнуть.
Дифференциальный диагноз. Большое значение имеет тщательно собранный анамнез, установление возможности профессиональных или бытовых интоксикаций, учет эпидемиологической обстановки в выявлении характера и причины заболевания. В неясных случаях прежде всего следует подумать о вирусном гепатите. Механическая (подпеченочная) желтуха возникает остро обычно лишь при закупорке общего желчного протока камнем при желчнокаменной болезни. Но в этом случае появлению желтухи предшествует приступ желчной колики; билирубин в крови в основном прямой, стул – обесцвеченный. При гемолитической надпеченочной желтухе в крови определяется свободный (непрямой) билирубин, стул интенсивно окрашен, осмотическая резистентность эритроцитов обычно снижена. В случае ложной желтухи (например, вследствие окрашивания кожи каротином при длительном и обильном употреблении в пищу апельсинов, моркови, тыквы) склеры обычно не окрашены, гипербилирубинемия отсутствует.
Лечение. Больных острым вирусным гепатитом (и при подозрении на него), а также инфекционными гепатитами другой этиологии обязательно госпитализируют в специальные отделения инфекционных больниц, а в очаге инфекции проводят санитарно-противоэпидемические мероприятия. Больных токсическими гепатитами госпитализируют в центры отравлений, где проводят мероприятия по удалению яда из организма (промывания желудка и т. д.), дезинтоксикационную терапию.
Назначают постельный режим, щадящую диету с ограничением жиров и увеличением содержания углеводов, большое количество фруктовых соков. В тяжелых случаях, особенно при выраженной анорексии и рвоте, в/в капельно вводят 5-10 %-ный раствор глюкозы (до 500 мл).
При появлении признаков загруженности или комы по показаниям проводят плазмаферез; если нет стойкого улучшения (прояснения сознания, нарастания уровня протромбина), на следующий день и далее процедуру повторяют.
Прогноз зависит от этиологии заболевания, тяжести поражения печени, своевременности лечебных мероприятий.
Профилактика острых гепатитов, учитывая многообразие их этиологических факторов, заключается в четком проведении санитарно-противоэпидемических мероприятий, соблюдении правил личной гигиены, обеспечении соответствующего санитарно-технического надзора на предприятиях, предотвращающего возможность производственных отравлений гепатотропными ядами. Не следует употреблять в пищу заведомо несъедобные или неизвестные, а также съедобные, но старые грибы.
Хронический гепатит – группа воспалительных заболеваний печени, характеризующихся различной степенью гепатоцеллюлярного некроза и воспаления длительностью течения более 6 мес. Среди хронических заболеваний печени хронический гепатит является наиболее частым.
Этиология, патогенез. Различают хронические вирусный, аутоиммунный и лекарственный гепатиты. Наиболее частой причиной хронических гепатитов являются вирусы гепатита В, С, D (развивается на фоне гепатита В) и G (открыт в 1995 г.). Вирус гепатита В не оказывает прямого цитопатогенного эффекта. В результате репликации вируса на поверхности инфицированных гепатоцитов появляются антигены, развивается иммунный ответ с повреждением паренхимы печени лимфоцитами. Репликация вируса происходит не только в печени, но и вне ее – в мононуклеарных клетках крови, костного мозга, лимфатических узлов, селезенки, половых, щитовидной, слюнной железах: эти органы также становятся мишенями иммунологической реакции. Вирусы гепатита С и D оказывают на гепатоциты прямой цитопатогенный эффект (см. также Вирусные гепатиты в главе «Инфекционные болезни»).
Этиология аутоиммунного гепатита неизвестна. В основе его патогенеза может лежать продуцирование аутоантител против поверхностных антигенов гепатоцитов либо наличие аутоантигенов на поверхности гепатоцитов, что так или иначе приводит к разрушению клеток печени собственными лейкоцитами.
Лекарственный гепатит может быть обусловлен прямым токсическим действием лекарственных средств (тетрациклина, парацетамола и др.) либо развитием идиосинкразии к ним (возможна при использовании изониазида, вальпроата натрия, индометацина и др.).
Клиническая картина хронического гепатита наблюдается также при некоторых наследственных заболеваниях (при недостаточности ?1-антитрипсина и гепатолентикулярной дегенерации – наследственный гепатит), гемохроматозе, злоупотреблении алкоголем (алкогольный гепатит); возможно также сочетание причинных факторов (смешанный гепатит).
Помимо хронических гепатитов, представляющих собой самостоятельное заболевание, встречаются также хронические неспецифического характера гепатиты, возникающие на фоне различных хронических заболеваний пищеварительного тракта (язвенная болезнь, рак желудка), системных заболеваний соединительной ткани (системная красная волчанка, ревматизм, ревматоидный артрит, склеродермия, дерматомиозит и др.), эндокринных заболеваний (тиреотоксикоз, сахарный диабет) и т. д. (вторичные, или реактивные, гепатиты). Наконец, во многих случаях этиология хронического гепатита остается невыясненной (так называемый криптогенный гепатит).
Симптомы, течение. Часты снижение аппетита, отрыжка, тошнота, рвота, плохая переносимость жиров, алкоголя, метеоризм, неустойчивый стул, общая слабость, снижение трудоспособности, гипергидроз. Характерны боль или чувство тяжести, полноты в правом подреберье, диспепсические явления, увеличение печени; реже выявляются желтуха, потемнение мочи, осветление кала, кожный зуд, субфебрилитет. Увеличение печени встречается у подавляющего большинства больных, однако чаще всего оно умеренное. Увеличение селезенки отсутствует или она увеличена незначительно. Боль в области печени тупого характера, постоянная. У трети больных выявляется нерезко выраженная (субиктеричность склер и неба) или умеренная желтуха. При хроническом гепатите В и аутоиммунном гепатите могут преобладать внепеченочные проявления – кожные высыпания, артралгии, полиневропатия, гломерулонефрит и др.
Часты, но неспецифичны увеличение СОЭ, диспротеинемия за счет снижения концентрации альбуминов и повышения глобулинов, преимущественно гамма-фракции. Положительны результаты белково-осадочных проб – тимоловой, сулемовой и др. Приблизительно у половины больных находят незначительную или умеренную гипербилирубинемию преимущественно за счет повышения содержания в сыворотке крови связанного (прямого) билирубина. В сыворотке крови больных увеличено содержание аминотрансфераз: АлAT, AcAT и ЛДГ, при затруднении оттока желчи – щелочной фосфатазы. Уровень повышения трансаминаз может использоваться для клинической оценки тяжести течения гепатита, хотя и не всегда отражает истинную тяжесть поражения печени. При легком течении гепатита отмечается повышение уровня трансаминаз на три нормальных значения от верхней границы, при среднем – на 3-10 норм, при тяжелом – более чем на 10 норм. Состояние печени помогают оценить ультразвуковое исследование, радионуклидное сканирование (уточняются размеры печени; при гепатитах иногда отмечается уменьшенное или неравномерное накопление радиофармацевтического препарата в ткани печени, иногда с повышенным его накоплением в селезенке). Пункционная биопсия печени позволяет не только подтвердить диагноз, но и оценить активность процесса (с учетом наличия перипортальных некрозов, внутридольковых фокальных некрозов и дистрофии гепатоцитов, портального воспаления), а также стадию процесса (степень фиброза, наличие цирроза печени).
При хроническом вирусном гепатите В в крови в большинстве случаев выявляется HbsAg; о репликации вируса свидетельствуют HbeAg, анти-НВс IgM, ДНК HBV. При гепатитах С и D выявляют РНК соответствующего вируса и антитела к нему.
Диагноз аутоиммунного гепатита основывается на характерных клинических и биохимических признаках (особенно характерна гипергаммаглобулинемия), гистологических данных (наличие ступенчатых некрозов), наличии высоких титров характерных аутоантител – к гладкой мускулатуре (SMA), антинуклеарных (ANA), к печеночно-почечным микросомам I типа (анти-LKM-I). Диагноз аутоиммунного гепатита требует исключения хронического гепатита вирусной или другой известной этиологии; важным диагностическим критерием является быстрый эффект глюкокортикоидной терапии. В отличие от других форм, аутоиммунный гепатит не требует 6 мес наблюдения для подтверждения диагноза; при наличии соответствующих признаков его можно диагностировать на любой стадии клинического течения.
Дифференциальный диагноз в случаях с яркой клинической картиной диффузного поражения печени в первую очередь нужно проводить с циррозом печени. При циррозе более выражены симптомы заболевания, печень обычно значительно плотнее, чем при гепатите; она может быть увеличенной, но нередко и уменьшенной в размерах (атрофическая фаза цирроза). Как правило, наблюдается спленомегалия, часто выявляются печеночные «знаки» (телеангиэктазии, печеночный язык, печеночные ладони), могут иметь место симптомы портальной гипертензии. Лабораторные исследования показывают значительные отклонения от нормы результатов так называемых печеночных проб; при пункционной биопсии – дезорганизация структуры печени, значительное разрастание соединительной ткани. При жировом гепатозе печень обычно более мягкая, чем при хроническом гепатите, селезенка не увеличена, решающее значение в диагностике имеет пункционная биопсия печени.
Дифференциальный диагноз с функциональными гипербилирубинемиями основывается на особенностях их клинической картины (легкая желтуха с гипербилирубинемией без яркой клинической симптоматики и изменения данных лабораторных печеночных проб и пункционной биопсии печени). Амилоидозу с преимущественной печеночной локализацией в отличие от хронического гепатита свойственны симптомы и других органных локализаций процесса, положительная проба с конго красным или метиленовым синим; диагноз подтверждается пункционной биопсией печени. При очаговых поражениях (опухоль, киста, туберкулема и др.) печень неравномерно увеличена, а сканирование определяет очаг деструкции печеночной паренхимы.
Течение. Традиционно выделяют персистирующий и активный гепатит. Персистирующий гепатит протекает бессимптомно или с незначительными симптомами. Характерно постоянное повышение уровня трансаминаз, изменения других лабораторных показателей незначительны. Обострения процесса нехарактерны.
Хронический активный (агрессивный) гепатит характеризуется выраженными жалобами и яркими объективными клиническими и лабораторными признаками. У некоторых больных наблюдаются системные ау то аллергические проявления заболевания (полиартралгия, кожные высыпания, гломерулонефрит и т. д.). Характерны частые рецидивы болезни, иногда наступающие под воздействием даже незначительных факторов (погрешность в диете, переутомление и т. д.). Частые рецидивы приводят к значительным морфологическим изменениям печени и развитию цирроза. В связи с этим прогноз при активном гепатите более тяжелый.
Лечение. Больные хроническим гепатитом вне обострения должны соблюдать диету с исключением острых, пряных блюд, тугоплавких животных жиров, жареной пищи. Рекомендуются творог (ежедневно до 100–150 г), неострые сорта сыра, нежирные сорта рыбы в отварном виде (треска и др.). При обострении гепатита показана госпитализация, постельный режим, более строгая щадящая диета с достаточным количеством белков и витаминов.
Единственным препаратом с доказанной эффективностью при лечении хронических вирусных гепатитов является альфа-интерферон. При хроническом гепатите В терапия интерфероном показана при обнаружении маркеров репликации вируса (HbeAg, анти-Hbc IgM, ДНК HBV) и повышении уровня трансаминаз более чем в 2 раза. Альфа-интерферон (интрон-А, веллферон, роферон и др.) вводят внутримышечно по 5 000 000 ЕД 3 раза в неделю в течение 6 мес или по 10 000 000 ME 3 раза в неделю в течение 3 мес. При хроническом гепатите С интерферонотерапия показана при обнаружении в сыворотке крови анти-HCV, РНК HCV и повышении уровня трансаминаз более чем в 2 раза. Альфа-интерферон вводят в/м в дозе 3 000 000 ME 3 раза в неделю на протяжении 2 мес; при снижении уровня трансаминаз терапию продолжают еще в течение 6 мес, при отсутствии положительной динамики лечение интерфероном прекращают. При хроническом гепатите D (при наличии в сыворотке крови HbsAg и (или) анти-Hbs и РНК HDV) альфа-интерферон вводят в/м по 5 000 000-10 000 000 ME в течение 12 мес.
Критериями эффективности лечения интерфероном являются исчезновение маркеров репликации вируса и нормализация уровня трансаминаз. Возможные побочные эффекты интерферонотерапии: гриппоподобный синдром (лихорадка, миалгии, артралгии, головная боль через 3–5 ч после введения препарата), тромбоцитопения, лейкопения, редко – анорексия, снижение массы тела, депрессия. Противопоказания к терапии интерфероном – декомпенсированный цирроз печени, тяжелые соматические заболевания, тромбоцитопения (менее 100 000/мкл), лейкопения (менее 3000/мкл), продолжение употребления наркотиков или алкоголя, наличие в анамнезе психических заболеваний (особенно депрессии).
Дезинтоксикационная терапия при хронических вирусных гепатитах включает внутривенное капельное введение гемодеза (200–400 мл в течение 3 дней), прием внутрь лактулозы (30–40 мл в сутки в течение месяца).
При лечении аутоиммунного гепатита патогенетическая иммуносупрессивная терапия проводится глюкокортикоидами. Обычно применяют преднизолон в дозе 30 мг в сутки в течение 1 мес, далее ежемесячно дозу снижают на 5 мг до уровня поддерживающей (10 мг в сутки), которую пациент принимает в течение нескольких лет. При недостаточной эффективности глюкокортикоидов, рецидивировании активности гепатита на фоне снижения дозы преднизолона, при развитии побочных эффектов глюкокортикоидов к терапии добавляют азатиоприн в начальной дозе 50 мг в сутки, поддерживающая доза – 25 мг в сутки. Через 2–4 года при стойкой ремиссии (исчезновении клинических и биохимических признаков заболевания) возможна полная отмена препаратов.
Симптоматическая терапия аутоиммунного гепатита включает применение полиферментных препаратов (креон, панцитрат и др.).
При алкогольном поражении печени ключевую роль в терапии играет полный отказ пациента от приема алкоголя. Для нормализации липидного обмена в печени при отсутствии признаков холестаза применяют эссенциале (4–6 капсул в сутки в течение 6–8 нед). При наличии признаков внутрипеченочного холестаза используют адеметионин (гептрал – по 800 мг в сутки в/в в течение 16 дней с последующим переходом на прием препарат внутрь в дозе 1600 мг в сутки). Препарат обладает также антидепрессивным действием.
При лекарственных гепатитах необходима отмена препарата, вызвавшего повреждение печени. В качестве вспомогательного средства используют гепатопротекторы (легалон 210–420 мг в сутки в течение 3–6 нед).
Профилактика хронических гепатитов сводится к профилактике вирусных гепатитов, борьбе с алкоголизмом, исключению возможности производственных и бытовых интоксикаций гепатотропными веществами, а также к своевременному выявлению и лечению острого и подострого гепатита. Больные хроническим гепатитом нуждаются в трудоустройстве (ограничение тяжелой физической нагрузки, освобождение от работ, связанных с частыми командировками и не позволяющих соблюдать режим питания). Больные подлежат диспансерному наблюдению, 2 раза в год проводится активное наблюдение с оценкой жалоб, объективного статуса, уровня трансаминаз, при необходимости проводится более полное обследование.
ГЕПАТОЗЫ – болезни печени, характеризующиеся дистрофическими изменениями ее паренхимы без выраженной мезенхимально-клеточной реакции. В зависимости от природы нарушения обмена веществ различают жировой и пигментные (см. Гипербилирубинемии врожденные) гепатозы.
Жировой гепатоз (жировая дистрофия, жировая инфильтрация, стеатоз печени) характеризуется жировой (иногда с элементами белковой) дистрофией гепатоцитов и хроническим течением.
Этиология, патогенез. Основные причины развития жирового гепатоза – алкоголизм, реже ожирение, сахарный диабет, другие эндокринные расстройства (синдром Кушинга, микседема, тиреотоксикоз, акромегалия), дефицит белка и витаминов, заболевания органов пищеварения, сопровождающиеся нарушениями всасывания (хронический панкреатит, язвенный колит и др.), хронические интоксикации четыреххлористым углеродом, фосфорорганическими соединениями, другими токсическими веществами, обладающими гепатотропным действием, бактериальными токсинами и др. Патогенез поражения печени в этих случаях в основном сводится к нарушению метаболизма липидов в гепатоцитах и образования липопротеидов.
Симптомы, течение. Возможна малосимптомная форма, при которой клиника маскируется проявлениями основного заболевания (тиреотоксикоз, сахарный диабет и др.), токсического поражения других органов или сопутствующих заболеваний желудочно-кишечного тракта. В других случаях наблюдаются выраженные диспепсические явления, общая слабость, тупая боль в правом подреберье; иногда – легкая желтуха. Печень умеренно увеличена, с гладкой поверхностью, болезненная при пальпации. Спленомегалия не характерна. Содержание аминотрансфераз в сыворотке крови умеренно или незначительно повышено, нередко также повышено содержание холестерина, (3-липопротеинов. Характерны результаты бромсульфалеиновой пробы: задержка выделения печенью этого препарата наблюдается в большинстве случаев. Другие лабораторные тесты малохарактерны. Решающее значение в диагностике имеют данные пункционной биопсии печени (жировая дистрофия гепатоцитов).
Течение относительно благоприятное: во многих случаях, особенно при исключении действия повреждающего агента и своевременном лечении, возможно выздоровление. Однако гепатоз в отдельных случаях может трансформироваться в хронический гепатит и цирроз.
Дифференциальный диагноз. Отсутствие спленомегалии позволяет с известной степенью уверенности дифференцировать хронические гепатозы с гепатитами и циррозами печени. При циррозах печени обычно имеются печеночные «знаки» (печеночные звездочки – телеангиэктазии, ярко-красного или малинового цвета язык, печеночные ладони и т. д.), признаки портальной гипертензии, чего не бывает при гепатозах. Следует иметь в виду также гепатолентикулярную дегенерацию, гемохроматоз. Очень большое значение для дифференциальной диагностики гепатоза с другими поражениями печени имеет чрескожная биопсия печени.
Лечение. Необходимо стремиться к прекращению действия этиологического фактора. Категорически запрещают прием алкогольных напитков. Назначают диету № 5 с повышенным содержанием полноценных белков животного происхождения (до 100–120 г/сут) и липотропных факторов (творог, отварная треска, дрожжи, изделия из гречневой, овсяной крупы и т. д.). Ограничивают поступление в организм жиров, особенно тугоплавких, животного происхождения. Назначают липотропные препараты: липоевую, фолиевую кислоту, витамин B12, препараты, содержащие экстракты и гидролизаты печени (сирепар по 5 мл в/м ежедневно, эссенциале и др.), легалон, при выраженных нарушениях жирового обмена (гиперхолестеринемии, гипертриглицеридемии, гиперлипопротеинемии) используют липофарм, липостабил.
ГЕПАТОЛЕНТИКУЛЯРНАЯ ДЕГЕНЕРАЦИЯ (гепатоцеребральная дистрофия, болезнь Вестфаля – Вильсона – Коновалова) – характеризуется нарушением обмена меди, поражением печени типа цирроза и деструктивными процессами в головном мозге. Встречается чаще всего в юношеском возрасте, относится к генетически обусловленным ферментопатиям, передается по аутосомно-рецессивному типу. В сыворотке крови больных снижено содержание церулоплазмина, связывающего медь (менее 0,2 г/л); значительно усилена абсорбция меди в кишечнике. Вследствие этого происходит повышенное отложение меди в печени (что ведет к развитию цирроза), ганглиях нервной системы (вызывая их токсическое поражение), в коже, по периферии роговицы глаза и в других тканях. В 5-10 раз усиливается выделение меди с мочой.
Симптомы, течение. Нередко заболевание начинается с признаков поражения печени (желтухи, рвоты, диспепсии) и диагностируется как хронический гепатит, цирроз печени, затем присоединяются неврологические расстройства: тремор конечностей, скандированная речь, амимия, далее развиваются гипертонус мышц конечностей, нарушения мышления. В других случаях поражение нервной системы развивается раньше, а затем у больных выявляется цирроз печени, обычно крупноузловой, по своим клиническим проявлениям в основном не отличающийся от циррозов другой этиологии. Отложение меди в почках ведет к гипераминоацидурии, а в ряде случаев – почечной глюкозурии. Диагностическое значение имеет гиперпигментация кожи – от темно-серого до коричневого цвета и наличие на периферии роговиц больного характерного зеленовато-коричневого ободка – так называемых колец Кайзера – Флейшера. Как правило, обнаруживается умеренная спленометалия. Диагноз подтверждается пункционной биопсией печени и лабораторными тестами: исследованием содержания церулоплазмина в сыворотке крови, концентрации меди в крови и суточной моче. В нелеченых случаях болезнь прогрессирует и через несколько лет после проявления явных симптомов заканчивается гибелью больных.
Лечение. Рекомендуется специальная диета с низким содержанием меди. Выделение меди с мочой увеличивает D-пеницилламин (купренил), назначаемый пожизненно (300-1000 мг в сутки).
ГЕПАТОЛИЕНАЛЬНЫЙ СИНДРОМ – сочетанное увеличение печени и селезенки. Наблюдается при заболеваниях печени (например, циррозах), при расстройствах кровообращения в системах воротной и селезеночной вен (например, тромбозах), болезнях накопления (гемохроматозе, гепатолентикулярной дегенерации и др.), инфекционных и паразитарных заболеваниях и др.
Симптомы, течение. Отмечается одновременное увеличение печени и селезенки, при значительной давности процесса – уплотнение их. Могут наблюдаться гиперглобулинемия, повышение СОЭ, изменение белково-осадочных проб. Гематологической особенностью гепатолиенального синдрома являются симптомы гиперспленизма – анемия, лейкопения и тромбоцитопения.
Лечение. Проводят лечение основного заболевания. При резко выраженном гиперспленизме – спленэктомия.
ГИПЕРБИЛИРУБИНЕМИИ ВРОЖДЕННЫЕ (ПИГМЕНТНЫЕ ГЕПАТОЗЫ) – группа наследственных энзимопатий, характеризующихся нарушением обмена билирубина и проявляющихся стойкой или перемежающейся желтухой при отсутствии выраженных изменений структуры и функции печени, явных признаков гемолиза и холестаза. Заболевания обусловлены нарушением процессов захватывания гепатоцитами свободного билирубина из крови, связывания его с глюкуроновой кислотой с образованием билирубин-глюкуронида (связанного билирубина) и последующего выделения его с желчью.
Во всех случаях гипербилирубинемия и желтуха обнаруживаются с раннего детства, в большинстве случаев (кроме синдрома Криглера – Найяра) – незначительны, могут иметь перемежающийся характер (усиливаться под влиянием погрешностей в диете, приема алкоголя, интеркуррентных заболеваний, физического переутомления и других причин). Нередки нерезко выраженные диспептические явления, легкая астенизация, слабость, быстрая утомляемость. Печень обычно не увеличена, мягка, безболезненна, функциональные пробы печени (за исключением гипербилирубинемии) не изменены. Радионуклидная гепатография изменений не выявляет. Селезенка не увеличена. Осмотическая резистентность эритроцитов, продолжительность их жизни – нормальны. Пункционная биопсия при всех формах (кроме синдрома Дубина – Джонсона) изменений не выявляет.
Синдром Жильбера (ювенильная интермиттирующая желтуха, синдром Мейленграхта) развивается вследствие снижения способности клеток печени захватывать и связывать билирубин. Характеризуется умеренным интермиттирующим повышением содержания несвязанного (непрямого) билирубина в крови, отсутствием других функциональных или морфологических изменений печени и аутосомно-доминантным типом наследования. Основное проявление болезни – желтушность склер, реже кожных покровов, появляющаяся в возрасте 20 лет и старше.
Синдром Криглера – Найяра I типа характеризуется крайне высоким содержанием в крови свободного (непрямого) билирубина из-за отсутствия в гепатоцитах глюкуронилтрансферазы, переводящей свободный билирубин в связанный, токсическим действием билирубина на базальные и стволовые ядра головного мозга с возникающей вследствие этого энцефалопатией, нередко приводящей больных к смерти в детском возрасте, и аутосомно-рецессивным типом наследования. Неврологические проявления включают повышение мышечного тонуса, нистагм, опистотонус, атетоз, тонические и клонические судороги; характерно отставание детей в психическом и умственном развитии. Синдром Криглера – Найяра II типа обусловлен частичным дефицитом того же фермента, желтуха менее интенсивна, неврологические нарушения не выражены, тип наследования аутосомнодоминантный.
Синдром Дубина – Джонсона (хроническая идиопатическая желтуха) характеризуется умеренным повышением содержания в крови связанного (прямого) билирубина вследствие нарушения механизмов его транспорта из микросом гепатоцитов в желчь, извращенными результатами теста на задержку бромсульфалеина со вторичным повышением его содержания в крови через 90 мин после в/в введения, неконтрастированием желчного пузыря при пероральной холецистографии, черным цветом печени из-за скопления в гепатоцитах коричневого липохромного пигмента, повышенным выделением с мочой копропорфирина и аутосомно-рецессивным типом наследования.
Ротора синдром (гипербилирубинемия идиопатическая типа Ротора) характеризуется умеренным повышением содержания в крови связанного билирубина, задержкой выделения печенью введенного в/в бромсульфалеина, повышенным выделением почками копропорфирина, отсутствием других функциональных и морфологических изменений печени, аутосомнорецессивным типом наследования.
Течение при всех формах (кроме синдрома Криглера – Найяра) доброкачественное, прогноз благоприятный; трудоспособность, как правило, сохранена. При синдроме Криглера – Найяра I типа больные обычно погибают в раннем детском возрасте, при II типе пациенты обычно доживают до зрелого возраста.
Лечение. Больные в специальном лечении, как правило, не нуждаются, лишь в период усиления желтухи назначают щадящую диету № 5. Запрещается употреблять алкогольные напитки, острую и жирную пищу, не рекомендуются физические перегрузки. При обострении синдромов Жильбера и Криглера – Найяра II типа показана терапия препаратами, способствующими индукции ферментов, осуществляющих связывание билирубина: фенобарбиталом (30-180 мг в сутки в течение 2–4 нед), зиксорином (по 0,2 г 2–3 раза в сутки в течение 2–4 нед). При синдроме Криглера – Найяра I типа терапия фенобарбиталом неэффективна (индукция фермента невозможна в связи с его отсутствием).
ГИПОВИТАМИНОЗЫ – см. Болезни витаминной недостаточности.
ДИАБЕТ БРОНЗОВЫЙ – см. Гемохроматоз.
ДИАРЕЯ (понос) – учащенное или однократное опорожнение кишечника с выделением жидких испражнений (обычно более 200–300 г за сутки).
Этиология, патогенез. В основе диареи может лежать увеличение активной секреции кишечником натрия и воды, повышение осмотического давления в полости кишки (снижение всасывания воды и элетролитов), нарушения перистальтики кишечника, повышение экссудации воды и электролитов в просвет кишечника. Избыточная секреция в тонкой кишке развивается при обсеменении ее патогенными микроорганизмами (например, холерным вибрионом, энтеропатогенными вирусами), при опухолях, выделяющих пептидные гормоны, синдроме Золлингера – Эллисона (вследствие повышенной продукции гастрина). Избыточная секреция в толстой кишке возможна при нарушении всасывания в тонком кишечнике жирных кислот с длинными цепями, желчных кислот (например, при дисбактериозе). Гиперосмолярная диарея развивается при мальабсорбции (например, целиакии), дефиците панкреатических ферментов (при хроническом панкреатите, раке поджелудочной железы) и желчных солей (при механической желтухе), под действием осмотических слабительных (сульфата магния, лактулозы). Нарушения перистальтики кишечника возможны при синдроме раздраженной толстой кишки, под влиянием некоторых слабительных средств (экстракт сенны, бисакодил, касторовое масло). Повышение экссудации воды и электролитов сопутствует экссудации белка в просвет кишки через поврежденную слизистую оболочку – при болезни Крона, язвенном колите, туберкулезе кишечника, кишечных инфекциях (дизентерия, сальмонеллез), при злокачественных опухолях и ишемических заболеваниях кишечника.
Симптомы, течение. Частота стула бывает различной, испражнения – водянистыми или кашицеобразными. При гиперсекреторной диарее стул обильный, водянистый, при гиперосмолярной – преобладает полифекалия (увеличение количества испражнений за счет непереваренных остатков), при моторной диарее наблюдается необильный частый жидкий стул, при гиперэкссудативной стул жидкий, иногда с примесью гноя и крови.
Характер испражнений зависит от заболевания. Так, наличие свежей или измененной крови в кале указывает на патологию толстой кишки, появление гноя и слизи – на воспалительный процесс. В частности, при дизентерии кал имеет сначала плотную консистенцию, потом становится жидким, скудным, в нем появляются слизь и кровь; при амебиазе – содержит стекловидную слизь и кровь, иногда кровь пропитывает слизь и испражнения приобретают вид малинового желе. При заболеваниях поджелудочной железы отмечается «жирный» кал (после смывания испражнений на унитазе остаются капли жира).
Различают диарею острую (продолжительностью менее 2–3 нед) и хроническую (продолжительностью более 3 нед). Причинами острой диареи чаще всего являются инфекционные (дизентерия, сальмонеллез и др.) и другие воспалительные заболевания кишечника (язвенный колит, болезнь Крона), прием лекарственных средств (слабительных, антибиотиков, содержащих соли магния антацидов и др.). Для острой инфекционной диареи характерны признаки интоксикации, лихорадка, анорексия, иногда – рвота. Причиной диареи, продолжающейся после перенесенного острого гастроэнтерита, могут быть персистирующая инфекция (лямблиоз, иерсениоз), приобретенная лактазная недостаточность, синдром раздраженной толстой кишки, а также нераспознанная ранее болезнь (например, целиакия, язвенный колит). Хроническая диарея может быть проявлением функциональных расстройств или органического заболевания кишечника, включая синдром раздраженной толстой кишки, опухоли кишечника, язвенный колит, болезнь Крона, синдром мальабсорбции и др.
Боль в гипогастрии может сопровождать понос при заболеваниях толстой кишки (дивертикулезе, болезни Крона, синдроме раздраженной толстой кишки, опухолях кишечника), в верхней половине живота – при панкреатате, синдроме Золлингера – Эллисона. Язвенный колит и дисбактериоз часто проявляются диареей без болевого синдрома.
Зловонный запах испражнений, наличие в них непереваренных остатков, ощущение урчания, переливания, вздутие живота – неспецифические признаки, встречающиеся при многих заболеваниях.
Легкие и недлительные поносы мало отражаются на общем состоянии больных, тяжелые и хронические приводят к дегидратации, потере электролитов (калия, натрия, магния), истощению, гиповитаминозам, выраженным изменениям в органах.
Для установления причины диареи проводят копрологическое и бактериологическое исследования. При подозрении на холеру, сальмонеллез, пищевую токсикоинфекцию больные подлежат немедленной госпитализации в инфекционное отделение.
Лечение направлено, в первую очередь, на устранение причины, вызвавшей диарею. Например, при недостаточности поджелудочной железы показаны ферментативные препараты – креон, фестал, мезим форте и др. Показана механически и химически щадящая диета с исключением продуктов, усиливающих моторно-эвакуаторную и секреторную функцию.
В целях восстановления эубиоза используют антибактериальные средства, предпочтение отдается препаратам, не нарушающим равновесие микробной флоры в кишечнике, – интетриксу, нифуроксазиду (эрсефурилу) и др. Используют бактериальные препараты – бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол, флонивин БС и др., а также хилак форте.
В качестве симптоматических средств используют карбонат кальция, препараты висмута, танальбин; отвары из коры дуба, травы зверобоя, корневища змеевика, лапчатки или кровохлебки, плодов черемухи, настой черники, соплодий ольхи, цветов ромашки, настойку красавки и др. Применяют адсорбирующие, вяжущие, обволакивающие средства (смекта, таннакомп и др.). Для замедления кишечной перистальтики используют спазмолитики (но-шпа, папаверин, бкускопан). Антидиарейным дествием обладает лоперамид (имодиум), снижающий тонус и моторику кишечника за счет влияния на опиатные рецепторы. Препарат используется при остром гастроэнтерите, моторных расстройствах, назначается в дозе 4 мг внутрь после первого жидкого стула, затем по 2 мг после каждой дефекации. При развитии дегидратации проводится инфузионная терапия либо регидрационные растворы (цитроглюкосолан, регидрон, гастролит) назначаются для приема внутрь.
ДИСБАКТЕРИОЗ КИШЕЧНЫЙ – синдром, характеризующийся избыточным микробным обсеменением тонкой кишки и изменением микробного состава толстой кишки. Если у здоровых людей в дистальных отделах тонкой кишки и в толстой кишке преобладают лактобактерии, анаэробные стрептококки, кишечная палочка, энтерококки и другие микроорганизмы, то при дисбактериозе равновесие между этими микроорганизмами нарушается, обильно развивается гнилостная или бродильная флора, грибы, преимущественно типа Candida, в кишечнике обнаруживаются микроорганизмы, в норме нехарактерные для него, большое количество микробов находится в содержимом проксимальных отделов тонкой кишки и в желудке. Активно развиваются условно-патогенные микроорганизмы, обычно обнаруживаемые в содержимом кишечника в небольших количествах, вместо непатогенных штаммов кишечной палочки (эшерихии) нередко обнаруживаются ее более патогенные штаммы. Таким образом, при дисбактериозе наблюдаются качественные и количественные изменения состава микробных ассоциаций в желудочно-кишечном тракте (меняется микробный пейзаж).
Этиология, патогенез. К кишечному дисбактериозу приводят заболевания желудка, протекающие с ахлоргидрией (хронический гастрит), кишечника (хронический энтерит, колит), поджелудочной железы, печени, почек, В12-дефицитная анемия, злокачественные новообразования, резекция желудка и двенадцатиперстной кишки, нарушения перистальтики. Причиной кишечного дисбактериоза может быть длительный, неконтролируемый прием антибиотиков, особенно широкого спектра действия, подавляющих нормальную кишечную флору и способствующих развитию тех микроорганизмов, которые имеют устойчивость к этим антибиотикам, а также применение цитостатиков, глюкокортикоидов, снижающих иммунорезистентность организма. Таким образом, дисбактериоз – проявление или одно из осложнений основного заболевания, но не самостоятельная нозологическая форма.
При дисбактериозе нарушается антагонистическая активность микрофлоры кишечника в отношении патогенных и гнилостных микроорганизмов. Продукты ненормального расщепления пищевых веществ необычной для кишечника микрофлорой (органические кислоты, альдегиды, индол, скатол, сероводород и др.), образующиеся в больших количествах, раздражают стенку кишки. Влияние микробных токсинов на структуру и активность мембранных ферментов обусловливает нарушение мембранного пищеварения в тонкой кишке, стимуляция ими секреции воды и электролитов энтероцитами – к секреторной диарее, преждевременная деконъюгация желчных кислот в кишечнике – к нарушению всасывания жиров, стеаторее.
Симптомы, течение. Характерны симптомы диспепсии, снижение аппетита, неприятный вкус во рту, тошнота, метеоризм, понос или запоры. Каловые массы имеют резкий гнилостный или кислый запах. Часто наблюдаются признаки общей интоксикации, наблюдается вялость, снижается трудоспособность.
Особенно тяжело протекает псевдомембранозный колит, развивающийся под влиянием токсинов синегнойной палочки (Clostridium dificile) у некоторых пациентов, длительно получавших антибиотики широкого спектра действия (ампициллин, клиндамицин, цефалоспорины и др.). Пседомембранозный колит характеризуется обильной водянистой диареей, быстро приводящей к обезвоживанию, схваткообразной болью в животе, болезненностью при пальпации нижних отделов живота, лихорадкой, лейкоцитозом. При эндоскопическом исследовании на слизистой оболочке ободочной кишки выявляют чешуйки желтого цвета (псевдомембраны), представляющие собой скопления фибрина, слизи и клеток, участвующих в воспалении.
Диагноз дисбактериоза подтверждается повторными исследованиями фекальной микрофлоры. При дисбактериозе обнаруживают снижение бифидо– и лактобактерий, снижение или увеличение эшерихий, появление штаммов с измененными свойствами, повышение количества кокков, обнаружение условно-патогенных палочек, большого количества грибов и клостридий. В копрограмме выявляют непереваренную клетчатку, крахмал, стеаторею. При биохимическом исследовании кала определяют щелочную фосфатазу, повышенный уровень энтерокиназы.
При длительном течении возможно развитие витаминной недостаточности (особенно дефицит витаминов группы В). Некоторые виды кишечного дисбактериоза (особенно стафилококковый, кандидамикозный, протейный, реже другие) могут переходить в генерализованную форму (сепсис).
Лечение в легких случаях амбулаторное, в более тяжелых – в стационарных условиях. Прекращают введение антибактериальных средств, которые могли повести к развитию дисбактериоза, назначают общеукрепляющую и десенсибилизирующую терапию (витамины, противогистаминные препараты и др.).
В целях устранения избыточного бактериального обсеменения кишки используют антибактериальные средства: при эшерихиозе – невиграмон, нитроксолин, котримаксазол (бисептол); при стафилококковом дисбактериозе – фуразалидон; при псевдомембранозном колите – метронидазол (внутрь или в/в по 500 мг 2 раза в сутки), котримаксазол (бисептол); при протейном дисбактериозе – фуразалидон, невиграмон, нитроксолин и др; при кандидамикозе – нистатин, леворин, при необходимости – кетоконазол, флюконазол. При дисбактериозе толстой кишки используют антисептики, оказывающие минимальное влияние на нормальную микрофлору, – интетрикс, нифуроксазид (эрсефурил) и др.
Для связывания токсинов при псевдомембранозном колите используют холестирамин. Применяют также энтеросорбенты на основе гранулированных активированных углей (карболен, карболонг и др.), смекту (улучшает свойства слизи желудочно-кишечного тракта, повышает резистентность слизистой оболочки, обладает цитопротективным действием).
Для нормализации кишечной флоры целесообразно применение бактериальных препаратов – бифидумбактерина, бификола, лактобактерина, бактисубтила, линекса, энтерола, флонивина БС и др. Эти препараты можно рекомендовать без предварительного курса антибактериальной терапии, если дисбактериоз проявляется только исчезновением или уменьшением числа представителей нормальной кишечной флоры. На патогенную флору воздействует также хилак форте, представляющий собой концентрат продуктов метаболизма нормальных микроорганизмов.
Если дисбактериозу сопутствует нарушение процессов пищеварения, целесообразно назначение препаратов пищеварительных ферментов (креон, фестал, мезим форте и т. д.). Для восстановления нарушенной моторики желудочно-кишечного тракта используют лоперамид (имодиум), дебридат. При нарушениях водно-электролитного балланса показана адекватная инфузионная терапия, при отсутствии тошноты и рвоты рекомендуют прием регидратационных растворов внутрь. При дисбактериозах, возникающих на фоне заболевания пищеварительного тракта (энтерит, колит и т. д.), необходимо рациональное его лечение.
Профилактика сводится к рациональному назначению антибиотиков, полноценному питанию и общеукрепляющей терапии лиц, переболевших тяжелыми заболеваниями органов пищеварения.
ДИСКИНЕЗИИ ЖЕЛЧНЫХ ПУТЕЙ – клинический синдром, характеризующийся несогласованным, чрезмерным или недостаточным сокращением желчного пузыря и сфинктера Одди. Наблюдается при органических заболеваниях желчевыделительной системы, поджелудочной железы, двенадцатиперстной кишки. В ряде случаев при обследовании не выявляют патологии органов пищеварения, тогда дискинезию рассматривают как самостоятельное заболевание неясной этиологии. При этом может определяться гипертония желчного пузыря или (и) пузырного протока, спазм сфинктера Одди или, наоборот, гипотония пузыря, недостаточность сфинктера Одди. Первичная дискинезия желчных путей чаще выявляется у женщин, лиц молодого возраста астенической конституции. Она нередко сочетается с другими нарушениями моторики желудочно-кишечного тракта – замедлением опорожнения желудка, синдромом раздраженной толстой кишки и др.
Симптомы, течение. Повышение тонуса желчного пузыря и спазм сфинктера Одди могут вызвать приступообразную боль в правом подреберье ноющего или схваткообразного характера, напоминающую приступ колики при желчнокаменной болезни. Возникновению приступов способствуют значительная нервно-психическая нагрузка, отрицательные эмоции, у женщин обострения могут быть связаны с менструальным циклом. Боль может иррадиировать в правую лопатку, правое плечо, иногда в область сердца, сопровождаться признаками вегетативной дистонии – резкой потливостью, бледностью, тошнотой, иногда головной болью, ощущением сердцебиения и т. д. Болевые приступы продолжаются от нескольких минут до нескольких дней; тупая давящая и ноющая боль в правом подреберье может сохраняться неделями, временами усиливаясь или затихая. В период болевого приступа живот не напряжен. Желтухи, лихорадочной реакции, лейкоцитоза и повышения СОЭ после приступа не наблюдается. Снижение тонуса желчного пузыря и недостаточность сфинктера Одди проявляются в основном малоинтенсивной болью в правом подреберье, часто длительной. При пальпации выявляется небольшая болезненность в области желчного пузыря.
Диагноз подтверждается данными многомоментного дуоденального зондирования, холесцинтиграфии, результатами оценки уровня базального давления сфинктера Одди при проведении эндоскопической манометрии. Ультразвуковое исследование органов брюшной полости, в диагностически сложных случаях – компьютерная томография подтверждают функциональный характер заболевания.
Течение обычно длительное с периодами обострений (в связи с эмоциональными стрессами, алиментарными нарушениями) и ремиссий. С течением времени, однако, возможно образование желчных камней или развитие воспалительного процесса в желчном пузыре и протоках.
Лечение. Регуляция режима питания, правильное чередование труда и отдыха, нормализация сна и других функций ЦНС (седативные препараты, транквилизаторы, физиотерапевтические процедуры). При повышении тонуса желчного пузыря, сфинктера Одди показаны диета № 5, 5а, спазмолитические средства (папаверин, но-шпа), блокаторы кальциевых каналов (нифедипин), тепловые физиотерапевтические процедуры, минеральная вода низкой минерализации (Славяновская и Смирновская, Ессентуки № 4 и № 20, Нарзан и др. обычно в горячем виде дробно, 5–6 приемов в день по 1/3-1/2 стакана).
При снижении тонуса желчного пузыря, недостаточности сфинктера Одди рекомендуются диета № 5, 15, лечебная физкультура и физиотерапевтические средства тонизирующего действия, желчегонные средства (аллохол, холензим и др.), закрытые тюбажи, курсовое лечение минеральной водой высокой минерализации типа Ессентуки № 17, Арзни, Баталинская и др.; воду назначают в холодном или слегка подогретом виде по 200–250 мл 2–3 раза в день за 30–90 мин до еды. Хирургическое лечение, как правило, не показано.
Профилактика дискинезий желчных путей заключается в соблюдении рационального режима и характера питания, нормализации режима труда и отдыха, систематическом занятии физкультурой, устранении стрессовых ситуаций, своевременном лечении невротических расстройств.
ДИСКИНЕЗИИ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА – функциональные заболевания, проявляющиеся нарушением тонуса и перистальтики органов пищеварения, имеющих гладкую мускулатуру (пищевода, желудка, желчных путей, кишечника), – эзофагоспазм, гастроэзофагеальная рефлюксная болезнь, функциональная диспепсия, дискинезии двенадцатиперстной кишки, желчных путей, синдром раздраженной толстой кишки.
ДИСКИНЕЗИЯ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ – клинический синдром, наблюдающийся при заболеваниях центральной и периферической нервной системы, эндокринных заболеваниях; нередко сопровождает язвенную и желчнокаменную болезни, панкреатит.
Симптомы: боль спастического характера и чувство давления или переполнения в эпигастральной области, тошнота, приступы рвоты. При рентгенологическом исследовании двенадцатиперстной кишки определяются длительная задержка взвеси сульфата бария в ней (свыше 40 с), чередование спазмов и расширений различных участков кишки, забрасывание контрастной массы в более проксимальные отделы кишки, желудок.
Лечение. Регуляция режима и характера питания, образа жизни, занятия физкультурой, седативные средства и транквилизаторы. При спастической дискинезии кишечника используют спазмолитические (папаверин, но-шпа) и холинолитические (гастроцепин) средства. При гипотонической дискинезии помогают самомассаж живота, лечебная физкультура, общеукрепляющая терапия, лекарственные средства, нормализующие моторику желудочно-кишечного тракта (домперидон, цизаприд и др.).
ДИСПЕПСИЯ – собирательный термин для обозначения субъективных проявлений расстройств пищеварения, включая боль, тяжесть, чувство переполнения в подложечной области, быстрое насыщение, жжение, тошноту, рвоту, отрыжку, изжогу, срыгивание, анорексию, а иногда и боль в животе, метеоризм, поносы и запоры. В последние годы под диспепсией предлагают понимать только боль или ощущение дискомфорта, локализуемое пациентом в подложечной области ближе к срединной линии. Ощущение дискомфорта включает тяжесть, распирание в подложечной области, тошноту, раннее насыщение. Различают органическую и функциональную (неязвенную) диспепсию.
Этиология. Причиной органической диспепсии может быть гастроэзофагеальная рефлюксная болезнь, язвенная болезнь, опухоль желудка, желчнокаменная болезнь, хронический панкреатит и др. Если при обследовании эти заболевания исключены, а признаки диспепсии сохраняются на протяжении 12 нед в течение года, диагностируется синдром функциональной диспепсии. Выявляемые у некоторых пациентов с функциональной диспепсией признаки гастрита не могут объяснить клиническую симптоматику, поскольку у большинства больных хроническим гастритом жалоб вообще нет.
В происхождении функциональной диспепсии могут играть роль личностные особенности пациента, способствующие формированию астенического состояния с частыми эпизодами тревоги, а также злоупотреблению алкоголем, курению, нарушению качества и режима питания. Важную роль в патогенезе функциональной диспепсии играют нарушения моторики желудка и двенадцатиперстной кишки. Расстройства способности фундального отдела желудка к расслаблению после приема пищи обусловливают чувство раннего насыщения, гастропарез – чувство переполнения в подложечной области, тошноту, рвоту; при нормальной эвакуаторной функции желудка причиной функциональной диспепсии может быть повышенная чувствительность рецепторов стенки желудка к растяжению.
Симптомы, течение. Условно выделяют язвенноподобный и диски нетический варианты функциональной диспепсии. При язвенноподобной диспепсии боли в подложечной области могут возникать натощак, по ночам, проходят после приема антацидов. Для дискинетического варианта характерны жалобы на раннее насыщение, чувство переполнения в желудке, тошноту, ощущение вздутия в верхней половине живота, дискомфорта, усиливающегося после приема пищи. Явления диспепсии нередко сопровождаются признаками депрессии, тревогой. Функциональная диспепсия нередко сочетается с синдромом раздраженной толстой кишки, что объясняют общностью их патогенетических механизмов.
При обнаружении таких симптомов, как лихорадка, дисфагия, примесь крови в кале, немотивированное похудание, анемия, лейкоцитоз, увеличение СОЭ, а также при возникновении диспепсии впервые в возрасте старше 45 лет диагноз функциональной диспепсии исключается. Для уточнения причины диспепсии используют рентгенологические, эндоскопические и ультразвуковые методы исследования, анализ крови, исследование кала на скрытую кровь; при необходимости выполняют суточное мониторирование пищеводного рН, компьютерную томографию.
Лечение. При органической диспепсии показано лечение основного заболевания. При функциональной диспепсии рекомендуют диетотерапию – целесообразны прием пищи малыми порциями и уменьшение общего ее количества, ограничение жиров, кофе, алкоголя, отказ от курения и др. При язвенноподобном варианте используют антациды, Н2-гистаминовые блокаторы (ранитидин, фамотидин), блокаторы протонного насоса (омепразол); при дискинетическом варианте – прокинетики (метоклопрамид, домперидон, цизаприд). Возможны применение психотерапевтических методов, использование анксиолитиков и антидепрессантов в небольших дозах.
ДУБИНА – ДЖОНСОНА СИНДРОМ – см. Гипербилирубинемии врожденные.
ДУОДЕНИТ – воспалительные заболевания двенадцатиперстной кишки. Встречаются часто, преимущественно у мужчин. Различают дуодениты острые и хронические, распространенные и ограниченные (главным образом луковицей двенадцатиперстной кишки – бульбит).
Острый дуоденит обычно протекает в сочетании с острым воспалением желудка и кишечника как острый гастроэнтерит, гастроэнтероколит; бывает катаральным, эрозивно-язвенным и флегмонозным.
Этиология, патогенез. Играют роль пищевые токсикоинфекции, отравления токсическими веществами, обладающими раздражающим действием на слизистую оболочку пищеварительного тракта, чрезмерный прием очень острой пищи обычно в сочетании с большим количеством крепких алкогольных напитков, повреждения слизистой оболочки двенадцатиперстной кишки инородными телами.
Симптомы, течение. Характерны боль в эпигастральной области, тошнота, рвота, общая слабость, болезненность при пальпации в эпигастральной области. Диагноз (в необходимых случаях) подтверждается дуоденофиброскопией, обнаруживающей воспалительные изменения слизистой оболочки двенадцатиперстной кишки. При очень редком флегмонозном дуодените резко ухудшается общее состояние больного, определяются напряжение мышц брюшной стенки в эпигастральной области, положительный симптом Щеткина – Блюмберга, лихорадка, нейтрофильный лейкоцитоз, повышение СОЭ. Дуоденальное зондирование и дуоденофиброскопия противопоказаны.
Острый катаральный и эрозивно-язвенный дуоденит обычно заканчивается самоизлечением через несколько дней; при повторных дуоденитах возможен переход в хроническую форму. При флегмонозном дуодените прогноз серьезный. Возможны осложнения: кишечные кровотечения, перфорация стенки кишки, развитие острого панкреатита.
Лечение. При остром катаральном и эрозивно-язвенном дуодените 1–2 дня – голод, постельный режим, промывания желудка слабым раствором перманганата калия с последующим введением 25–30 г сульфата магния в стакане воды (в целях очищения кишечника). В последующие дни – диета № 1a-1, вяжущие и обволакивающие средства внутрь, при боли – спазмолитические и холинолитические препараты. При флегмонозном дуодените лечение оперативное в сочетании с антибиотикотерапией.
Хронический дуоденит бывает поверхностным, атрофическим, интерстициальным (без атрофии желез) или эрозивно-язвенным.
Этиология, патогенез. Имеют значение нерегулярное питание с частым употреблением острой, раздражающей, слишком горячей пищи, алкоголизм. Бульбит, как правило, связан с гастритом, язвенной болезнью желудка, двенадцатиперстной кишки. Дистальный дуоденит нередко сопутствует заболеваниям поджелудочной железы (хроническому панкреатиту), печени (желчных путей, кишечника). Хронический дуоденит наблюдается также при лямблиозе, гельминтозах. Помимо непосредственного воздействия раздражающего агента на слизистую оболочку двенадцатиперстной кишки, в патогенезе хронического дуоденита имеет значение протеолитическое действие на нее активного желудочного сока (при трофических нарушениях, дискинезиях).
В развитии хронического дуоденита в последние годы большое значение придают инфекции Helicobacter pylori. Антральный хеликобактерный гастрит способствует сбросу кислого желудочного содержимого в двенадцатиперстную кишку, метаплазии в ней желудочного эпителия. Внедрение Helicobacter pylori в метаплазированные клетки снижает устойчивость слизистой оболочки двенадцатиперстной кишки к воздействию кислотнопептического фактора, развивается эрозивное поражение луковицы двенадцатиперстной кишки.
Симптомы, течение. Характерна боль в эпигастральной области – постоянная, тупого характера или язвенноподобная, ощущение полноты или распирания в верхних отделах живота после еды, снижение аппетита, тошнота, иногда рвота. Пальпаторно отмечается болезненность глубоко в эпигастральной области. Диагноз подтверждается дуоденофиброскопией. При необходимости проводят биопсию слизистой оболочки двенадцатиперстной кишки. Данные рентгенологического исследования малохарактерны. Течение длительное с периодами обострения (при пищевых погрешностях и пр.).
Прогноз благоприятный при соответствующем лечении. Осложнения: кишечные кровотечения при эрозивно-язвенной форме дуоденита.
Лечение в период обострения проводят в стационаре. Назначают диету № 1а, затем 16, вяжущие, обволакивающие средства (де-нол, сукральфат и др.). При повышенной кислотности показаны антисекреторные средства (омепразол, ранитидин или фамотидин). Симптоматическая терапия проводится антацидами (альмагель, фосфалюгель, маалокс и др.), прокинетиками (домперидон, цизаприд, дебридат и др.). При лямблиозных и гельминтозных дуоденитах показана соответствующая химиотерапия.
Профилактика. Рациональное регулярное питание, борьба с алкоголизмом, своевременное лечение других заболеваний, на фоне которых возникает вторичный дуоденит. Больные хроническим дуоденитом должны находиться под диспансерным наблюдением.
ЕЮНИТ – см. Энтерит.
ЖЕЛТУХА – синдромы различного происхождения, характеризующиеся желтушным окрашиванием кожи и слизистых оболочек.
Желтуха (истинная) – симптомокомплекс, характеризующийся желтушным окрашиванием кожи и слизистых оболочек, обусловленный накоплением в тканях и крови билирубина. Ложная желтуха – желтушное окрашивание кожи (но не слизистых оболочек!) вследствие накопления в ней каротинов при длительном и обильном употреблении в пищу моркови, апельсинов, тыквы, а также возникающая при приеме внутрь акрихина, пикриновой кислоты и некоторых других препаратов.
Истинная желтуха появляется в результате несоответствия между образованием билирубина и его выделением. Причиной нарушения желчевыделительной функции печени могут быть: поражение печеночных клеток (паренхиматозная желтуха), нарушение оттока желчи по желчным протокам (механическая желтуха – см. главу «Хирургические болезни»), усиленный распад эритроцитов (гемолиз) с освобождением большого количества билирубина, который печень не в состоянии переработать (гемолитическая желтуха – см. «Болезни системы крови»).
Паренхиматозная (печеночная) желтуха возникает при различных поражениях паренхимы печени. Наблюдается при тяжелых формах вирусного гепатита, иктерогеморрагическом лептоспирозе, отравлениях гепатотоксическими ядами, сепсисе, хроническом агрессивном гепатите и т. д. Вследствие поражения гепатоцитов снижается их функция по улавливанию свободного (непрямого) билирубина из крови, связыванию его с глюкуроновой кислотой с образованием нетоксичного водорастворимого билирубинаглюкуронида (прямого) и выделению последнего в желчные капилляры. В результате в сыворотке крови повышается содержание билирубина (до 50-200 мкмоль/л, реже больше). Однако в крови повышается не только содержание свободного, но и связанного билирубина (билирубина-глюкуронида) – за счет его обратной диффузии из желчных капилляров в кровеносные при дистрофии и некробиозе печеночных клеток. Возникает желтушное окрашивание кожи, слизистых оболочек.
Для паренхиматозной желтухи характерен цвет кожи – шафрановожелтый, красноватый («красная желтуха»). Вначале желтушная окраска проявляется на склерах и мягком небе, затем окрашивается кожа. Паренхиматозная желтуха сопровождается зудом кожи, однако менее выраженным, чем механическая, так как пораженная печень меньше продуцирует желчных кислот (накопление которых в крови и тканях и вызывает этот симптом). При длительном течении паренхиматозной желтухи кожа может приобретать, как и при механической, зеленоватый оттенок (за счет превращения отлагающегося в коже билирубина в биливердин, имеющего зеленый цвет). Обычно повышается содержание альдолазы, аминотрансфераз, особенно аланинаминотрансферазы, изменены другие печеночные пробы. Моча приобретает темную окраску (цвета пива) за счет появления в ней связанного билирубина и уробилина. Кал обесцвечивается за счет уменьшения содержания в нем стеркобилина. Соотношение количества выделяемого стеркобилина с калом и уробилиновых тел с мочой (являющееся важным лабораторным признаком дифференциации желтух), составляющее в норме 10: 1-20: 1, при печеночноклеточных желтухах значительно снижается, достигая при тяжелых поражениях до 1: 1.
Течение зависит от характера поражения печени и длительности действия повреждающего начала; в тяжелых случаях может возникнуть печеночная недостаточность.
Дифференциальный диагноз проводится с гемолитической, механической и ложной желтухой; он основывается на анамнезе, клинических особенностях паренхиматозной желтухи и данных лабораторных исследований.
Лечение. Проводят лечение основного заболевания.
ЖЕЛЧНОКАМЕННАЯ БОЛЕЗНЬ – см. главу «Хирургические болезни».
ЗАПОР (констипация) – нарушение функции кишечника, выражающееся в увеличении интервалов между актами дефекации по сравнению с индивидуальной нормой или в систематически недостаточном опорожнении кишечника. Запором считают хроническую задержку опорожнения кишечника более чем на 48 ч, сопровождающуюся затруднением акта дефекации, чувством неполного опорожнения с отхождением малого количества (менее 100 г) кала повышенной твердости.
Этиология. Функциональные запоры возникают при недостаточном поступлении с пищей клетчатки, воды (алиментарные запоры) и при недостаточной физической активности, в том числе у послеоперационных больных, после инфаркта миокарда, при преимущественно сидячем образе жизни (гиподинамические запоры). Органическое поражение кишечника служит причиной запоров при закупорке просвета толстой и прямой кишки (например, при сужении кишки опухолью, рубцами, механическом сдавлении прямой кишки извне), нарушении функции мышечного слоя стенки толстой кишки (например, при синдроме раздраженной толстой кишки, системной склеродермии), болезненности дефекации (анальные трещины, тромбоз наружных геморроидальных узлов, проктит). Внекишечные причины лежат в основе запоров неврогенных (при функциональных либо органических заболеваниях ЦНС, частых сознательных подавлениях рефлекса на дефекацию, обусловленных условиями жизни или труда, – отсутствие туалета, работа водителя, продавца и т. д.), «эндокринных» (при понижении функции гипофиза, щитовидной, паращитовидной желез, яичников), токсических (при хронических профессиональных отравлениях свинцом, ртутью, таллием), медикаментозных (вызываемых наркотическими анальгетиками, антацидами, содержащими алюминий, холиноблокаторами, спазмолитиками, препаратами железа, висмута, антагонистами кальция, постоянным приемом слабительных средств и др). Перечисленные причины могут вызвать преимущественно двигательные расстройства кишечника (спастические, атонические), либо нарушения секреции и всасывания, либо вазомоторные нарушения; однако в большинстве случаев конечный результат (клинические проявления) – следствие сочетания нескольких нарушений. У некоторых пациентов при обследовании вы-явить причину хронического запора не удается, в этих случаях констатируют наличие идиопатического запора.
Симптомы, течение. Характерна длительная задержка дефекации. При атонических запорах каловые массы обильные, оформленные, колбасовидные; нередко начальная порция очень плотная, большего, чем в норме, диаметра, конечная – полуоформленная. Дефекация осуществляется с большим трудом, очень болезненная; вследствие надрывов слизистой оболочки анального канала на поверхности каловых масс могут появиться прожилки свежей крови. При синдроме раздраженной толстой кишки испражнения приобретают форму овечьего кала (фрагментированный стул). Запоры часто сопровождаются метеоризмом, чувством давления, расширения, спастической болью в животе. Длительные запоры нередко сопровождаются усталостью, вялостью, снижением работоспособности, головными болями, раздражительностью, снижением аппетита, сердцебиением, потливостью. Рентгенологическое исследование выявляет замедление продвижения каловых масс по кишечнику.
Лечение. При запорах, обусловленных органическими заболеваниями толстой кишки, проводят лечение основного заболевания. При хронических запорах в ежедневном пищевом рационе увеличивают количество продуктов, содержащих большое количество растительной клетчатки (овощи, фрукты). Особенно показаны чернослив, свекла, морковь. При спастических запорах диета должна быть более щадящей, мясо и рыбу назначают в отваренном виде, овощи и фрукты – в протертом или в виде пюре. Целесообразно регулярно принимать свежую простоквашу и другие молочнокислые продукты. Больным с атоническими запорами рекомендуют более активный образ жизни, лечебную гимнастику, циркулярный душ, субаквальные ванны. При спастической дискинезии кишечника помогают парафиновые аппликации, хвойные ванны и другие тепловые процедуры, способствующие снятию спазмов кишечника. Если причиной запора в первую очередь является чрезмерная психоэмоциональная лабильность, назначают психотропные средства. При спастических запорах кишечника показаны спазмолитики (папаверин; но-шпа), холинолитические средства (гастроцепин), для коррекции моторно-эвакуаторных нарушений используют прокинетики (домперидон, цизаприд, дебридат и др.).
Применение слабительных средств показано главным образом при запорах у лиц преклонного возраста, больных, прикованных к постели, лиц с психическими заболеваниями. Слабительные средства прямо или опосредованно раздражают рецепторы слизистой оболочки кишечника и вызывают рефлекторное усиление его перистальтики. Различают слабительные средства, действующие на уровне толстого кишечника (кора крушины, лист сенны, бисакодил, гутталакс и др.), на уровне тонкого кишечника (касторовое, оливковое, другие растительные масла, солевые слабительные – сульфат магния и др.), на все отделы кишечника (кафиол, форлакс и др.). Побочные эффекты – нарушение функции кишечника, развитие поноса с метаболическими расстройствами, обезвоживания, снижение функции кишечных ферментов, атония толстого кишечника. При регулярном использовании солевые слабительные нарушают питание организма, препятствуя всасыванию питательных веществ в тонком кишечнике; частый прием касторового масла раздражает тонкий кишечник и также нарушает пищеварение; к слабительным средствам растительного происхождения, действующим на тонкий кишечник быстро развивается привыкание. Противопоказания: кишечная непроходимость, «острый живот», другие воспалительные заболевания в брюшной полости, острые лихорадочные состояния. Усиленная перистальтика кишечника может нежелательно сказаться на течении беременности (например, касторовое масло может стимулировать родовую деятельность).
Прогноз при своевременно назначенном лечении хороший.
ИЛЕИТ– см. Энтерит.
КАНДИДОЗ (кандидамикоз, молочница) – группа заболеваний, вызванных дрожжеподобными грибами рода Candida. Грибы рода Candida обнаруживают на фруктах, овощах, в молочнокислых продуктах, сточных водах бань и т. д., они также являются частыми обитателями (сапрофитами) слизистых оболочек полости рта, пищеварительного тракта, дыхательных путей, влагалища, кожи здоровых людей. Экзогенная передача грибов происходит контактным, возможно, и воздушно-капельным путем, при употреблении в пищу продуктов, содержащих дрожжеподобные грибы. Возникновению кандидоза способствуют нарушения защитных сил организма (тяжелые истощающие заболевания, опухоли, сахарный диабет, авитаминозы и т. д.), а также длительное бесконтрольное применение антибиотиков широкого спектра действия, подавляющих нормальную микрофлору слизистых оболочек и кожи, антагонистов грибов рода Candida. Различают кандидамикоз кожи (см. главу «Кожные и венерические болезни»), изолированный кандидамикоз внутренних органов, пищеварительной системы, легких, мочеполовой системы, влагалища, кандидозный сепсис.
Кандидоз пищеварительной системы чаще всего проявляется поражением слизистой оболочки рта, глотки; характеризуется появлением мелких красных пятен, позже точечных белых налетов на слизистой оболочке языка, щек, гортани, которые могут сливаться, образуя четко очерченные очаги, покрытые молочно-белыми пленками, по удалении которых обнаруживаются эрозированные поверхности. При этом больные отмечают жжение во рту, болезненность слизистых, затруднение (из-за боли) жевания и глотания. Поражение пищевода чаще локализуется в его средней трети, характеризуется отеком и гиперемией его слизистой оболочки, изъязвлениями, покрытыми беловатой пленкой, болезненной дисфагией. Кандидамикоз желудка и кишечника встречается редко и протекает в виде катарального или эрозивного гастрита, энтерита, энтероколита. Тяжелые формы язвенного кандидамикоза желудочно-кишечного тракта могут осложниться желудочно-кишечными кровотечениями, перфорацией и развитием перитонита.
Кандидозный сепсис представляет собой генерализованную форму кандидоза, характеризуется тяжелым общим состоянием больного, гектической лихорадкой, образованием абсцессов в различных органах (в почках, печени, поджелудочной железе, головном мозге, мышцах и т. д.), нередко сопровождается гнойным менингитом, бородавчато-язвенным эндокардитом. Прогноз во многих случаях неблагоприятный.
Диагноз кандидамикозного поражения пищеварительного тракта устанавливают при наличии характерного поражения слизистой оболочки полости рта с молочницей в сочетании с симптомами поражения других органов системы пищеварения. Определить поражение пищевода, желудка, толстой кишки можно при эндоскопическом исследовании (при этом берут отделяемое язвенного поражения, пленки на лабораторное исследование; производят биопсию из пораженных мест). Достоверным является диагноз кандидоза при лабораторном выделении дрожжеподобных грибов (исследуется отделяемое язвенных поражений слизистых оболочек, гной, желчь, при кандидозном сепсисе – кровь), а также обнаружение грибов в гистологических препаратах, полученных при прицельной биопсии. Имеют диагностическую ценность положительные реакции с вакциной грибов Candida в разведении исследуемой сыворотки 1: 200 и выше, с полисахаридным антигеном в реакции связывания комплемента (при разведении сыворотки 1: 20 и выше).
Лечение стационарное. Назначают нистатин по 500 тыс. ЕД 4 раза в день (при генерализованном кандидозном сепсисе суточную дозу увеличивают до 4–6 млн ЕД). При кандидозе прямой кишки используют свечи с нистатином (содержащие 250–500 тыс. ЕД препарата). При кандидозе пищевода применяют кетоконазол в дозе 200 мг в сутки или флуконазол 50-100 мг в сутки; если лечение неэффективно, проводят терапию амфотерицином В.
Профилактика. Устранение возможности заражения от больных кандидозом; санитарно-технический контроль, механизация и автоматизация труда, использование средств личной гигиены и профилактики на предприятиях, где возможны профессиональные кандидозы. Тщательное врачебное наблюдение за больными, которым проводится лечение антибиотиками широкого спектра действия; параллельное назначение витаминов группы В, при возможности – периодическая замена антибиотика; при длительном лечении – профилактическое назначение нистатина или леворина.
КАРДИОСПАЗМ – см. Ахалазия кардии.
КАРЦИНОИД (карциноидный синдром) – редко встречающаяся потенциально злокачественная гормонально-активная опухоль, происходящая из хромаффинных клеток. Преимущественная локализация этой опухоли – в червеообразном отростке, реже в подвздошной, толстой (особенно прямой) кишке, еще реже – в желудке, желчном пузыре, поджелудочной железе; исключительно редко возникает в бронхах, яичнике и других органах.
Этиология. Происхождение многих симптомов заболевания обусловлено гормональной активностью опухоли. Доказано значительное выделение клетками опухоли серотонина, лизил-брадикинина и брадикинина, гистамина, простагландинов.
Симптомы, течение. Клиническая картина складывается из местных симптомов, обусловленных самой опухолью, и так называемого карциноидного синдрома, обусловленного ее гормональной активностью. Выявляется локальная болезненность; нередко отмечаются признаки, напоминающие острый или хронический аппендицит (при наиболее частой локализации опухоли в червеобразном отростке) или симптомы кишечной непроходимости, кишечного кровотечения (при локализации в тонкой или толстой кишке), боль при дефекации и выделение с калом алой крови (при карциноиде прямой кишки), похудание, анемизация. Карциноидный синдром включает своеобразные вазомоторные реакции, приступы бронхоспазма, гиперперистальтики желудочно-кишечного тракта, характерные изменения кожи, поражения сердца и легочной артерии. В выраженной форме он наблюдается не у всех больных, чаще – при метастазах опухоли, особенно множественных, в печень и другие органы. Наиболее характерное проявление карциноидного синдрома – внезапное кратковременное покраснение кожи лица, верхней половины туловища, сопровождающееся общей слабостью, ощущением жара, тахикардией, гипотензией, иногда слезотечением, насморком, бронхоспазмом, тошнотой и рвотой, поносом и схваткообразной болью в животе. Приступы продолжаются от нескольких секунд до 10 мин, в течение дня они могут повторяться многократно. С течением времени гиперемия кожи может стать постоянной и обычно сочетается с цианозом, возникают гиперкератоз и гиперпигментация кожи пеллагроидного типа. Часто у больных определяется недостаточность трехстворчатого клапана сердца и стеноз устья легочного ствола (реже другие пороки сердца), недостаточность кровообращения.
Лабораторное исследование в подавляющем большинстве случаев показывает повышенное содержание в крови 5-гидрокситриптамина (до 0,1–0,3 мкг/мл) и в моче – конечного продукта его превращения – 5-гидроксиндолуксусной кислоты (свыше 100 мг/сут). При рентгенологическом исследовании опухоль выявить трудно из-за ее небольших размеров и эксцентрического роста. Особенностью опухоли являются медленный рост и сравнительно редкое метастазирование, вследствие чего средняя продолжительность жизни больных составляет 4–8 лет и более. Наиболее часто метастазы обнаруживают в регионарных лимфатических узлах и печени. Смерть может наступить от множественных метастазов и кахексии, сердечной недостаточности, кишечной непроходимости.
Лечение хирургическое (радикальное удаление опухоли и метастазов). Симптоматическая терапия приливов заключается в назначении блокаторов альфа-адренергических рецепторов (фентоламин), менее эффективны глюкокортикоиды, нейролептики фенотиазинового ряда, блокаторы Н2-гистаминовых рецепторов (ранитидин).
КИШЕЧНАЯ ЛИМФАНГИЭКТАЗИЯ – см. Энтеропатия экссудативная гипопротеинемическая.
КИШЕЧНАЯ ЛИПОДИСТРОФИЯ (болезнь Уиппла, стеаторея идиопатическая) – редкое системное заболевание с преимущественным поражением тонкой кишки и нарушением всасывания жиров. Встречается преимущественно у мужчин среднего и пожилого возраста. Возбудитель заболевания – грамположительные бациллы Tropheryma Whippelli.
Основными симптомами являются упорный понос (до 5-15 раз в сутки), общее истощение, коликоподобная боль в животе, артралгии. Стул обильный, светлый, пенистый или мазевидный, иногда своеобразный «хилезный». Постепенно развивается мальабсорбция, нарастают проявления белковой недостаточности, гиповитаминоза, нарушения водно-электролитного баланса и др. Могут возникать гипопротеинемические отеки на ногах. Возможна субфебрильная лихорадка. Кожа сухая и гиперпигментированная. Периферические лимфатические узлы увеличены, плотноваты, но безболезненны. Живот вздут, мягкий, в ряде случаев при пальпации можно определить очаговое уплотнение у места прикрепления брыжейки тонкой кишки, образованное конгломератом увеличенных лимфатических узлов. Возможно поражение сердца (эндокардит, миокардит, перикардит), органов дыхания (хронический трахеобронхит, плеврит, пневмонит), ЦНС (головная боль, деменция, эпилептические припадки, офтальмоплегия, нарушения слуха, зрения и др.), почек (интерстициальный нефрит).
В крови определяются умеренный нейтрофильный лейкоцитоз (в ряде случаев эозинофилия), гипопротеинемия, гипохолестеринемия, гипокальциемия. Характерным признаком служит выявление в испражнениях больного большого количества нейтрального жира, кристаллов жирных кислот, непереваренных мышечных волокон. При рентгенологическом исследовании отмечается утолщение складок слизистой оболочки тонкой кишки, снижение ее тонуса и перистальтики.
Диагноз устанавливают при аспирационной биопсии слизистой оболочки тонкой кишки: при гистологическом исследовании биоптатов выявляется атрофия кишечных ворсинок и обнаруживаются специфические для заболевания макрофаги с пенистой цитоплазмой, окрашивающейся в розовый цвет реактивом Шиффа (тельца Сиераки). При электронной микроскопии в макрофагах обнаруживают разрушенные бациллы. Дифференциальный диагноз проводится с хроническим энтеритом, энтероколитом, европейским и тропическим спру, дисахаридазодефицитными и глютеновой энтеропатиями, экссудативной энтеропатией, хроническим панкреатитом.
Течение. Заболевание начинается незаметно, постепенно, с полиартралгии или умеренных поносов, но затем быстро прогрессирует, возникают выраженные нарушения кишечного пищеварения и всасывания. Средняя продолжительность жизни нелеченных больных 2 года, при своевременном выявлении заболевания прогноз благоприятный.
Лечение в периоды обострения процесса стационарное. Назначают диету с повышенным содержанием белка, витаминов и ограничением жиров. Медикаментозная терапия: бисептол или антибиотики широкого спектра действия (тетрациклин, ампициллин, эритромицин) в течение года. Проводится симптоматическое лечение мальабсорбции.
КОЛИТ – группа заболеваний, характеризующихся острым и хроническим воспалением слизистой оболочки толстой кишки.
Колит гранулематозный – см. Крона болезнь в главе «Хирургические болезни».
Колит ишемический – сегментарное поражение толстой кишки, обусловленное нарушением ее кровоснабжения. Чаще поражается область селезеночной кривизны, реже – поперечная ободочная, нисходящая и сигмовидная кишки.
Этиология, патогенез: поражение нижней брыжеечной артерии у пожилых лиц, страдающих атеросклерозом; предрасполагающим фактором является анатомическая особенность отхождения этой артерии под острым углом от аорты.
Симптомы, течение. Гангренозная (некротическая) форма возникает при полной закупорке нижней брыжеечной артерии, проявляется приступом резчайших болей в левой половине живота, признаками кишечной непроходимости, ректальным кровотечением и затем перитонитом. Преходящая эпизодическая форма – «перемежающаяся хромота кишечника» – наблюдается при частичной закупорке этой артерии; проявляется болью в левой половине живота или эпигастрии, возникающей сразу или вскоре после еды, диареей, вздутием живота, иногда рвотой. Постепенно может развиться исхудание. При пальпации живота определяется болезненность соответственно локализации места поражения участка толстой кишки, иногда – защитное напряжение мышц передней брюшной стенки.
Диагноз подтверждается ирриго-, ректоромано– и колоноскопией. При ирригоскопии в зоне поражения обнаруживается картина «псевдотумора» с дефектом наполнения в виде «отпечатка большого пальца». Эндоскопическое исследование выявляет отечность слизистой оболочки пораженного участка, подслизистые кровоизлияния, в хронических случаях – воспалительную инфильтрацию слизистой оболочки, изъязвления и вследствие рубцевания язв – стриктуры пораженного участка кишки. Селективная брыжеечная ангиография позволяет подтвердить нарушение проходимости брыжеечной артерии.
Течение хронической формы прогрессирующее, прогноз в большинстве случаев неблагоприятный. Осложнения: острые кишечные профузные кровотечения, некроз участка кишки с развитием перитонита, постепенное сужение пораженного сегмента вследствие воспалительно-рубцовых процессов в стенке кишки.
Лечение. Больных с гангренозной формой ишемического колита срочно госпитализируют в хирургический стационар. Гангренозная и стриктурная формы требуют хирургического лечения. При хронической форме болезни назначают спазмолитические и холинолитические лекарственные средства.
Колит неспецифический язвенный – см. «Хирургические болезни».
Колит острый обычно бывает распространенным, часто сочетается с одновременным острым воспалением слизистой оболочки тонкой кишки (острый энтероколит), а иногда и желудка (гастроэнтероколит).
Этиология, патогенез. Возбудители острого колита – шигеллы (бактериальная дизентерия), сальмонеллы, реже другая патогенная бактериальная флора, вирусы и т. д. Его причиной могут быть небактериальные пищевые отравления, грубые погрешности в питании. Значительно меньшая роль принадлежит некоторым общим инфекциям, пищевой аллергии, токсическим веществам. Воспалительный процесс в толстой кишке возникает вследствие местного действия на слизистую оболочку кишки повреждающих факторов, которые находятся в содержимом кишечника либо (токсины, бактерии и др.) поступают гематогенным путем и оказывают действие при выделении слизистой оболочкой (экскреторная функция кишки).
Симптомы, течение. Остро возникают боль тянущего или спастического характера, урчание в животе, потеря аппетита, поносы, общее недомогание. Стул жидкий с примесью слизи. В более тяжелых случаях стул водянистый, содержит большое количество слизи, иногда кровь; частота стула до 15–20 раз в сутки; могут присоединяться императивные позывы на дефекацию, болезненные тенезмы. Повышается температура тела (до 38 °C и выше). В особо тяжелых случаях резко выражены симптомы общей интоксикации, язык сухой, обложенный серым или грязно-серым налетом; живот несколько вздут, а при сильном поносе втянут. При пальпации отмечаются болезненность по ходу толстой кишки, в различных ее отделах – урчание.
При ректороманоскопии определяются гиперемия и отек слизистой оболочки дистальных отделов толстой кишки, на стенках кишки видно большое количество слизи, а в более тяжелых случаях – гноя; могут быть эрозии, изъязвления и кровоизлияния. Исследование крови выявляет умеренный лейкоцитоз с палочкоядерным сдвигом, повышение СОЭ.
В легких случаях состояние больного быстро улучшается; в тяжелых случаях заболевание приобретает затяжной характер. Осложнения: абсцессы печени, пиелит, перитонит, сепсис.
Лечение. Больных острым колитом госпитализируют (при подозрении на инфекционную природу заболевания – в инфекционные больницы). Назначают антибактериальную или противопаразитарную терапию, при токсических колитах – солевые слабительные. В первый день разрешают только обильное питье (несладкий или полусладкий чай), затем, на 2– 5-й день, диету № 4, затем № 4б и 4 в. При обезвоживании капельно п/к или в/в вводят 0,9 %-ный раствор хлорида натрия, 5 %-ный раствор глюкозы или гемодез. Внутрь назначают обволакивающие и вяжущие средства (висмута нитрат основной по 1 г 4–6 раз в день, танальбин, каолин и др.), препараты пищеварительных ферментов, холинолитические средства. Для нормализации кишечной флоры назначают эрсефурил, интетрикс, колибактерин, бификол и др.
Профилактика такая же, как при остром энтерите.
Колит псевдомембранозный – см. Дисбактериоз.
Колит хронический – хроническое воспалительное поражение толстой кишки. Нередко сочетается с воспалительным поражением тонкой кишки (энтероколит) и желудка. Диагноз хронического колита как самостоятельного заболевания может быть поставлен только после тщательного обследования пациента (бактериологического исследования кала, колоноскопии с биопсией, рентгенологического исследования толстой кишки) при невозможности установить точную причину воспалительных изменений толстой кишки.
Этиология, патогенез. Хронический колит может быть связан с перенесенными острыми кишечными инфекциями (шигеллез, сальмонеллез, иерсениоз и др.), глистными и паразитарными инвазиями, дисбактериозом. Среди колитов неинфекционного происхождения выделяют радиационный, токсический, аллергический и гиперсенситивный алиментарный. Токсические колиты возникают вследствие длительных экзогенных интоксикаций соединениями ртути, свинца, фосфора, мышьяка и др. Токсические колиты эндогенного происхождения возникают вследствие раздражения стенки кишки выводимыми ею продуктами, образовавшимися в организме (при уремии, подагре). Колиты аллергической природы наблюдаются при пищевой аллергии, при непереносимости некоторых лекарственных и химических веществ, повышенной индивидуальной чувствительности организма к некоторым видам бактериальной флоры кишечника и продуктам распада микроорганизмов. Лекарственные колиты связаны с длительным бесконтрольным применением слабительных средств, нестероидных противовоспалительных средств, антибиотиков и некоторых других лекарств. Нередко при хронических колитах несколько этиологических факторов взаимно усиливают болезнетворное действие. В основе патогенеза хронического колита лежат дисбактериоз, расстройства моторной и секреторной функции толстой кишки.
Симптомы, течение. Чаще наблюдается тотальное поражение всей толстой кишки (панколит). Основными симптомами являются нарушение стула (хронический понос или запор), боль в различных отделах живота, иногда болезненные тенезмы, метеоризм, диспептические расстройства. В большинстве случаев, особенно при правостороннем колите, преобладают поносы – дефекация возникает до 10–15 раз и более в сутки, нередко наблюдается чередование поноса и запора. При обострении процесса появляются ложные позывы на дефекацию, сопровождающиеся отхождением газа и отдельных комочков каловых масс, покрытых тяжами или хлопьями слизи, или слизи с прожилками крови, или периодическим отхождением слизи в виде пленок (колит псевдомембранозный). Боль при колите обычно схваткообразная либо тупая, ноющая, локализуется преимущественно в боковых и нижних отделах живота, усиливается после приема пищи и перед дефекацией. Метеоризм при колите объясняется нарушением переваривания пищи в тонкой кишке и дисбактериозом. Часто наблюдаются анорексия, тошнота, отрыжка, ощущение горечи во рту, урчание в животе и т. д. Могут наблюдаться слабость, общее недомогание, снижение трудоспособности, астеноневротический синдром, похудание, нерезко выраженные симптомы полигиповитаминоза и анемии.
При поверхностной пальпации нередко выявляются участки болезненности брюшной стенки, располагающиеся по ходу толстой кишки, при хроническом перивисцерите отмечается резистентность мышц передней брюшной стенки в соответствующих участках. При глубокой пальпации пораженные участки толстой кишки обычно болезненны и спастически сокращены, могут иметь место чередование спастически сокращенных и расширенных участков, наполненных плотным или жидким содержимым, сильное урчание и даже плеск в соответствующем отделе кишки.
Испражнения нередко зловонны; при копрологическом исследовании определяется большое количество слизи и лейкоцитов, а также эритроцитов (при эрозивных и язвенных формах). Бактериологические исследования кала выявляют нарушения микрофлоры толстой кишки.
При обострениях колита могут быть умеренный нейтрофильный лейкоцитоз со сдвигом влево, повышение СОЭ, субфебрилитет. Обострение аллергического колита, помимо болевого приступа, часто сопровождается лихорадкой, эозинофилией, появлением кристаллов Шарко – Лейдена в испражнениях. Гнойные, фибринозные и некротически-язвенные колиты протекают со значительно более тяжелой клинической картиной.
Ирригоскопия при хроническом колите особых изменений не выявляет; обнаруживаются функциональные нарушения (ускорение или замедление перистальтики кишки, усиленная гаустрация, спастические сокращения или, наоборот, атония кишечной стенки). При тяжелых формах колитов выявляются изменения рельефа слизистой оболочки кишки за счет воспалительного отека и инфильтрации, в ряде случаев участки рубцово-воспалительного сужения просвета кишки. Ректороманоскопия, сигмоидоскопия и колоноскопия чаще всего обнаруживают гиперемию, отек и кровоточивость слизистой оболочки кишки, реже – эрозии, бледность слизистой оболочки при атрофическом колите. Диагноз хронического колита подтверждается при гистологическом исследовании – выявляют признаки воспаления слизистой оболочки кишки с лимфоцитарной инфильтрацией.
Сегментарные колиты. Хронический тифлит чаще сопутствует хроническому энтериту и аппендициту, нередко – алиментарного происхождения или слепая кишка вовлекается в процесс при хроническом правостороннем аднексите. Протекает с упорными болями в правой подвздошной области, иррадиирующими в пах, поясницу; вздутием и урчанием в правой половине живота в большинстве случаев с обильным полужидким стулом 3–5 раз в сутки («коровий кал»), В области слепой кишки и восходящего отдела ободочной кишки – болезненность, иногда они спастически сокращены, иногда расслаблены, при их ощупывании отмечается сильное урчание. При перитифлите в период обострения воспалительного процесса может определяться нерезко выраженный симптом Щеткина – Блюмберга, что может симулировать обострение хронического аппендицита.
Изолированный трансверзит возникает сравнительно редко и во многих случаях сочетается с колоптозом. Поражение поперечной ободочной кишки и особенно ее дистальной части часто обусловлено затруднением прохождения ее содержимого через необычно заостренный левый изгиб в нисходящую ободочную кишку (вследствие значительного опущения поперечной ободочной кишки, образования спаек, аномалии развития толстой кишки и других причин) – так называемый синдром селезеночной кривизны. Проявляется тупой болью в эпигастральной, околопупочной областях и левом подреберье, нередко усиливающейся после еды, метеоризмом, ощущением распирания живота, которые облегчаются после дефекации, нарушениями стула. При пальпации определяется болезненная, нередко опущенная и неравномерно спазмированная поперечная ободочная кишка. При выраженных явлениях перипроцесса в области селезеночного изгиба могут возникнуть симптомы частичной, а в редких случаях – полной непроходимости кишечника.
Проктит и проктосигмоидит – наиболее частые формы хронического колита. В их происхождении особую роль играют бактериальная дизентерия, хронический запор, систематическое раздражение слизистой оболочки прямой кишки при злоупотреблениях слабительными и лечебными клизмами, свечами. Проявляются болью в левой подвздошной области и в области заднего прохода, болезненными тенезмами, метеоризмом; боль может сохраняться некоторое время после дефекации, возникать при проведении очистительной клизмы. Нередко наблюдаются запоры в сочетании с тенезмами; стул необильный, иногда типа «овечьего кала», содержит много видимой слизи, а нередко кровь и гной. При пальпации отмечается болезненность сигмовидной кишки, ее спастическое сокращение или урчание (при поносе). В ряде случаев выявляется дополнительная петля сигмовидной кишки – долихосигма (врожденная аномалия развития). Осмотр анальной области и пальцевое исследование прямой кишки позволяют оценить состояние ее сфинктера, выявить нередко встречающуюся сопутствующую патологию, развивающуюся на фоне хронического проктита (геморрой, трещины заднего прохода, парапроктит, выпадение прямой кишки и др.). Большое диагностическое значение имеет ректороманоскопия.
Дифференциальный диагноз. В первую очередь следует исключить колиты инфекционного или паразитарного происхождения. Возникновение хронического колита после острого проктосигмоидита заставляет заподозрить самый частый вид инфекционного колита – дизентерийный. Нахождение шигелл при бактериологическом исследовании позволяет подтвердить диагноз. Для диагноза хронических колитов, возникающих в результате паразитарных инвазий, основное значение имеет обнаружение соответствующих возбудителей, цист, члеников или яичек гельминтов в испражнениях.
Хронические колиты следует дифференцировать от хронических энтеритов, панкреатитов, анацидных гастритов, однако очень часто встречается и сочетание этих заболеваний с хроническим колитом. Опухоли толстой кишки могут протекать под маской хронического колита, поэтому в подозрительных случаях всегда нужно проводить ирригоскопию, а при недостаточно ясной картине – эндоскопию с биопсией.
Течение хронического колита в одних случаях длительное, малосимптомное, в других – постепенно прогрессирующее с чередованием периодов обострений и ремиссий, развитием атрофических изменений в стенке кишки. При своевременном лечении прогноз благоприятный. Осложнения: перфорация язв при тяжелом язвенном колите, кишечные кровотечения, сужение просвета кишки (при рубцевании язв), спаечный процесс.
Лечение в период обострения проводится в стационаре; больных инфекционными и паразитарными колитами лечат в инфекционных отделениях больниц. Показано частое дробное питание (4–6 раз в сутки), диета механически щадящая (слизистые супы, пюре, фрикадельки, паровые мясные и рыбные котлеты и т. д.). Пища должна содержать 100–120 г белка, 100–120 г легко усваиваемых жиров (сливочное, растительное масла), около 400–500 г углеводов. В период наибольшей остроты процесса временно ограничивают поступление в организм углеводистых продуктов (до 350 и даже 250 г) и жиров. Жиры переносятся и усваиваются больными хроническими заболеваниями кишечника лучше, если они поступают в организм не в чистом виде, а в связи с другими пищевыми веществами (в процессе кулинарной обработки пищи). Переносимость углеводов и растительной клетчатки значительно повышается при их соответствующей кулинарной обработке (протирание, варка на пару, в наиболее тяжелых случаях – гомогенизированные овощные пюре и др.).
Витамины назначают внутрь в виде поливитаминов или парентерально (С, В2, В6, В12 и др.). Фрукты используют в виде киселей, соков, пюре, в печеном виде (яблоки), а в период ремиссии – и в натуральном виде, за исключением тех, которые способствуют усилению процессов брожения в кишечнике (виноград) или обладают послабляющим действием, что нежелательно при поносах (чернослив, инжир и др.). Холодная пища и напитки, низкомолекулярные сахара, молочнокислые продукты с кислотностью выше 90° по Тернеру усиливают перистальтику кишечника, поэтому их при обострениях колита и поносах исключают, как и острые приправы, пряности, тугоплавкие жиры, черный хлеб, свежие хлебные продукты из сдобного или дрожжевого теста, капусту, свеклу, кислые сорта ягод и фруктов, ограничивают поваренную соль. Основная диета в период обострения – № 2, 4 и 4а (при преобладании бродильных процессов), по мере стихания воспалительного процесса – диета № 46 и более расширенная, приближающаяся к нормальной – диета № 4в (пища в непротертом виде). Полезно ацидофильное молоко (150–200 г 3 раза в день). При наличии сопутствующих заболеваний (холецистит, панкреатит, атеросклероз) в диету вносят необходимые коррективы.
По показаниям проводят лечение кишечного дисбактериоза. Применяют антибиотики широкого спектра действия (тетрациклины; левомицетин, аминогликозиды и др.) или сульфаниламидные препараты (сульгин, фталазол, бисептол) в обычных дозах. Наиболее эффективным во многих случаях является назначение интетрикса, энтеросептола, интестопана, которые оказывают угнетающее действие в первую очередь на патогенную флору кишечника, уменьшают бродильные и гнилостные процессы. Полезны колибактерин, бифидумбактерин, бификол, лактобактерин и другие бактериальные препараты; антибактериальные средства назначают короткими курсами.
При проктосигмоидите назначают микроклизмы (ромашковые, таниновые, протарголовые, из взвеси висмута нитрата), а при проктите – вяжущие средства (ксероформ, дерматол, цинка окись и др.) в свечах, нередко в комбинации с белладонной и анестезином.
При поносе рекомендуются вяжущие и обволакивающие средства (танальбин, тансал, висмута нитрат основной, белая глина и др.), настои и отвары растений, содержащие дубильные вещества (отвары 15: 2000 корневищ змеевика, лапчатки или кровохлебки по 1 ст. л. 3–6 раз в день, настой или отвар плодов черемухи, плодов черники, соплодий ольхи, травы зверобоя и др.), холинолитики (гастроцепин, метацин и др.).
При выраженном метеоризме рекомендуются уголь активированный (по 0,25-0,5 г 3–4 раза в день), настой листа мяты перечной (5: 200 по 1 ст. л. несколько раз в день), цветков ромашки (10: 200 по 1–2 ст. л. несколько раз в день) и другие средства. Если понос обусловлен в первую очередь секреторной недостаточностью желудка, поджелудочной железы, сопутствующим энтеритом, полезны препараты пищеварительных ферментов – креон, панцитрат, панкреатин, фестал и др.
Большое место в терапии обострений хронических колитов занимают физиотерапевтические методы (кишечные орошения, грязевые аппликации, диатермия и др.) и санаторно-курортное лечение (Ессентуки, Железноводск, местные санатории для больных с заболеваниями кишечника).
Трудоспособность больных при средней тяжести и тяжелых формах хронических колитов, особенно сопровождающихся поносами, ограничена. Им не показаны виды работ, связанные с невозможностью соблюдать режим питания, частыми командировками.
Профилактика: своевременное лечение острых колитов, диспансеризация реконвалесцентов, санитарно-просветительная работа, направленная на разъяснение населению необходимости соблюдения рационального режима питания, полноценной диеты, тщательного прожевывания пищи, своевременной санации полости рта, а при необходимости – протезирования зубов, занятий физической культурой и спортом, укрепления нервной системы. Необходимо строгое соблюдение правил техники безопасности на производствах, связанных с химическими веществами, способными вызвать поражения толстой кишки.
МАЛЬАБСОРБЦИИ СИНДРОМ (синдром недостаточности всасывания) – симптомокомплекс, возникающий вследствие расстройства переваривания и всасывания в тонкой кишке. Различают первичный (наследственно обусловленный) и вторичный (приобретенный) синдром недостаточности всасывания.
Этиология, патогенез. Причина возникновения первичного синдрома недостаточности всасывания – наследственные нарушения структуры слизистой оболочки кишечной стенки и генетически обусловленная кишечная ферментопатия. В частности, недостаточность дисахаридаз (ферментов, обеспечивающих процессы гидролиза углеводов-дисахаридов) проявляется нарушением всасывания продуктов, содержащих соответствующие углеводы. К развитию вторичного синдрома недостаточного всасывания приводят заболевания желудка (хронический гастрит с секреторной недостаточностью, резекция желудка, демпинг-синдром), кишечника (язвенный колит, болезнь Крона, болезнь Уиппла, экссудативная энтеропатия, целиакия, дивертикулез и дивертикулит, обширная резекция и опухоли тонкой кишки, бактериальные, вирусные поражения кишечника, паразитарные, глистные инвазии и др.), печени (хронический гепатит, цирроз печени, холестаз), поджелудочной железы (хронический панкреатит, резекция поджелудочной железы), сосудистые расстройства (ишемический колит), интоксикации (алкогольная, уремия и др.), применение некоторых лекарственных средств (антибиотиков, цитостатиков, иммунодепрессантов, нестероидных противовоспалительных средств и др.), эндокринные заболевания (например, тиреотоксикоз) и др.
При острых и подострых состояниях основное значение имеет нарушение внутрикишечного переваривания пищевых продуктов и ускоренный пассаж содержимого по кишечнику, при хронических – дистрофические и атрофически-склеротические изменения слизистой оболочки тонкой кишки, укорочение и уплощение ворсин и крипт, резкое сокращение числа микроворсинок, развитие фиброзной ткани в стенке кишки с нарушением в ней крово– и лимфотока, нарушение процессов пристеночного пищеварения. Все перечисленные изменения приводят к недостаточному поступлению в организм продуктов гидролиза белков, жиров, углеводов, а также минеральных солей и витаминов через кишечную стенку. Синдром мальабсорбции неизбежно сопровождается дисбактериозом тонкой кишки, усугубляющим нарушения пищеварения и всасывания, моторики кишечника, усиливающим кишечную секрецию.
Симптомы, течение. Клиническая картина синдрома мальабсорбции складывается из диареи и других кишечных проявлений (полифекалия, стеаторея, креаторея, амилорея) и расстройств обмена веществ – белкового, жирового, витаминного, водно-солевого. Характерны постепенное истощение больного вплоть до кахексии, дистрофические изменения во внутренних органах с постепенно возникающими нарушениями их функции. При гипопротеинемии ниже 40–50 г/л возникают гипопротеинемические отеки. Недостаточность тиамина проявляется парестезиями, болями в ногах, бессонницей, никотиновой кислоты – глосситом, изменениями кожи, аскорбиновой кислоты – кровоточивостью десен, кровоизлияниями в кожу, витамина А – нарушениями сумеречного зрения, витамина В12, фолиевой кислоты, железа – анемией. Дефицит натрия обусловливает тахикардию, артериальную гипотонию, жажду, сухость во рту, дефицит калия – боли и слабость мышц, снижение сухожильных рефлексов, экстрасистолию, недостаток кальция – остеопороз, остеомаляцию. Характерны трофические изменения кожи, ногтей, прогрессирующая атрофия мышц, явления полигландулярной недостаточности, общая слабость, в тяжелых случаях – психические расстройства, ацидоз.
Лабораторные методы позволяют определить гипопротеинемию, гипохолестеринемию, гипогликемию и другие нарушения как следствие недостаточного всасывания в кишечнике. При копрологическом исследовании отмечается повышенное выделение непереваренных пищевых веществ, а также продуктов их ферментативного расщепления. Стеаторея (обнаружение капель нейтрального жира) – проявление недостаточности панкреатической липазы, амилорея (непереваренные зерна крахмала) – панкреатической амилазы, креаторея (непереваренные мышечные волокна) появляется при нарушении переваривания белков. Для исследования процессов всасывания используется проба с D-ксилозой, методы с применением меченных радионуклидами альбумина или жиров. Интестиноскопия (еюноскопия) с обязательной биопсией выявляет атрофические изменения слизистой оболочки тонкой кишки, в некоторых случаях позволяет уточнить причину нарушенного всасывания (например, при целиакии, болезнях Крона, Уиппла).
Течение зависит от характера основного заболевания и возможности его излечения.
Лечение первичного синдрома нарушенного всасывания подразумевает диету с исключением или ограничением непереносимых продуктов. При вторичном синдроме проводят лечение основного заболевания. Симптоматическая терапия включает парентеральное питание, введение витаминов, плазмы, белковых гидролизатов, раствора глюкозы, препаратов железа, средств, влияющих на ремоделирование костной ткани (метаболитов витамина D и др.), питательные кишечные клизмы, коррекцию нарушений электролитного обмена. В качестве заместительной терапии применяют панкреатические ферменты (креон, панцитрат, менее эффективны фестал, панзинорм, мезимфорте и др.). Проводится лечение сопутствующего дисбактериоза (биологические бактерийные препараты, по показаниям – антибактериальные средства). Антидиарейный эффект оказывают вяжущие средства, энтеросорбенты (смекта и др.).
ПАНКРЕАТИТ ОСТРЫЙ – см. главу «Хирургические болезни».
ПАНКРЕАТИТ ХРОНИЧЕСКИЙ – заболевание, характеризующееся хроническим воспалением поджелудочной железы. Встречается обычно в среднем и пожилом возрасте, чаще у женщин.
Этиология. Основные причины хронического панкреатита – хронический алкоголизм (особенно у мужчин) и желчнокаменная болезнь (чаще у женщин). Реже в качестве этиологического фактора выступают применение некоторых лекарственных средств (тиазидов, фуросемида, тетрациклина, сульфаниламидов и др.), муковисцидоз (чаще выявляется у детей), гиперпаратиреоз, семейная гиперхолестеринемия, гемохроматоз, недостаточное содержание белка и жиров в пище (недоедание). В хронический может перейти острый панкреатит со стенозированием главного панкреатического протока. Предрасполагают к возникновению хронического панкреатита спазмы, воспалительный стеноз или опухоль большого сосочка двенадцатиперстной кишки, препятствующие выделению панкреатического сока в двенадцатиперстную кишку, а также недостаточность сфинктера Одди, облегчающая свободное попадание дуоденального содержимого в проток поджелудочной железы, особенно содержащейся в кишечном соке энтерокиназы, активирующей трипсин.
Патогенез. Важную роль играет задержка выделения и внутриорганная активация панкреатических ферментов – трипсина и липазы, осуществляющих аутолиз паренхимы железы. Деструкция ткани железы и прогрессирующий воспалительный процесс приводят к атрофии, склерозированию органа. В основе хронического калькулезного панкреатита лежит поражение протоков и канальцев за счет образования в них камней и белковых пробок, которые в дальнейшем могут кальцифицироваться. Различают хронический панкреатит кальцифицирующий (обычно алкогольной этиологии, характеризуется наличием камней в ткани железы и протоках, дилатацией протоков), обструктивный (с обструкцией панкреатических протоков кальцинатами, опухолью, при стенозе или опухоли фатерова соска и др.) и паренхиматозный (воспалительный).
Симптомы, течение. Боль в эпигастральной области и левом подреберье, признаки экзокринной (поносы, стеаторея, похудание) и эндокринной (присоединение сахарного диабета) недостаточности. Боль локализуется в эпигастральной области справа при преимущественной локализации процесса в области головки поджелудочной железы, при вовлечении в воспалительный процесс ее тела – в эпигастральной области слева, при поражении ее хвоста – в левом подреберье; нередко боль иррадиирует в спину и имеет опоясывающий характер, может ирради-ировать в область сердца, имитируя стенокардию. Боль может быть постоянной или приступообразной и появляться через некоторое время после приема жирной или острой пищи. Отмечается болезненность в эпигастральной области и левом подреберье. Нередко болезненна точка в левом реберно-позвоночном углу (симптом Мейо – Робсона). Иногда определяются зона кожной гиперестезии соответственно зоне иннервации восьмого грудного сегмента слева (симптом Кача) и некоторая атрофия подкожной жировой клетчатки в области проекции поджелудочной железы на переднюю стенку живота.
Болевой синдром нередко сопровождается диспепсией. Часты полная потеря аппетита и отвращение к жирной пище. Однако при развитии сахарного диабета, наоборот, больные могут ощущать сильный голод и жажду. Часто наблюдаются повышенное слюноотделение, отрыжка, приступы тошноты, рвоты, метеоризм, урчание в животе.
Стул в легких случаях нормальный, в более тяжелых – понос или чередование запора и поноса. Характерен панкреатический понос с выделением обильного кашицеобразного зловонного с жирным блеском кала; копрологическое исследование выявляет стеаторею, креаторею.
В крови в период обострения определяют повышение СОЭ, нейтрофильный лейкоцитоз. При развитии сахарного диабета выявляют гипер-гликемию и глюкозурию. Содержание амилазы и липазы в крови может быть повышено (в период обострения панкреатита), понижено или оставаться в пределах нормы; хронический панкреатит можно заподозрить при пониженной концентрации этих ферментов. Обзорный рентгеновский снимок живота нередко позволяет выявить кальцинаты в поджелудочной железе. Ультразвуковое исследование показывает размеры и интенсивность тени поджелудочной железы; при хроническом панкреатите выявляют расширение протоков и повышение эхогенности поджелудочной железы с нечеткими ее контурами. В диагностически сложных случаях проводят компьютерную томографию, позволяющую выявить увеличение и деформацию поджелудочной железы, кальцинаты, псевдокисты, расширение панкреатического протока, фокальные изменения плотности ткани железы. Состояние протоков поджелудочной железы (наличие обструкции и др.) позволяет оценить эндоскопическая ретроградная холангиопанкреатография. Это исследование проводится чаще при тяжелых панкреатитах перед предполагаемой операцией.
Течение заболевания затяжное. С годами, по мере разрушения паренхимы поджелудочной железы болевой синдром стихает, в клинической картине на первый план выступают признаки экзо– и эндокринной недостаточности. Осложнения: абсцесс поджелудочной железы; холангит; механическая желтуха вследствие сдавления поджелудочной железой общего желчного протока; тромбоз селезеночной вены с варикозным расширением вен желудка; образование псевдокист и др. Возможны желудочнокишечные кровотечения из варикозных вен желудка и пищевода, при прорыве кист или абсцессов в кишечник. При тяжелом обострении возможно развитие гиповолемического шока. На фоне длительно протекающего панкреатита возможно развитие рака поджелудочной железы.
Хронический панкреатит дифференцируют прежде всего с опухолью под-желудочной железы, при этом большое значение приобретают ретроградная холангиопанкреатография, ультразвуковое сканирование поджелудочной железы, компьютерная томография. Может возникнуть необходимость дифференциальной диагностики хронического панкреатита с желчнокаменной болезнью, язвенной болезнью желудка и двенадцатиперстной кишки (следует учитывать также возможность сочетания этих заболеваний), хроническим энтеритом и реже другими формами патологии системы пищеварения.
Лечение. В начальных стадиях заболевания и при отсутствии тяжелых осложнений – консервативное; в период обострения лечение целесообразно проводить в условиях стационара гастроэнтерологического профиля (в период резкого обострения лечение такое же, как при остром панкреатите).
При тяжелых обострениях, протекающих обычно с ночными болями и рвотой, целесообразно голодание в течение 1–3 сут; по показаниям проводится парентеральное питание, водно-солевой баланс корректируется парентеральным введением раствора Рингера, глюкозы и др. Нередко приходится прибегать к постоянной зондовой аспирации желудочного сока (особенно при отсутствии эффекта в первые часы от других лечебных мероприятий и наличии анамнестических указаний на желудочную гиперсекрецию при предыдущих обследованиях). После стихания болевого синдрома и прекращения рвоты переходят к пероральному питанию (обычно с 4 дня от начала лечения). Оно должно быть дробным, 5-6-разовым, но небольшими порциями. Исключают алкоголь, маринады, жареную, жирную и острую пищу, крепкие бульоны, обладающие значительным стимулирующим действием на поджелудочную железу. Рацион питания должен включать повышенное количество белков (стол № 5) в виде нежирных сортов мяса, рыбы, свежего нежирного творога, неострого сыра. Содержание жиров умеренно ограничивают (до 80–70 г в сутки), прежде всего за счет исключения свиного, бараньего жира. При значительной стеаторее содержание жиров в пищевом рационе еще более уменьшают (до 50 г). Ограничивают углеводы, особенно моно– и дисахариды; при развитии сахарного диабета, последние полностью исключают. Пищу дают в теплом виде.
Медикаментозная терапия при обострении хронического панкреатита включает применение холино– и спазмолитических препаратов в сочетании с антацидами, Н2-блокаторами, анальгетиками, ферментными препаратами. Снижение кислотности желудочного содержимого с помощью антацидов (альмагель, фосфалюгель, ремагель, гастерингель, маалокс и др. каждые 2–3 ч) и Н2-блокаторов (ранитидин 300–450 мг в сутки, фамотидин 40–60 мг в сутки внутрь, при тяжелом обострении – парентерально) уменьшает секрецию поджелудочной железы, обеспечивает ей функциональный покой, помогает купировать болевой синдром. При сильной боли показаны ненаркотические анальгетики (анальгин 2 мл 50 %-ного раствора в/в), баралгин (5 мл в/в), в особо тяжелых случаях – наркотические анальгетики (промедол) в соче-тании с холинолитическими и спазмолитическими средствами (платифиллин, гастроцепин, но-шпа, папаверин). В целях обезболивания возможно в/в капельное введение лидокаина (400 мг препарата в 100 мл изотонического раствора хлорида натрия).
С целью дезиинтоксикации в/в вводят гемодез, при возникновении гиповолемии – 10 %-ный раствор альбумина, 5-10 %-ный раствор глюкозы и другие плазмозамещающие жидкости. Антибиотики (полусинтетические пенициллины или цефалоспорины – ампиокс 1,5–2 г в/м 4 раза в сутки, цефоперазон 1–2 г в/м или в/в 2 раза в сутки, цефуроксим 1 г в/м или в/в 3 раза в сутки в течение 7-10 дней и др.) используют главным образом для профилактики инфекционных осложнений панкреатита.
При симптомах внешнесекреторной недостаточности поджелудочной железы проводится пожизненная заместительная терапия полиферментными препаратами (креон, панцитрат, фестал, мезим форте и др. перед каждым приемом пищи). Признаками ее адекватности служат прекращение диареи, метеоризма, болей в животе, исчезновение стеатореи, стабилизация веса. Для улучшения моторики желудочно-кишечного тракта применяют домперидон (мотилиум), или цизаприд (координакс), или дебридат.
После снятия острых явлений и в целях профилактики обострения в дальнейшем рекомендуется курортное лечение в санаториях гастроэнтерологического профиля. Показано применение минеральных вод: Славяновская, Смирновская, Ессентуки № 4, Боржоми. Больным хроническим панкреатитом не показаны виды работ, при которых невозможно соблюдение четкого режима питания; при тяжелом течении заболевания – перевод на инвалидность.
Хирургическое лечение рекомендуется при тяжелых болевых формах хронического панкреатита, рубцово-воспалительном стенозировании общего желчного и (или) панкреатического протока, абсцедировании или развитии кисты железы, рецидивирующих желудочно-кишечных кровотечениях.
Профилактика: отказ от приема алкоголя, своевременное лечение заболеваний, играющих этиологическую роль в возникновении панкреатита, обеспечение рационального питания и режима дня.
ПЕЧЕНОЧНАЯ НЕДОСТАТОЧНОСТЬ – синдром, характеризующийся нарушением одной или многих функций печени вследствие острого или хронического повреждения ее паренхимы. Различают печеночную недостаточность острую и хроническую. При острой печеночной недостаточности печеночная энцефалопатия развивается в течение 8 нед с момента появления первых признаков заболевания печени. Хроническая печеночная недостаточность развивается постепенно, на протяжении нескольких месяцев, однако присоединение провоцирующих факторов (прием алкоголя, пищеводно-желудочное кровотечение из варикозно-расширенных вен пищевода, интеркуррентная инфекция, прием больших доз мочегонных препаратов или одномоментное удаление большого количества асцитической жидкости и др.) может быстро спровоцировать развитие печеночной энцефалопатии.
Этиология. Острая печеночная недостаточность может возникнуть при тяжелых формах вирусного гепатита, отравлениях промышленными (соединения мышьяка, фосфора и др.), растительными (несъедобные грибы) и другими гепатотропными ядами, некоторыми лекарствами (в частности, парацетамолом). В редких случаях причиной острой печеночной недостаточности может стать острая жировая дистрофия печени у беременных (наблюдается в последнем триместре беременности, клинически не отличима от вирусного гепатита), гепатолентикулярная дегенерация, аутоиммунный гепатит, синдром Бадда – Киари. Хроническая печеночная недостаточность возникает при прогрессировании многих хронических заболеваний печени (цирроз, злокачественные опухоли и т. д.).
Патогенез. Печеночная недостаточность объясняется дистрофией и распространенным некробиозом гепатоцитов и (при хронических формах) массивным развитием портокавальных анастомозов, через которые значительная часть крови из воротной вены поступает в полые и затем – в артериальное русло, минуя печень. Это еще более снижает ее участие в дезинтоксикации вредных веществ, всасывающихся в кишечнике, в частности продуктов белкового распада (аммиака и др.). Наиболее страдает антитоксическая функция печени, снижается также ее участие в различных видах обмена (белковом, жировом, углеводном, электролитном, витаминном и др.).
Симптомы: печеночная энцефалопатия (сонливость, спутанность сознания, кома; подробнее – см. в главе «Нервные болезни»), прогрессирующая желтуха, инфекционные осложнения (в том числе сепсис), гипогликемия, почечная недостаточность (повышение уровня креатинина крови), ДВС-синдром, желудочно-кишечное кровотечение (следствие нарушения синтеза факторов свертывания), нарушения водно-электролитного баланса (гипокалиемия, задержка в организме натрия и воды вследствие вторичного гиперальдостеронизма).
Лабораторные исследования показывают значительные отклонения от нормы многих или всех печеночных проб; повышен уровень билирубина, снижено содержание в крови альбумина, протромбина, фибриногена, холестерина. Обычно увеличено содержание в крови аминотрансфераз, особенно аланинаминотрансферазы, часто отмечаются анемия, тромбоцитопения, увеличение СОЭ.
Лечение. Больных с острой печеночной недостаточностью (независимо от ее стадии) немедленно госпитализируют (при вирусном гепатите – в инфекционные больницы, при токсических поражениях печени – в центры отравлений). При остро возникшей печеночной недостаточности и печеночной коме очень важно интенсивными лечебными мероприятиями поддержать жизнь больного в течение критического периода (нескольких дней), рассчитывая на значительную регенераторную способность печени. Проводят лечение основного заболевания, при токсических поражениях печени – мероприятия, направленные на удаление токсического фактора.
В целях дезинтоксикации используют слабительные средства, высокие очистительные клизмы 1–2 раза в сутки. Показано применение лактулозы – синтетического дисахарида, разлагающегося в толстой кишке на молочную, муравьиную и уксусную кислоты. Закисление кишечного содержимого вызывает осмотическую и кислотную диарею, изменяет бактериальную флору в пользу непродуцирующих азот бактерий и снижает концентрацию свободного (неионизированного) аммиака в кишечнике. Лактулозу внутрь назначают по 15–45 мл 2–4 раза в сутки. Препарат противопоказан при подозрении на кишечную непроходимость. Побочные эффекты при передозировке – дегидратация, гипернатриемия, выраженная диарея. Кроме того, лактулоза может назначаться в виде клизм (к 700 мл воды добавляют 300 мл лактулозы, 2–4 клизмы в сутки).
Альтернативой лактулозе при лечении печеночной энцефалопатии может служить антибиотик неомицин, подавляющий продуцирующую аммиак флору кишечника. Препарат может приниматься внутрь (по 1 г каждые 4–6 ч) или в виде клизм (1–2 г в 100–200 мл изотонического раствора хлорида натрия 2–4 раза в сутки). Его побочные эффекты – нефро– и ототоксическое действие. При непереносимости неомицина может быть назначен метронидазол – 250 мг 3 раза в сутки. В тяжелых случаях, при неэффективности монотерапии, проводят комбинированное лечение лактулозой и неомицином.
Ограничивают, а при тяжелой печеночной недостаточности полностью исключают из пищевого рациона белки (мясо, рыба, творог, яйца). Достаточное энергообеспечение достигается внутривенным введением глюкозы; учитывая обычную для этих больных гипокалиемию, в раствор добавляют 3–6 г хлорида калия. Введение изотонического раствора хлорида натрия противопоказано. Проводится витаминотерапия (витамины группы В, аскорбиновая кислота, для борьбы с кровоточивостью – викасол). Для профилактики стессорного гастрита применяют блокаторы Н2-гистаминовых рецепторов (ранитидин, фамотидин). При развитии инфекционных осложнений проводится антибиотикотерапия. При нарастании почечной недостаточности (уровень калия в сыворотке крови свыше 6 ммоль/л, уровень креатинина – свыше 400 ммоль/л) показано проведение гемодиализа.
Категорически запрещают прием спиртных напитков, наркотиков, барбитуратов. Больные хроническими заболеваниями печени, осложнившимися печеночной недостаточностью, нетрудоспособны и нуждаются в переводе на инвалидность.
Профилактика острой печеночной недостаточности сводится к профилактике инфекционных и токсических поражений печени. Профилактика хронической печеночной недостаточности – своевременное лечение заболеваний печени, которые могут послужить ее причиной. Большое значение имеет борьба с алкоголизмом.
ПИЩЕВАЯ АЛЛЕРГИЯ. Этиология, патогенез. Аллергические поражения органов пищеварения бывают пищевого, лекарственного, бактериального и прочего происхождения. Пищевая аллергия наблюдается при употреблении в пищу определенных, нередко сезонных продуктов: некоторых овощей, фруктов, ягод, грибов, редких морских и рыбных продуктов. Аллергия может развиваться также после приема лекарств (и попадания в организм других химических веществ), обладающих высокими сенсибилизирующими свойствами (антибиотики, сульфаниламидные препараты, гидразины, атофан, производные пиразолона и др.). Возможно аллергическое поражение пищеварительной системы при ингаляционном поступлении в организм некоторых аллергенов: пыльцы цветов, пыли и паров некоторых химических веществ. Аллергенами могут быть также белковые антигены, образующиеся при распаде бактерий, паразитирующих в желудочно-кишечном тракте простейших, гельминтов. Аллергические реакции могут провоцироваться психическим состоянием больного, метеорологическими факторами, у женщин обострение симптомов может быть связано с менструальным циклом. Аллергические поражения органов пищеварения могут быть острыми и хроническими, протекать приступообразно с более или менее длительными интервалами полного отсутствия симптомов.
Аллергическое поражение желудочно-кишечного тракта может проявляться регионарными отеками (типа отека Квинке), участками гиперемии слизистой оболочки, петехиями и более крупными геморрагиями; может наблюдаться увеличение лимфатических узлов брюшной полости. Аллергическое поражение печени встречается в виде холестатического, реже паренхиматозного гепатита и жировой дистрофии печени, в особо тяжелых случаях – со множественными массивными некрозами печеночной паренхимы; иногда имеет место гранулематозный гепатит.
Симптомы, характерные для поражения органов пищеварения, довольно редко выходят на первое место в общей клинической картине аллергической реакции.
При поражении пищевода наблюдаются дисфагия и загрудинная боль, обычно при глотании. Поражение желудочно-кишечного тракта проявляется болью в животе, иногда острыми абдоминальными кризами, симулирующими острые хирургические заболевания брюшной полости. Могут наблюдаться желудочно-кишечные кровотечения. Поражение печени проявляется ее увеличением, желтухой, изменением функциональных биохимических показателей (бромсульфалеиновой реакции, аминотрансфераз, белковых фракций, белковых осадочных проб и др.).
Тяжелые случаи – с массивным некрозом печеночной паренхимы – протекают очень остро и заканчиваются печеночной недостаточностью и гибелью больного в несколько дней.
Диагноз устанавливают на основании других аллергических проявлений и четкой связи во многих случаях с определенным фактором, заставляющим заподозрить аллергическую природу заболевания (прием некоторых лекарств, употребление таких продуктов, как клубника, апельсины, икра, крабы и др.). Значительная эозинофилия крови также позволяет предположить аллергическую природу заболевания.
Лечение. Необходимо устранить аллерген, назначить щадящую диету (стол № 1-1а при поражении желудочно-кишечного тракта и № 5а-5 при поражении печени). Проводят десенсибилизирующую терапию. В тяжелых случаях, не поддающихся обычной терапии, назначают глюко-кортикоиды.
ПОНОСЫ – см. Диарея.
ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ СИНДРОМ – симптомокомплекс, характеризующийся повышением давления в бассейне воротной вены, расширением естественных портокавальных анастомозов, асцитом, спленомегалией. Различают внепеченочную форму портальной гипертензии, когда препятствие кровотоку локализовано во внепеченочных отделах воротной вены (подпеченочная гипертензия) или во внеорганных отделах печеночных вен (надпеченочная гипертензия), внутрипеченочную (препятствие кровотоку локализовано в самой печени) и смешанную формы портальной гипертензии. Выделяют также острый и хронический синдромы портальной гипертензии.
Затруднение кровотока в воротной вене приводит к расширению ее анастомозов, при этом при подпечен очной форме портальной гипертензии в основном налаживаются иортоиортальные пути коллатерального кровообращения (в обход места препятствия), а при внутри– и надпеченочной форме – портокавальные (из воротной вены в нижнюю и верхнюю полые): возникает варикозное расширение вен пищевода и желудка, геморроидального сплетения, расширяются поверхностные вены, расходящиеся в разные стороны от пупка. Вследствие застоя крови, повышения давления в воротной вене, а также гипоальбуминемии образуется асцит, увеличивается селезенка.
Симптомы, течение. На ранней стадии протекает бессимптомно, в более поздних случаях характерно появление асцита, расширение геморроидальных и подкожных околопупочных вен (в виде «головы Медузы»), возникновение повторных геморроидальных или профузных пищеводножелудочных кровотечений; последние нередко являются причиной гибели больных.
Диагноз подтверждается (косвенно) при эндоскопическом исследовании пищевода (обнаруживается варикозное расширение его вен). При УЗИ признаками портальной гипертензии служат расширение воротной вены до 13 мм, снижение скорости кровотока по ней либо ретроградный кровоток, а также обнаружение портокавальных коллатералей (параумбиликальная вена, варикозные расширения селезеночной вены и др.). Компьютерная томография также позволяет выявить расширение воротной вены, а иногда и коллатеральных сосудов. Радионуклидное сканирование печени выявляет неоднородное поглощение нуклидов печенью и увеличенное поглощение их селезенкой и костным мозгом. Венография (селезеночная или транспеченочная портография) в необходимых случаях позволяет выявить уровень и (предположительно) причину нарушения портального кровотока. Оценить давление в воротной вене можно с помощью баллонного катетера, проведенного через бедренную или яремную вену в мелкую печеночную вену до упора (при этом создается давление, практически соответствующее портальному).
Течение и прогноз определяются характером заболевания, вызвавшего портальную гипертензию, и присоединением осложнений, наиболее грозным из которых является пищеводно-желудочное кровотечение. Быстрое удаление большого количества асцитической жидкости и назначение больших доз диуретиков больным хроническими заболеваниями печени с синдромом портальной гипертензии может спровоцировать возникновение печеночной комы. При отсутствии хирургического лечения больные, у которых наблюдалось пищеводно-желудочное кровотечение, живут не более 1–1,5 лет.
Лечение направлено на основное заболевание. Проводится терапия асцита (фуросемид, спиронолактон, при недостаточном эффекте – парацентез), кровотечений из варикозно-расширенных вен пищевода (метод выбора – склерозирующая терапия, которая в дальнейшем проводится систематически по мере выявления варикоза). Давление в воротной вене снижают нитраты и бета-адреноблокаторы в небольших дозах. Больным противопоказаны физические нагрузки. При рецидивирующих, несмотря на склеротерапию, кровотечениях показано хирургическое лечение (чаще всего наложение портокавального или спленоренального анастомоза, по показаниям – пересадка печени).
ПОСТГЕПАТИТНЫЙ СИНДРОМ (гипербилирубинемия постгепатитная, желтуха постгепатитная) – симптомокомплекс, характеризующийся остаточной легкой гипербилирубинемией с повышенным содержанием в крови преимущественно непрямого (свободного) билирубина, выявляющийся у части больных, перенесших острый (обычно вирусный) гепатит, без признаков других функциональных и морфологических изменений печени. У больных иногда отмечаются общая слабость, быстрая утомляемость, легкие диспептические явления. Печень обычно нормальных размеров или слегка увеличена, мягкая, безболезненная.
На протяжении нескольких недель или месяцев отмечается полная регрессия симптомов.
Лечение. Больные в стационарном лечении не нуждаются. Диета: исключение острых и жирных блюд, алкогольных напитков. Рекомендуются легкие желчегонные средства (экстракт кукурузных рылец, минеральная вода типа Ессентуки) курсами, витаминотерапия. Тепловые и электрические процедуры на область печени не рекомендуются. Трудоспособность больных сохранена, но необходимо ограничение физических и нервных перегрузок.
РАЗДРАЖЕННОЙ ТОЛСТОЙ КИШКИ СИНДРОМ (синдром раздраженного кишечника, дискинезия толстой кишки, слизистая колика, хронический спастический колит) – расстройства моторной и секреторной функции кишечника при отсутствии органических изменений органов. Заболевание чаще встречается в возрасте 20–40 лет у женщин.
Этиология, патогенез. В развитии заболевания играют роль нервно-психические факторы (тип личности, психический статус – тревога, депрессия и др.), особенности питания (отказ от полноценного завтрака, поспешность при приеме пищи, недостаточное количество клетчатки в рационе), гинекологические заболевания (дисменорея) и др. Определенное значение в поддержании расстройств функции кишечника имеет сопутствующий дисбактериоз.
Симптомы, течение. Характерны схваткообразные или тупые, распирающие боли в животе (как правило, усиливаются после приема пищи, перед актом дефекации и уменьшаются после дефекации), запоры (стул реже 3 раз в нед), поносы (жидкий стул чаще чем 3 раза в день, светлый, нередко с примесью слизи), возможно чередование запоров и поносов. Нередко наблюдаются «овечий кал», метеоризм, ощущение вздутия живота, его переполнения, урчание и другие диспептические расстройства. Отличительным признаком синдрома раздраженной толстой кишки служит отсутствие каких-либо жалоб в ночное время. Часто наблюдаются признаки вегетативной дистонии: головная боль, парестезии, сердцебиение, ощущение комка в горле, чувство неполного вдоха, учащенное мочеиспускание и др. При осмотре может выявляться спастически сокращенная болезненная нисходящая (иногда восходящая и ободочная) толстая кишка.
При эндоскопическом исследовании изменений толстой кишки не обнаруживают, однако инсуффляция воздуха бывает болезненной. При рентгенологическом исследовании могут выявляться диффузное или сегментарное сужение просвета кишки, неравномерный пассаж взвеси сульфата бария по кишке.
Дополнительные исследования необходимы для исключения органических заболеваний органов пищеварения (опухоли кишечника, неспецифический язвенный колит, болезнь Крона, гельминтозы, полипоз, дивертикулез, туберкулез). Примесь крови в кале, выраженное похудание, анемия, повышение СОЭ делают диагноз синдрома раздраженной толстой кишки маловероятным.
Течение заболевание волнообразное, с периодами ремиссий и рецидивами, но не прогрессирующее.
Лечение: диетотерапия, психотерапия. Проводится симптоматическая терапия запоров (увеличение клетчатки в рационе, достаточное количество жидкости, лактулоза 30–60 мл в сутки, или гуталакс 10–12 капель перед сном, или форлакс 2 пакетика в сутки в комбинации с бисакодилом 13 драже в сутки перед сном), поносов (смекта 1 пакет 3 раза в сутки после еды, лоперамид 2 мг 2 раза в сутки и более), спастических болей – спазмолитики, холиноблокаторы (но-шпа, гастроцепин, бускопан). При снижении тонуса кишки используют домперидон (мотилиум по 10 мг 3 раза в сутки), цизаприд (координакс по 20 мг 2 раза в сутки), дебридат (по 1 таблетке 3 раза в сутки). Показано лечение сопутствующего дисбактериоза (антимикробные средства – эрсефурил, интетрикс, метронидазол, бактериальные средства – бифидобактерин, лактобактерин и др., а также хилак форте). По показаниям применяют психотропные средства (трициклические антидепрессанты – амитриптилин и др., селективные ингибиторы обратного захвата серотонина – флуоксетин и др.).
СКОРБУТ – см. главу «Болезни витаминной недостаточности» (недостаточность витамина С).
СПРУ НЕТРОПИЧЕСКАЯ – см. Энтеропатия кишечная (глютеновая).
СПРУ ТРОПИЧЕСКАЯ (тропическая диарея) – тяжелое хроническое заболевание, характеризующееся воспалительно-атрофическими изменениями слизистой оболочки, упорными поносами, глосситом и нормохромной анемией; распространено в странах с тропическим и субтропическим климатом, очень редко среди жителей средней полосы. Чаще болеют женщины, особенно в период беременности, и лица пожилого возраста.
Этиология и патогенез изучены недостаточно. Развитию заболевания предрасполагают неполноценное питание (преимущественно растительной пищей), недостаточное употребление в пищу белка, дефицит витаминов, тяжелые инфекционные заболевания, предшествующие бактериальные и протозойные энтероколиты, ослабление и истощение организма, эндокринные дисфункции (в период лактации у женщин, угасание половой функции), нервно-психические перенапряжения. Недостаток в пище витаминов, усугубленный нарушением их всасывания в кишечнике, способствует возникновению дистрофических изменений во внутренних органах, а дефицит фолиевой кислоты и витамина B12 – развитию анемии. Эффективность антибиотикотерапии свидетельствует в пользу микробной природы заболевания.
Симптомы, течение. Заболевание начинается с неопределенных диспепсических жалоб, ощущений урчания, переливания в животе, метеоризма, чувства жжения в языке. Затем появляется упорный понос; испражнения жидкие, пенистые, белесоватого цвета (от большого содержания неусвоенного жира). При вовлечении в процесс дистальных отделов толстой кишки присоединяются тенезмы; испражнения содержат примесь слизи и гноя. Развивается мальабсорбция, больные худеют, возникают признаки полигиповитаминоза. Кожа сухая, гиперпигментирована, живот резко вздут, перкуторно над ним определяется громкий тимпанический звук. Характерен эрозивноязвенный глоссит; постепенно сосочки языка атрофируются, язык становится гладким, блестящим («лаковый язык»).
Лабораторные исследования выявляют анемию (нормо– или гиперхромную), гипопротеинемию (проявление мальабсорбции), повышение уровня трансаминаз. Кал имеет кислую реакцию, в нем определяются большое количество капель непереваренного жира, кристаллы жирных кислот, мыл, мышечных волокон, непереваренной клетчатки. При рентгенологическом исследовании – сглаженность рельефа слизистой оболочки и резко ускоренный пассаж контрастной взвеси по кишечнику; иногда определяются горизонтальные уровни скоплений жидкости и газа в кишечных петлях.
Эндоскопическое исследование и биопсия слизистой оболочки желудка, двенадцатиперстной, толстой кишки подтверждают наличие воспалительноатрофических изменений в органах пищеварения.
Дифференциальный диагноз проводят с амебиазом, дизентерией, банальными формами энтероколита. Гиперхромная анемия в ряде случаев может вызвать трудности в дифференциальной диагностике с B12-дефицитной анемией; однако наличие диареи, данные биопсии слизистых оболочек пищеварительного тракта позволяют поставить правильный диагноз.
Лечение: в период обострения заболевания и выраженных проявлений синдрома недостаточности питания проводят в стационаре. Назначают диету с некоторым ограничением жиров (свиного, бараньего) и углеводов, повышенным содержанием белка (140–160 г) и витаминов. Пища должна быть хорошо механически обработана (протертая, провернутая через мясорубку и т. д.), приготовлена на пару. Питание дробное 4–5 раз в день. Применяют антибиотики широкого спектра действия (тетрациклин 250 мг 4 раза в сутки или доксициклин 100 мг 2 раза в сутки в течение 4 нед), витамин B12, фолиевую кислоту.
ТУБЕРКУЛЕЗ ПИЩЕВАРИТЕЛЬНОЙ СИСТЕМЫ. Туберкулез пищевода представляет одну из редких локализаций этого заболевания и в большинстве случаев наблюдается у лиц с далеко зашедшими его легочными формами незадолго до смерти.
Этиология, патогенез. Микобактерии туберкулеза попадают в пищевод при заглатывании инфицированной мокроты, при активном туберкулезе гортани, надгортанника и глотки, реже лимфо– или гематогенным путем, а также в результате непосредственного перехода туберкулезного процесса с окружающих органов: бифуркационных лимфатических узлов, позвоночника, щитовидной железы, гортани, глотки. Туберкулезные язвы возникают в результате казеозного распада туберкулезных бугорков. Встречаются также милиарная и стенозирующая формы туберкулезного поражения пищевода.
Симптомы, течение. Заболевание может протекать бессимптомно, однако чаще его симптомы затушевываются более выраженными проявлениями туберкулезного поражения других органов (прежде всего легких и гортани) и тяжелым общим состоянием больного.
Наиболее ярким симптомом является дисфагия, которая при наличии изъязвлений слизистой оболочки может сопровождаться резкой болью.
Рентгенологическое исследование выявляет крупные туберкулезные язвы и рубцовое сужение просвета пищевода.
Диагноз облегчает эзофагоскопия, биопсия, бактериологическое исследование материала, полученного из язвы.
Лечение проводят в специализированных противотуберкулезных больницах. При туберкулезных язвах пищевода внутрь дополнительно назначают препараты висмута, местные анестетики. При рубцовом сужении пищевода проводят бужирование; в ряде случаев для поддержания питания больного временно накладывают гастростому.
Прогноз определяется выраженностью туберкулезных изменений в легких и других органах. Осложнения: фистулезные сообщения пищевода с трахеей, бронхами, плеврой, гнойный медиастенит; прорыв казеозной полости в крупный сосуд грозит профузным кровотечением. При заживлении туберкулезных язв образуются стриктуры пищевода, нарушается его проходимость: в результате спаечного процесса между бифуркационными лимфатическими узлами и стенкой пищевода образуются его тракционные дивертикулы.
Туберкулез желудка встречается очень редко, обычно в терминальной фазе легочного туберкулеза. В последнее время, однако, у больных туберкулезом легких в результате длительного лечения противотуберкулезными препаратами обнаруживаются «лекарственные гастриты».
Симптомы, течение. Заболевание может протекать бессимптомно или же сопровождаться болью в эпигастральной области, отрыжкой, рвотой, резким снижением аппетита; как правило, наблюдаются общее истощение, лихорадка, повышенная потливость.
Диагноз туберкулеза желудка подтверждается рентгенологическим исследованием и гастрофиброскопией. Поэтому особую ценность имеет прицельная биопсия. При исследовании желудочного сока часто выявляется ахилия, в желудочном содержимом (чаще в промывных водах) обнаруживают микобактерии туберкулеза.
Течение и прогноз в большинстве случаев определяются тяжестью легочной и других локализаций туберкулеза. Редкими осложнениями являются перфорация туберкулезной язвы желудка, желудочное кровотечение, рубцовый стеноз привратника.
Лечение проводят в специализированных туберкулезных стационарах. Больным с туберкулезным поражением желудка назначают щадящую диету (стол № la-1) и симптоматические средства (как при лечении язвенной болезни желудка и двенадцатиперстной кишки).
Туберкулез поджелудочной железы встречается очень редко. Даже у больных активным туберкулезом легких он выявляется лишь в 0,52 % случаев.
Симптомы, течение. Больные предъявляют жалобы на отрыжку, понижение аппетита, тошноту, боль в верхнем левом квадранте живота, нередко опоясывающего характера, поносы, усиленную жажду (при нарушении инкреторной функции поджелудочной железы), прогрессирующее истощение, повышенную потливость, недомогание, лихорадку. Кожа иногда приобретает темноватую окраску, как при аддисоновой болезни. При пальпации поджелудочной железы отмечается болезненность в месте ее расположения.
Диагноз. Для подтверждения диагноза проводят эхографию, ретроградную панкреатохолангиографию, вирсунгографию, сканирование поджелудочной железы, исследование ее внешней и внутренней секреции (характерна недостаточность функции). Дифференциальный диагноз проводят с неспецифическими панкреатитами, злокачественными и доброкачественными опухолями поджелудочной железы.
Лечение осуществляют в специализированых противотуберкулезных клиниках. Назначают также дробное 5-6-разовое питание, щадящую диету с ограниченным содержанием жиров, исключением острых продуктов и повышенным содержанием белка. При признаках внешнесекреторной недостаточности поджелудочной железы назначают ферментные препараты, как при хроническом панкреатите.
Туберкулез печени сопровождает туберкулез кишечника в 79–99 % случаев. Туберкулезные микобактерии проникают в печень гематогенным или лимфогенным путем, возможно также распространение процесса по желчным ходам. Чаще всего наблюдаются милиарная форма или множественные туберкуломы печени с казеозным распадом в центре. Встречаются также неспецифические изменения в печени при туберкулезе легких в виде реактивного гепатита, жировой дистрофии, амилоидоза или лекарственного гепатита (при длительном применении туберкулостатических средств).
Симптомы, течение. Анорексия, общее недомогание, слабость, повышенная потливость, субфебрилитет, боль в правом подреберье. Печень увеличена, край ее плотный, в ряде случаев поверхность неровная (при транулематозной форме) или удается прощупать узел на ее поверхности (туберкулему). Нередко увеличена селезенка. Заподозрить туберкулезное поражение печени можно в том случае, если у больного легочным туберкулезом обнаруживается увеличение печени, отмечается боль в правом подреберье.
Диагноз подтверждается лапароскопией, пункционной биопсией печени, эхографией и сканированием.
Лечение. К противотуберкулезным средствам дополнительно назначают диету № 5а и 5, при резком нарушении функции печени вводят сирепар.
Туберкулез кишечника обнаруживают у 60–90 % лиц, умерших от туберкулеза. Микобактерии туберкулеза попадают в кишечник чаще всего гематогенным или лимфогенным путем либо при заглатывании инфицированной мокроты, слюны и слизи, особенно при туберкулезном поражении гортани и глотки. Чаще поражаются дистальные отделы подвздошной и слепой кишки, аппендикс, реже – восходящая, поперечная, ободочная кишка.
Симптомы, течение. Вначале туберкулезное поражение кишечника может протекать бессимптомно или с общими симптомами – нарушением аппетита, тошнотой и тяжестью в животе после еды, слабостью, недомоганием, субфебрильной лихорадкой, повышенной потливостью, вздутием кишечника. Неустойчивым стулом, малохарактерными болями в животе. В дальнейшем боль становится более постоянной, локализуется чаще в правой подвздошной области и около пупка, при пальпации определяются плотные болезненные утолщения стенок слепой кишки и конечной части подвздошной кишки. При поражении прямой кишки наблюдаются тенезмы и ложные позывы. При туберкулезном мезадените боль локализуется в глубине живота несколько влево и книзу от пупка или по ходу брыжейки тонкой кишки. Во время рентгенологического исследования кишечника обнаруживают изъязвления слизистой оболочки, дискинетические явления, рубцовые стенозы, иногда дефекты наполнения слепой кишки. Поражение толстой кишки может быть уточнено при колоноскопии. При исследовании кала отмечают положительные реакции на скрытую кровь и пробу ребунале на растворимый белок. В крови – гипохромная анемия, лейкопения с относительным лимфоцитозом, при обострении – нейтрофильный лейкоцитоз, увеличение СОЭ.
Течение туберкулеза кишечника при отсутствии соответствующего лечения обычно прогрессирующее. Прогноз в значительной степени определяется тяжестью туберкулезного поражения легких и других органов. Осложнения: сужение просвета кишки, перфорация туберкулезных язв, перитонит и кишечное кровотечение.
Дифференциальный диагноз проводят с неспецифическим энтероколитом, болезнью Крона, неспецифическим язвенным колитом, раком слепой кишки.
Лечение. В период обострения назначают пищу в протертом виде, дробно (4–5 раз в день), богатую белками, легко усвояемыми жирами и витаминами. При нарушении ферментативных процессов – препараты пищеварительных ферментов (панцитрат, панзинорм, фестал и др.), поливитамины, при железодефицитной анемии – препараты железа парентерально.
УИППЛА БОЛЕЗНЬ – см. Кишечная липодистрофия.
ХОЛЕЦИСТИТ ОСТРЫЙ – см. главу «Хирургические болезни».
ХОЛЕЦИСТИТ ХРОНИЧЕСКИЙ. Клиницисты используют этот диагноз для обозначения хронического воспалительного поражения желчного пузыря, сопровождающегося характерной симптоматикой, включая рецидивирующую желчную колику. Морфологически хронический холецистит диагностируется при обнаружении толстостенного, фиброзного, сокращенного желчного пузыря с изъязвлениями и Рубцовыми изменениями его слизистой оболочки. При этом четкой взаимосвязи между клиническими и морфологическими признаками не выявлено, однако и те и другие коррелируют с наличием желчнокаменной болезни.
Этиология, патогенез. Хроническое воспаление стенки желчного пузыря в большинстве случаев связано с желчнокаменной болезнью или ее осложнениями (см. главу «Хирургические болезни»). Причиной хронического бескаменного холецистита могут быть паразитарные инфекции (лямблиоз и др.), бактериальная флора (кишечная палочка, стрепто-, стафилококки и др.), реже заболевание развивается в результате сепсиса, травмы, ожогов.
Проникновение микробной флоры в желчный пузырь происходит контактным (из кишечника), гематогенным или лимфогенным путем. Предрасполагающим фактором возникновения бактериального холецистита является застой желчи в желчном пузыре вследствие желчнокаменной болезни, сдавления и перегибов желчных протоков, дискинезии желчного пузыря и желчных путей. Застою желчи в желчном пузыре также способствуют опущение внутренних органов, беременность, малоподвижный образ жизни, редкие приемы пищи и др.
Непосредственным толчком к вспышке воспалительного процесса в желчном пузыре часто являются переедание, особенно прием очень жирной и острой пищи, алкогольных напитков, острый воспалительный процесс в другом органе (ангина, пневмония, аднексит и т. д.).
Симптомы, течение. Хронический калькулезный холецистит чаще проявляется рецидивирующими приступами желчной колики, реже – постоянной тупой болью в правом подреберье. Для бескаменного холецистита более характерна тупая, ноющая боль в области правого подреберья постоянного характера или возникающая через 1–3 ч после приема обильной и особенно жирной и жареной пищи. Нередки диспепсические явления: ощущение горечи и металлического вкуса во рту, отрыжка воздухом, тошнота, метеоризм, нарушение дефекации (нередко чередование запора и поноса), а также раздражительность, бессонница; желтуха не характерна. В целом, однако, клиническая картина не позволяет определенно дифференцировать калькулезные и бескаменные поражения желчного пузыря.
При пальпации живота, как правило, определяются чувствительность, а иногда и выраженная болезненность в проекции желчного пузыря на переднюю брюшную стенку и легкое мышечное сопротивление брюшной стенки (резистентность), положительные симптомы Мюсси – Георгиевского, Ортнера, Образцова – Мерфи. При осложнениях хронического холецистита (хронический гепатит, холангит) печень несколько увеличена с плотноватым и болезненным при пальпации краем. Желчный пузырь в большинстве случаев не пальпируется, так как обычно он сморщен вследствие хронического рубцово-склерозирующего процесса.
При обострениях наблюдаются нейтрофильный лейкоцитоз, повышение СОЭ и температурная реакция. Признаки хронического холецистита определяются при ультразвуковом исследовании и компьютерной томографии в виде утолщения стенок пузыря, деформации его и т. д. При холецистографии отмечается изменение формы желчного пузыря, часто его изображение получается нечетким вследствие нарушения концентрационной способности слизистой оболочки, иногда в нем обнаруживаются камни. После приема раздражителя – холецистокинетика (обычно два яичных желтка) – отмечается недостаточное сокращение желчного пузыря. В диагностике бескаменного холецистита важную роль играет дуоденальное зондирование, бактериологическое исследование желчи (особенно повторное) позволяет определить возбудителя холецистита.
Течение хронического бескаменного холецистита в большинстве случаев длительное, характеризуется чередованием периодов ремиссии и обострений. Прогноз в большинстве случаев благоприятный. Ухудшение общего состояния больных и временная потеря их трудоспособности – лишь на периоды обострений болезни. Возможно присоединение холангита, гепатита, панкреатита. Часто воспалительный процесс является «толчком» к образованию камней в желчном пузыре.
Хронический холецистит дифференцируют с язвенной болезнью, хроническим панкреатитом, синдромом раздраженной толстой кишки.
Лечение хронического калькулезного холецистита – это лечение желчнокаменной болезни. При обострениях хронического бескаменного холецистита больных госпитализируют в хирургические или терапевтические стационары и лечение проводят, как при остром холецистите. В легких случаях возможно амбулаторное лечение. Назначают постельный режим, диетическое питание (диета № 5а) с приемом пищи 4–6 раз в день, противопаразитарные, антибактериальные средства (эритромицин, доксициклин, ципрофлоксацин, цефуроксим акстеил, бисептол и др.). Для устранения дискинезии желчных путей, спастических болей, улучшения желчеоттока используют спазмолитические и холинолитические средства (папаверина гидрохлорид, но-шпа, метацин и др.), а при нерезких обострениях и в период стихания воспалительных явлений – слепые (беззондовые) тюбажи с сульфатом магния или теплой минеральной водой (Ессентуки № 17 и др.). При выраженной боли применяют баралгин, анальгин в/м, паранефральные новокаиновые блокады, вводят 30–50 мл 0,25-0,5 %-ного раствора новокаина внутрикожно над областью максимальной болезненности или же назначают электрофорез с новокаином на эту зону. Для улучшения оттока желчи из желчного пузыря как в период обострения, так и в период ремиссии широко применяют желчегонные средства: аллохол (по 2 таблетки 3 раза в сутки), холензим (по 1 таблетке 3 раза в сутки), фламин (по 1 таблетке 3 раза в сутки) и т. п., курс лечения – 3–4 нед. По показаниям используют ферментные препараты (креон, или дигестал, или фестал, или панзинорм и т. п.), средства, нормализующие моторику желудочно-кишечного тракта (цизаприд, домперидон, дебридат и др.), антациды (фосфалюгель, маалокс и др.). В период стихания воспалительного процесса можно назначить тепловые физиотерапевтические процедуры на область правого подреберья (УВЧ, индуктотермия и др.).
Проводят лечение минеральной водой (Ессентуки № 4 и № 17, Славяновская, Смирновская и др.), а также сульфатом магния (по 1 ст. л. 25 %-ного раствора 2 раза в день) или карловарской солью (по 1 ч. л. в стакане теплой воды 3 раза в день). После стихания обострения холецистита и для профилактики последующих обострений показано санаторнокурортное лечение (Ессентуки, Железноводск, Трускавец, Моршин и др.). Хирургическое лечение хронического бескаменного холецистита обычно не проводится.
Профилактика хронического холецистита заключается в соблюдении режима питания, занятиях спортом, физкультурой, профилактике ожирения, лечении очаговой инфекции. Больные нуждаются в диспансерном наблюдении.
ЦЕЛИАКИЯ (глютеновая энтеропатия, спру европейская, спру нетропическая, идиопатическая стеаторея) – редкое заболевание (ферментопатия) кишечника, характеризующееся атрофией слизистой оболочки тонкой кишки в ответ на введение глютена – полипептида, содержащегося в некоторых злаковых (пшенице, ржи, ячмене, овсе).
Этиология, патогенез. Заболевание обусловлено врожденным отсутствием или пониженной выработкой кишечной стенкой ферментов, расщепляющих глютен. Отсутствие (или относительная недостаточность) выработки этой пептидазы особенно проявляется при нарушениях питания, преобладании в пище злаковых, содержащих глютен, при кишечных инфекциях, во время беременности. Продукты неполного переваривания глютена (глиадин и др.) токсически действуют на кишечную стенку и стимулируют развитие аутоиммунных реакций, вызывая атрофию слизистой оболочки тонкой кишки и развитие синдрома мальабсорбции.
Симптомы, течение. В подавляющем большинстве случаев первые симптомы появляются в детстве. Характерен частый (до 10 раз в день) кашицеобразный стул с сероватым оттенком после употреблении в пищу продуктов, изготовленных из пшеницы, ржи и ячменя, увеличение живота за счет снижения тонуса кишечника, снижение массы тела. В запущенных случаях развивается хронический энтерит с синдромом недостаточности всасывания, безбелковыми отеками, остеопорозом, железо дефицитной анемией, полигиповитаминозами, нарушениями электролитного баланса и др. Возможно развитие дисбактериоза. У детей при отсутствии лечения наблюдается задержка психомоторного развития.
При копрологическом исследовании определяется стеаторея, при эндоскопии выявляется поперечная исчерченность складок тонкой кишки, при гистологическом исследовании – признаки ее атрофии. Известную помощь в дифференциальной диагностике могут оказывать выявление антител к глютену, наличие признаков заболевания с раннего детства, обострение симптомов заболевания при значительном добавлении к пищевому рациону продуктов из пшеницы, ржи, ячменя, овса, а также обратное развитие симптомов болезни при переводе больного на безглютеновую диету (глютен отсутствует во всех продуктах животного происхождения, в кукурузе, рисе, соевых бобах, картофеле, овощах, фруктах, ягодах и других продуктах).
Лечение: пожизненное соблюдение аглютеновой диеты (исключение из рациона хлеба, кондитерских, макаронных изделий, колбас, сосисок и других продуктов, содержащих злаки). При неэффективности аглютеновой диеты в течение 3 мес, тяжелом течении заболевания (появлении безбелковых отеков) применяют глюкокортикоиды (преднизолон 20 мг в сутки в течение 7 дней). При развитии дисбактериоза проводят терапию антимикробными средствами (фуразалидон, интетрикс и др.), затем – бактериальными препаратами (бифидумбактерин, бификол и др.). По показаниям применяют полиферментные препараты (креон, панцитрат, фестал и др.). Для уменьшения кишечной гиперсекреции используют вяжущие, обволакивающие, адсорбирующие вещества. По показаниям проводится заместительная терапия белковой, витаминной недостаточности, коррекция нарушений водно-электролитного обмена.
ЦИНГА – см. главу «Болезни витаминной недостаточности» (недостаточность витамина С).
ЦИРРОЗ ПЕЧЕНИ – хроническое прогрессирующее заболевание, характеризующееся нарушением структуры органа в связи с развитием фиброза и паренхиматозных узлов.
Этиология. Цирроз может развиться в исходе вирусного гепатита В и С; аутоиммунного гепатита, вследствие хронического алкоголизма, воздействия токсических веществ и лекарственных средств (метотрексат, амиодарон); на почве холестаза при длительном сдавлении или закупорке желчных протоков; метаболических расстройств (гемохроматоз, гепатоцеребральная дистрофия, недостаточность оц-антитрипсина, врожденный тирозиноз), венозного застоя (хроническая правожелудочковая недостаточность, синдром Бадда – Киари). При неустановленной этиологии говорят о криптогенном циррозе печени.
Патогенез. Непосредственное поражение печеночной ткани инфекционным или токсическим фактором происходит при длительном воздействии иммунологических нарушений, проявляющихся в приобретении белками печени антигенных свойств и выработке к ним антител. В основе первичного (холангиолитического) билиарного цирроза лежит длительный внутрипеченочный холестаз. При вторичном билиарном циррозе печени имеет значение нарушение оттока желчи по внепеченочным желчным протокам, холангит, выработка антител к белкам эпителиальных клеток желчных канальцев. При всех видах цирроза развиваются дистрофия и некробиоз гепатоцитов, наблюдаются выраженная мезенхимальная реакция, разрастание соединительной ткани, вследствие чего нарушаются дольчатая структура печени, внутрипеченочный кровоток, лимфоток, отток желчи. Нарушение внутрипеченочного кровотока вызывает гипоксию и усиливает дистрофические изменения в паренхиме печени. Характерна также узловая регенерация гепатоцитов. По степени функциональных нарушений различают цирроз компенсированный и декомпенсированный, по морфологическим признакам мелкоузловой, крупноузловой и смешанный.
Симптомы, течение. Наряду с увеличением или уменьшением размеров печени характерны ее уплотнение, сопутствующая спленомегалия, симптомы портальной гипертензии (асцит, варикозное расширение вен гемморроидального сплетения, пищевода и кардиального отдела желудка, а также подкожных околопупочных вен, расходящихся в разные стороны от пупочного кольца – «голова Медузы»), желтуха. Нередко наблюдается тупая или ноющая боль в области печени, усиливающаяся после погрешностей в диете и физической работы; диспепсические явления; кожный зуд, обусловленный задержкой выделения и накоплением в тканях желчных кислот. При осмотре больного выявляются характерные для цирроза «печеночные знаки»: телеангиэктазии («звездочки», «паучки») на коже верхней половины туловища, эритема ладоней («печеночные ладони»), «лаковый язык» малинового цвета, «печеночный язык». Нередки ксантелазмы, ксантомы, пальцы в виде барабанных палочек, у мужчин – гинекомастия, нарушение роста волос на подбородке и в подмышечных впадинах.
Часто выявляют анемию (нормохромную, иногда – макроцитарную, после кровотечения из варикозно-расширенных вен – гипохромную), лейко– и тромбоцитопению (признаки гиперспленизма), повышение СОЭ, удлинение протромбинового времени. При биохимическом исследовании наблюдаются гипербилирубинемия, повышение уровня щелочной фосфатазы (особенно при билиарном циррозе), трансаминаз (чаще при алкогольном гепатите с исходом в цирроз). Отмечают гипергаммаглобулинемию, изменение показателей белковых и осадочных проб (сулемовой, тимоловой и др.). При желтухе в моче обнаруживают уробилин, билирубин, содержание стеркобилина в кале уменьшено.
Диагноз устанавливают на основании клинической картины, данных лабораторных исследований (которые, однако, слабо коррелируют с гистологической картиной). Ультразвуковое исследование выявляет повышенную эхогенность ткани печени с появлением хаотически расположенных акустически плотных участков. При радионуклидном сканировании характерно снижение накопления радионуклидов в печени и их повышенное нерегулярное поглощение селезенкой и костным мозгом. Эндоскопическое исследование позволяет выявить варикозное расширение вен пищевода. Диагноз верифицируют с помощью лапароскопии с биопсией ткани печени и пункционной биопсии, выявляющей узлы с окружающей их фиброзной тканью.
Компенсированный цирроз характеризуется удовлетворительным самочувствием больных и при наличии характерных для цирроза клиниколабораторно-морфологических изменений – сохранением основных функций печени. Обычно у этих больных все же наблюдаются повышенная утомляемость, снижение работоспособности, метеоризм. Дскомпенсированный цирроз печени проявляется признаками печеночной недостаточности (печеночной энцефалопатией, кровотечениями, внепеченочными кожными знаками и др.), асцитом, портальной гипертензией, лабораторными изменениями, свидетельствующими о снижении функциональной способности печени. Для оценки степени декомпенсации цирроза печени используется классификация Чайлда (табл. 11).
Прогноз неблагоприятный при декомпенсированном циррозе, несколько лучше (в отношении продолжительности жизни и длительности сохранения работоспособности) – при компенсированном. При вторичном билиарном циррозе прогноз во многом определяется причинами, вызвавшими закупорку желчного протока (опухоль, камень и др.) и возможностью их устранения. Ухудшается прогноз больных с кровотечениями из варикознорасширенных вен пищевода и желудка в анамнезе; такие больные нередко погибают от повторного кровотечения. При декомпенсированном циррозе печени повышен риск рака печени, возможно развитие спонтанного перитонита.
Таблица 11. Классификация цирроза печени (по Чайлду)
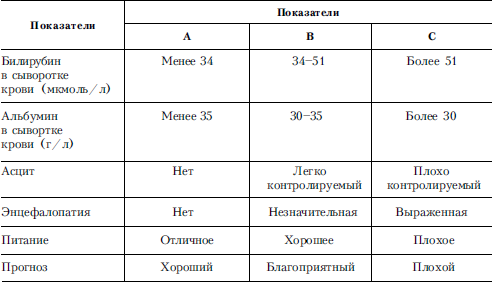
Лечение
Терапия цирроза печени во многом зависит от его этиологии. При циррозе печени, развившемся в исходе аутоиммунного гепатита, показано лечение преднизолоном (поддерживающая доза – 5-10 мг), при недостаточном эффекте и отсутствии противопоказаний (гранулоцитопении и тромобоцитопении) – азатиоприном (25 мг в сутки); при циррозе печени, развившемся на фоне хронического вирусного гепатита В или С (при наличии признаков репликации вируса, высокой активности гепатита) – интерферонотерапия; при первичном билиарном циррозе – урсодезоксихолевая кислота (750 мг в сутки постоянно), холестирамин, связывающий желчные кислоты в кишечнике и препятствующий их обратному всасыванию (4-12 г в сутки в зависимости от выраженности кожного зуда); при вторичном билиарном циррозе – хирургическое лечение с целью устранения закупорки или сдавления общего желчного протока; при гемохроматозе – дефероксамин (десферал) 500-1000 мг в сутки в/м и кровопускания; при гепато-лентикулярной дегенерации – постоянный прием пенцилламина в индиви-дуально подобранной дозе (подробнее – см. соответствующие разделы).
При остром кровотечении из варикозно-расширенных вен пищевода необходимы срочная госпитализация в хирургический стационар, голод, введение сосудосуживающих средств (вазопрессин, соматостатин и др.), остановка кровотечения с помощью механической баллонной тампонады или эндоскопической склеротерапии (паравазального или интравазального введения склерозантов).
При компенсированном циррозе проводят диспансерное наблюдение за больными (не реже 2 раз в год), показаны диета № 5, регулярное 4– 5-разовое питание, ограничение физических нагрузок (особенно при портальной гипертензии), прием полиферментных препаратов (креон, панцитрат, мезим форте и др.) курсами по 2–3 нед. Запрещаются алкогольные напитки. При портальном циррозе со значительным варикозным расширением вен пищевода или упорным, не поддающимся лечению асцитом в целях разгрузки портальной системы профилактически накладывают хирургическим путем портокавальный или спленоренальный анастомоз (или производят другие типы операций). Больные циррозом печени ограниченно трудоспособны или нетрудоспособны и нуждаются в переводе на инвалидность.
Профилактика: рациональное питание, действенный санитарнотехнический надзор на производствах, связанных с гепатотропными ядами, борьба с алкоголизмом. Своевременное лечение хронических гепатитов и заболеваний, протекающих с холестазом.
ЦИРРОЗ ПЕЧЕНИ ПИГМЕНТНЫЙ – см. Гемохроматоз.
ЭЗОФАГИТ – группа заболеваний с острым, подострым или хроническим течением, характеризующихся воспалением слизистой оболочки пищевода.
Этиология. Самой частой причиной эзофагита является заброс желудочного сока в пищевод вследствие недостаточности кардии – рефлюксэзофагит (см. Гастроэзофагеальная рефлюксная болезнь). Коррозивные эзофагиты возникают вследствие раздражения слизистой оболочки пищевода химическими веществами (крепкие кислоты, щелочи). Лекарственное поражение пищевода может быть вызвано приемом таблетированных форм тетрациклинов, хинидина, нестероидных противовоспалительных средств, сульфата железа и др. Риск возникновения лекарственного эзофагита выше у лиц со структурными аномалиями пищевода (при стриктурах, опухолях пищевода, грыже пищеводного отверстия диафрагмы, при сдавлении пищевода левым предсердием, дугой аорты); его развитию способствуют горизонтальное положение пациента, запивание таблеток малым количеством воды, прием алкоголя. Инфекционно-воспалительные заболевания пищевода развиваются главным образом у пациентов с иммунодефицитными состояниями, могут вызываться грибками (кандидозные эзофагиты); вирусами герпеса, иммунодефицита человека, цитамегаловирусами; редко – бактериями.
Патогенез: в большинстве случаев – непосредственное раздражающее воздействие на слизистую оболочку пищевода, в том числе пептическое (при недостаточности кардии и рефлюкс-эзофагите).
Симптомы, течение. Эзофагиты проявляются дисфагией (ощущением замедления или препятствия при прохождении пищи по пищеводу), одинофагией (болью при прохождении пищи), болью за грудиной (может потребоваться проведение дифференциального диагноза со стенокардией), изжогой (жжение за грудиной при контакте слизистой оболочки пищевода с кислым желудочным содержимым – характерный признак рефлюксэзофагита). При геморрагическом эзофагите могут быть рвота алой кровью и мелена.
Осложнения: при коррозивном эзофагите возможны перфорация стенки пищевода, медиастинит или перитонит; при геморрагическом и эрозивном эзофагите – пищеводные кровотечения. Тяжелые эзофагиты могут привести к стриктуре и рубцовому укорочению пищевода; последнее способствует образованию или увеличению имеющейся аксиальной грыжи пищеводного отверстия диафрагмы.
Важнейшую роль в диагностике эзофагита играет эндоскопическое исследование. При коррозивном эзофагите на фоне гиперемированной слизистой оболочки выявляют кровоточащие эррозированные и изъязвленные участки различной формы (эндоскопическое исследование выполняют с особой осторожностью). Для лекарственного поражения пищевода характерны одна или несколько язв, окруженных неизмененной слизистой оболочкой. В случае кандидозной природы эзофагита на гиперемированной слизистой оболочке пищевода выявляют желто-белые рельефные наложения. При герпетическом эзофагите на слизистой оболочке пищевода определяются типичные пузырьки (такие же, как в носогубной области), из которых в последующем формируются ограниченные язвы небольшого размера. На ранних стадиях цитамегаловирусного поражения пищевода выявляют линейные серпообразные язвы в средней и нижней трети пищевода. Диагноз грибкового эзофагита подтверждают при микроскопическом исследовании мазков, цитомегаловирусного – с помощью иммуногистологического исследования с моноклональными антителами, при поражении пищевода ВИЧ диагноз основывается на электронно-микроскопическом исследовании образцов пораженных тканей.
Лечение. При коррозивном эзофагите лечение проводят в условиях стационара. Назначают механически, термически и химически щадящую диету № 1 (в ряде случаев на несколько дней рекомендуется голодание, питание через зонд или парентеральное). Применяют вяжущие, обволакивающие средства, местные анестетики, по показаниям – антибиотики. Во избежание формирования стриктуры при коррозивных эзофагитах рано начинают бужирование пищевода, при циркулярных ожогах пищевода используют глюкокортикоиды (преднизолон 1,5–2 мг/кг в сутки с постепенным снижением дозы вплоть до полной отмены в течение 2 мес).
При лекарственном эзофагите соответствующий препарат отменяют и назначают антациды. При невозможности отмены лекарств, вызвавших повреждение пищевода, рекомендуют перейти на их жидкие лекарственные формы, препараты принимают в вертикальном положении и запивают достаточным количеством воды.
При кандидозном эзофагите используют противогрибковые средства (нистатин, при иммунодефицитных состояниях – флюконазол или кетоконазол, при рефрактерности – амфотерицин), при герпетическом и цитомегаловирусном – ацикловир.
Прогноз при коррозивных эзофагитах весьма серьезный; при всех формах в значительной степени зависит от своевременности и систематичности проводимого лечения.
ЭЗОФАГОСПАЗМ (диффузный спазм пищевода) – характеризуется эпизодическим функциональным нарушением перистальтики пищевода и спастическим сокращением его стенки. Различают эзофагоспазм первичный, являющийся следствием кортикальных нарушений регуляции функции пищевода (развивается на фоне психоэмоциональных стрессов), и вторичный (рефлекторный и симптоматический), возникающий вследствие повышенной чувствительности слизистой оболочки пищевода (при рефлюкс-эзофагите, язвенной болезни, новообразованиях пищевода и желудка и т. д. или при заболеваниях, сопровождающихся общим судорожным синдромом, например эпилепсии). Длительный выраженный эзофагоспазм приводит к резкой гипертрофии мышечной оболочки стенки пищевода.
Симптомы, течение. Характерна непостоянная дисфагия, иногда имеющая парадоксальный характер: возникающая при приеме жидкости и отсутствующая при проглатывании плотной и кашицеобразной пищи. Дисфагия может провоцироваться приемом холодной или, напротив, очень горячей пищи, курением, употреблением алкоголя, поспешной едой и т. д. Длительно и упорно протекающая дисфагия может приводить к истощению. Часто отмечается загрудинная боль, связанная с глотанием, но в ряде случаев напоминающая стенокардию. Диагноз подтверждается рентгенологическим исследованием: при проглатывании контрастной взвеси выявляются разнообразные спастические деформации пищевода. Оценить моторную функцию пищевода и выявить эзофагеальные спазмы позволяет эзофагоманометрия. Течение может быть длительным. Осложнениями являются формирование истинных дивертикулов пищевода, аксиальной грыжи пищеводного отверстия диафрагмы.
Дифференциальный диагноз проводят с начальными стадиями ахалазии кардии. Основное значение имеет рентгенологическое исследование, при котором устанавливается нормальная проходимость кардии, хорошо выявляется газовый пузырь желудка. Эзофагофиброскопия позволяет исключить рак пищевода и другие его органические поражения, нередко протекающие с вторичным эзофагоспазмом.
Лечение при вторичном эзофагоспазме в первую очередь должно быть направлено на основное заболевание. Рекомендуются регулярное частое (4–6 раз в день) дробное питание, механически и термически щадящая диета. Медикаментозная терапия включает применение нитратов (изосорбида мононитрат, динитрат), антагонистов кальция (верапамил 80 мг 3 раза в сутки, коринфар 10 мг 3 раза в сутки), холинолитических препаратов (бускопан), спазмолитиков (но-шпа, папаверин). Если эзофагоспазм обусловлен или поддерживается гастроэзофагеальным рефлюксом, холино– и спазмолитики не показаны, в этом случае рекомендуется прием прокинетиков (домперидон, цизаприд). При сопутствующем эзофагите рекомендуется прием местноанестезирующих, обволакивающих, антацидных средств (алмагель или альмагель А, де-нол, гастал и др.). По показаниям применяют седативные средства, антидепрессанты. Отсутствие эффекта от консервативной терапии служит показанием к оперативному лечению (эзофагомиотомия).
ЭНТЕРИТ – группа острых или хронических заболеваний, характеризующихся воспалением слизистой оболочки тонкой кишки.
Энтерит острый. При остром энтерите часто в патологический процесс одновременно вовлекается также желудок (гастроэнтерит) и толстая кишка (гастроэнтероколит).
Этиология, патогенез. Выделяют острые энтериты: 1) инфекционного и вирусного происхождения (с клинической картиной тяжелого энтерита протекают холера, брюшной тиф, сальмонеллезы, иногда грипп и т. д.); 2) алиментарные (обусловленные перееданием с приемом большого количества острой либо слишком грубой пищи, раздражающих слизистую оболочку приправ, крепких алкогольных напитков); 3) токсические (при отравлениях соединениями мышьяка, сулемой и другими ядами; отравлениях грибами – бледной поганкой, мухоморами, ложными опятами, другими ядовитыми веществами небактериальной природы, которые могут содержаться в пищевых продуктах – косточковых плодах, некоторых рыбных продуктах – печень налима, щуки, икра скумбрии и т. д.); 4) аллергические (при идиосинкразии к некоторым пищевым продуктам – землянике, яйцам, крабам и т. д. или при аллергической реакции на лекарственные средства – препараты йода, брома, некоторые сульфаниламиды, антибиотики и т. п.).
Патогенез обусловлен либо непосредственным действием патологического начала на слизистую оболочку тонкой кишки, либо его гематогенным заносом (микробы, токсины) в кишечные сосуды, а затем повреждающим действием при выделении слизистой оболочкой в просвет кишечника либо вследствие аутоиммунных механизмов. Предрасполагающими моментами к возникновению острого гастроэнтерита являются местное (холодное питье) либо общее охлаждение организма, полигиповитаминозы, злоупотребление продуктами, богатыми грубой клетчаткой, и другие факторы.
Симптомы, течение. Заболевание может начинаться с местных симптомов – тошноты, рвоты, диареи, выраженного урчания в животе, иногда спастических болей. Затем к ним присоединяются слабость, общее недомогание, холодный пот, лихорадка (температура может достигать 38–39 °C и выше), явления общей интоксикации, симптомы сосудистого коллапса. В других случаях общие симптомы появляются первыми, а спустя некоторое время (от получаса до нескольких часов) к ним присоединяются признаки воспалительного поражения тонкой кишки. При пальпации живота отмечаются болезненность в эпигастральной области, иногда сильное урчание в слепой кишке. Наблюдаются умеренный, реже выраженный лейкоцитоз, повышение СОЭ.
Дифференциальный диагноз неинфекционных энтеритов проводят прежде всего с острыми кишечными инфекциями (холерой, брюшным тифом, пищевыми интоксикациями), а также с общими инфекционными, в том числе вирусными, заболеваниями, которые могут протекать с энтеритным синдромом. Большое значение имеет эпидемиологический анамнез. Бактериологическое исследование испражнений часто позволяет выделить патогенного возбудителя (при инфекционных острых энтеритах). Детальный расспрос больного облегчает дифференциальную диагностику алиментарных, токсических, аллергических энтеритов.
В легких и среднетяжелых случаях заболевание заканчивается выздоровлением через несколько дней. Тяжелые формы могут осложняться кишечными кровотечениями, некрозом и перфорацией тонкой кишки. При токсических и аллергических энтеритах могут иметь место сопутствующие поражения других органов – сердца, печени, почек и т. д.
Лечение. Больных тяжелым энтеритом, а также энтеритом токсического происхождения (дальнейшее течение которого определить в первые часы болезни трудно) обязательно госпитализируют. Больных инфекционными энтеритами госпитализируют в инфекционные больницы. Во всех случаях острого энтерита с целью удаления из желудочно-кишечного тракта токсинов желудок промывают (зондовым или беззондовым способом) слабым раствором гидрокарбоната натрия, дают внутрь слабительное (30 мл касторового масла или 25 г сульфата магния в 100 мл воды). В первые 12–24 ч назначают голод, рекомендуют обильное питье (кипяченая вода, несладкий чай). При выраженной общей интоксикации назначают п/к или в/в капельные вливания изотонического раствора натрия хлорида или 5 %-ного раствора глюкозы. Внутрь назначают препараты пищеварительных ферментов (креон, панцитрат, фестал и др.), а в дальнейшем в целях нормализации кишечной флоры – колибактерин, бифидумбактерин, бификол, лактобактерин. Со 2-го дня заболевания больным разрешают нежирный бульон, протертые каши на воде, сухари; в последующие дни диету расширяют.
Профилактика острых энтеритов заключается в строгом соблюдении правил личной гигиены, употреблении в пищу только тщательно вымытых овощей и фруктов, рациональном питании, исключении продуктов, которые могут оказать токсическое действие на организм (неизвестные грибы и т. д.).
Энтерит хронический – клинический синдром, характеризующийся нарушением функции тонкой кишки, кишечными расстройствами и изменениями обмена веществ. В классификации ВОЗ хронический энтерит не упоминается (к хроническим воспалениями кишечника относят только болезнь Крона и язвенный колит), поэтому предпочтительнее использование термина «мальабсорбция» с уточнением причины заболевания. Диагностика хронического энтерита возможна только у небольшой части больных с гистологическими признаками хронического воспалительно-дистрофического процесса после исключения заболеваний тонкой кишки другой этиологии.
Этиология. Имеют значение пищевая аллергия, алиментарные нарушения (гиперсенситивный пищевой энтерит, эозинофильный энтерит); производственные интоксикации при нарушениях техники безопасности и хронических отравлениях соединениями свинца, фосфора, мышьяка и др.; бытовые интоксикации, в частности лекарственные (нестероидные противовоспалительные средства, глюкокортикоиды, цитостатики, иммунодепрессанты); ионизирующие излучения (радиационные энтериты – производственные при нарушении техники безопасности или возникающие в результате лучевой терапии злокачественных новообразований органов брюшной полости); ишемия тонкой кишки при сосудистой недостаточности.
Патогенез. Наиболее изученные механизмы развития заболевания: непосредственное хроническое повреждающее воздействие этиологического фактора на стенку тонкой кишки (токсическое, раздражающее); длительно существующий дисбактериоз, сопровождающийся раздражением и токсическим действием продуктов ненормального расщепления пищевых веществ под влиянием ферментов необычной кишечной флоры (органические кислоты, альдегиды, индол, скатол, метан, сероводород и др.), а также бактериальных токсинов на слизистую оболочку кишечной стенки; иммунологические механизмы; нарушение функции пищеварительных желез; микроциркуляторные расстройства.
Симптомы, течение. Боль (если имеет место) обычно носит тупой, редко спастический характер, локализуется в околопупочной области; здесь же нередко отмечается болезненность при пальпации живота и сильном давлении (несколько левее и выше пупка – симптом Поргеса), болезненность по ходу брыжейки тонкой кишки (по направлению от пупка к правому крестцово-подвздошному сочленению – симптом Штернберга). Боль при сотрясении тела, ходьбе может быть признаком перивисцерита. Урчание и плеск при пальпации слепой кишки – важный признак энтерита (симптом Образцова).
Синдром кишечной диспепсии проявляется малохарактерными диспепсическими жалобами: ощущением давления, распирания и вздутия живота, особенно после еды, тошнотой, ощущением урчания, переливания в животе и др., которые возникают в результате нарушения переваривания пищевых веществ в кишечнике, ускорения их пассажа по тонкой кишке, а также нарушения всасывания в кишечнике. Иногда при тяжелом энтерите вскоре после еды возникают слабость, головокружение и другие общие явления, напоминающие демпинг-синдром.
Энтеритный копрологический синдром: частый (до 15–20 раз в сутки) кашицеобразный, с непереваренными частицами пищи, но без видимой слизи, часто зловонный, с пузырьками газа стул. Характерна полифекалия: общее количество каловых масс за сутки может достигать 1,5–2 кг. Иногда возникают резкие позывы к дефекации вскоре после еды, а после дефекации – резкая слабость, сопровождаемая холодным потом, дрожанием рук (еюнальная диарея). В нетяжелых случаях и при отсутствии сопутствующего колита может отсутствовать понос и даже наблюдаться запор. Характерна непереносимость молока: после его приема усиливаются метеоризм, понос. Обострение заболевания вызывают прием острой пищи, содержащей большое количество жиров и углеводов, переедание. Часто имеет место своеобразный желтоватый (золотистый) цвет каловых масс вследствие наличия невосстановленного билирубина и большого количества жира, придающего каловым массам глинистый вид. При микроскопическом исследовании: большое количество остатков непереваренной пищи (лиентерея), капли нейтрального жира (стеаторея), капельки, глыбки и кристаллы жирных кислот и нерастворимых мыл, мышечные волокна (креаторея), свободный внеклеточный крахмал (амилорея), большое количество слизи, равномерно перемешанной с каловыми массами.
Синдром недостаточности всасывания (мальабсорбции) проявляется постепенным снижением массы тела больного (в тяжелых случаях вплоть до кахексии), общей слабостью, недомоганием, понижением работоспособности. В крови гипопротеинемия, гипохолестеринемия, обычно уплощается сахарная кривая. Проба с D-ксилозой (низкое содержание в крови пентоз через 2 ч после приема больным внутрь D-ксилозы и сниженная экскреция их с мочой) подтверждает нарушение всасывания. Анемия бывает железодефицитной, в ряде случаев В12-дефицитной, но нередко имеет смешанный характер, с нормальным цветным показателем. Нередки явления гиповитаминоза (витаминов В1, В2, B6, В12, D, К, А, биотина, фолиевой кислоты); их проявлением могут быть сухость кожи, ангулярные стоматиты, выпадение волос, ломкость ногтей, полиневриты, нарушения сумеречного зрения и т. д. В крови понижается концентрация ряда ионов, особенно Са, в тяжелых случаях возникают патологическая хрупкость костей и другие признаки гипопаратиреоидизма. Гипофизарная недостаточность проявляется нерезко выраженными явлениями несахарного диабета (полидипсия, полиурия в сочетании с гипоизостенурией), надпочечниковая – нерезко выраженными явлениями аддисонизма (гиперпигментация кожи, особенно закрытых от действия света участков кожных складок ладоней, слизистой оболочки рта, а также артериальная и мышечная гипотония). Нарушение функции половых желез у мужчин проявляется импотенцией, у женщин – аменореей.
Рентгенологически при хроническом энтерите чаще всего определяется ускоренный пассаж бариевой взвеси по тонкой кишке и неравномерное скопление ее в различных петлях кишки; нередко видны утолщенные отечные складки слизистой оболочки, в тяжелых случаях – их сглаживание вследствие процесса атрофии.
При аспирационной биопсии из верхних отделов тощей кишки наблюдаются воспалительные и дистрофические изменения слизистой оболочки, уменьшение размеров ворсинок, уплощение клеток поверхностного эпителия и его щеточной каймы, в тяжелых стадиях – развитие склеротических изменений.
Течение хронического энтерита прогрессирует постепенно или бурно, в редких случаях самостоятельно, а также под влиянием лечения и строго выдержанной диеты наблюдается регрессия симптомов заболевания.
Лечение в период обострения проводится в стационаре. Назначают диету № 4-4а, б, в. Пищевой рацион вне обострения должен содержать достаточное количество белка (130–150 г) в основном животного происхождения (телятина, нежирное говяжье или куриное мясо, рыба, яйца, творог) и легко усваиваемых жиров (100–110 г). Исключают тугоплавкие жиры животного происхождения (бараний, свиной); в период обострения процесса количество жиров временно уменьшают до 60–70 г. Количество углеводов в дневном рационе обычное – как при легкой и средней физической нагрузке (около 500–450 г), однако ограничивают продукты, содержащие большое количество клетчатки. Последнее достигается помимо подбора продуктов, тщательной механической обработкой пищи (протертые овощи и фрукты, пюре). При поносах исключают из пищевого рациона чернослив, инжир, капусту, виноград, черный хлеб, свежевыпеченные мучные продукты, орехи, бродильные напитки – пиво, квас. Режим частого (5–6 раз в день) дробного питания; вся пища принимается в теплом виде. В период обострения процесса пища назначаются в механически щадящем виде – в виде слизистых отваров, супов, протертых каш, пюре, паровых котлет, суфле и т. д. При поносах хороший эффект оказывает систематический прием ацидофильного молока (по 100–200 г 3–4 раза в день) и несладких соков и киселей из фруктов и ягод, содержащих дубильные вещества (черника, черная смородина, гранаты, груши и др.). При явлениях авитаминоза назначают витамины, в первую очередь В1; В2, В6, В12, фолиевую кислоту, витамин А, при геморрагических явлениях – витамин К (викасол). Особенно полезны комплексные витаминные препараты: пангексавит, декамевит, ундевит и др.
Антибиотики широкого спектра действий при хроническом энтерите не находят большого применения из-за опасности дисбактериоза. Чаще назначают колибактерин, бифидумбактерин, бификол и производные оксихинолина: энтеросептол, интестопан. Препараты пищеварительных ферментов (желудочный сок и аналогичные лекарственные средства, панкреатин, фестал, холензим, абомин и др.) показаны при преимущественном нарушении полостного внутрикишечного пищеварения.
В период обострения процесса, особенно сопровождающегося поносом, показано пероральное применение вяжущих и обволакивающих средств (нитрат висмута основного, танальбин, теальбин, отвары корневища или корней змеевика, кровохлебки, лапчатки – 4,0-15,0: 200,0 или настоев цветов пижмы, травы зверобоя, шишек ольхи и др. – 10,0-30,0: 200,0 по 1 ст. л. 5–6 раз в день).
При тяжелых энтеритах с явлениями недостаточности всасывания назначают повторно внутривенно вливания плазмы, белковых гидролизатов (аминопептид, гидролизат казеина, аминокровин и др.) – 1 л/сут; в более легких случаях их вводят через интрагастральный зонд капельно.
Из физиотерапевтических процедур наиболее эффективны согревающие компрессы, парафиновые аппликации, озокерит, диатермия, индуктотермия и т. д. Курортное лечение в санаториях Железноводска, Ессентуков, Пятигорска, Миргорода, Боржоми. В тяжелых случаях хронического энтерита показаны трудоустройство больных и перевод на инвалидность. Необходимы своевременное лечение острых и подострых энтеритов и диспансеризация больных хроническим энтеритом с целью профилактики рецидивов болезни и возникновения возможных осложнений.
ЭНТЕРОКОЛИТ – см. Энтерит, Колит.
ЭНТЕРОПАТИЯ ЭКССУДАТИВНАЯ ГИПОПРОТЕИНЕМИЧЕСКАЯ (кишечная лимфангиэктазия, болезнь Гордона) – редкое заболевание, характеризующееся расширением лимфатических сосудов и повышенной проницаемостью кишечной стенки, значительной потерей белка через желудочно-кишечный тракт. Первичная экссудативная энтеропатия наблюдается в основном у лиц молодого возраста. Вторичная энтеропатия развивается в связи с заболеваниями желудка (гипертрофическим гастритом), кишечника (при хроническом энтерите, целиакии, болезни Крона, болезни Уиппа, неспецифическом язвенном колите и др.), при циррозе печени и др. При первичной экссудативной гипопротеинемической энтеропатии определенное значение имеют семейная предрасположенность, сенсибилизация организма.
Симптомы, течение. Заболевание характеризуется поносом, гипопротеинемическими отеками. В тяжелых случаях развивается общее истощение. Нередки гипохромная анемия, незначительный лейкоцитоз с наклонностью к лимфопении. Гипопротеинемия отмечается в основном за счет снижения содержания альбуминов и гамма-глобулинов; гипохолестеринемия; гипокальциемия. В испражнениях повышено содержание нейтрального жира, жирных кислот и мыл. Специальные лабораторные методы исследования обнаруживают повышенное содержание белка в тонкокишечном секрете и повышенное выделение его с испражнениями. Радиоизотопное исследование экскреторной функции тонкой кишки позволяет определить увеличение радиоактивности фекалий и быстрое снижение радиоактивности крови после в/в введения сывороточного альбумина, меченного хромом-51, т. е. подтверждает повышенную потерю белка из организма через кишечник. В биоптатах из слизистой оболочки кишки наблюдаются характерное расширение лимфатических сосудов, воспалительная инфильтрация ткани. В расширенных лимфатических сосудах и синусах мезентериальных лимфатических узлов – липофаги, содержащие в цитоплазме микрокапельки жира.
Дифференциальный диагноз проводится с энтеритами, энтероколитами, а также спру, целиакией. С достоверностью установить диагноз экссудативной энтеропатии позволяет энтеробиопсия. Заболевание протекает хронически и медленно прогрессирует. Больные подвержены интеркуррентным инфекциям (пневмонии, гнойные инфекции, ангины и т. д.), которые могут послужить причиной их гибели.
Лечение в период обострения проводят в стационаре. Назначают механически и химически щадящую диету с повышенным содержанием белка, витаминов, ограничением жидкости, поваренной соли и жира. По показаниям проводится заместительная терапия белковыми препаратами, витаминами, препаратами кальция, железа. При отеках одновременно с переливаниями плазмы n различных белковых препаратов применяют диуретические средства, верошпирон.
ЯЗВА ТОНКОЙ КИШКИ НЕСПЕЦИФИЧЕСКАЯ (идиопатическая, пептическая, трофическая, круглая и др.). Первичная язва тонкой кишки – редкое заболевание, характеризующееся появлением одного или множественных изъязвлений преимущественно в подвздошной кишке, напоминающих по морфологии пептические язвы желудка и двенадцатиперстной кишки. Встречается преимущественно у мужчин.
Этиология и патогенез неизвестны. Предрасполагающими факторами являются местные сосудистые нарушения, повышенная триптическая активность сока поджелудочной железы, длительное применение некоторых препаратов (преднизолона, солей калия и др.).
Симптомы малохарактерны и диагноз часто устанавливается во время операции при возникновении осложнений (перфорации, кишечное кровотечение). Иногда наблюдаются боль в эпигастрии или правой подвздошной области, возникающая через 3–4 ч после еды, локальная болезненность в этой области и напряжение мышц передней брюшной стенки при пальпации. Исследование кала выявляет скрытое кровотечение. При прицельном рентгенологическом исследовании иногда удается обнаружить язвенную нишу в тонкой кишке. Дифференциальную диагностику проводят с туберкулезными язвами, язвами тонкой кишки при брюшном тифе, амилоидозе, регионарном энтерите, распадающейся опухоли.
Возможные осложнения: кишечные кровотечения, перфорация, стенозирование кишки.
Лечение: предпочтительно хирургическое лечение, абсолютно показанное при возникновении осложнений и в диагностически сомнительных случаях (нельзя исключить изъязвление опухоли).
ЯЗВЕННАЯ БОЛЕЗНЬ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ – хроническое рецидивирующее заболевание, основным признаком которого является образование дефекта (язвы) в стенке желудка или двенадцатиперстной кишки.
Этиология, патогенез. Принято считать, что язвенная болезнь является полиэтиологическим заболеванием. К развитию болезни предрасполагает наследственность, свидетельством этому служат заболевания у близких родственников, конкордантность возникновения и идентичность локализации язвенной болезни у монозиготных близнецов. К доказательным генетическим факторам относят показатели максимальной секреции соляной кислоты, содержание пепсиногена-I в сыворотке крови, повышение высвобождения гастрина в ответ на еду. В ряду генетически обусловленных факторов язвенной болезни существенное место отводится групповой специфичности крови, ее резус-принадлежности, способности секретировать антигены, ответственные за выработку гликопротеинов желудочной слизи и др. Важную роль могут также играть генетические особенности психического статуса.
В последние годы наиболее частой причиной развития язвенной болезни принято считать инфекцию Helicobacter pylori. Эти бактерии обнаруживаются преимущественно в антральном отделе желудка под слоем слизи на поверхности эпителиоцитов. В двенадцатиперстной кишке Helicobacter pylori находят только в участках желудочной метаплазии. Считаются доказанными несколько механизмов повреждающего действия этих бактерий на слизистую оболочку – непосредственное прилипание микроорганизмов к клеткам эпителия, аммиак, выделяемый под действием фермента уреазы и бактериальные цитотоксины. В то же время роль хеликобактера в этиологии язвенной болезни остается спорной. В пользу хеликобактерной теории свидетельствуют: частое обнаружение этих микроорганизмов при язвенной болезни; связь рецидива гастродуоденальных язв с сохранением инфекции. Против нее: в условиях эксперимента можно воспроизвести хеликобактерный гастрит, но не язву; язвенная болезнь не имеет эпидемиологических характеристик инфекции; спонтанного заживления язвы не происходит с исчезновением хеликобактера; с возрастом частота хеликобактерного гастрита нарастает, а дуоденальных язв снижается. Неясно также, почему язва локализуется чаще в двенадцатиперстной кишке, а не в желудке, где обсеменение хеликобактером всегда более выражено. Хеликобактерная теория не может объяснить сезонные обострения язвенной болезни. Наконец, вызывает тревогу тот факт, что со времени возникновения хеликобактерной теории язвенной болезни и широкого внедрения эрадикационной терапии отмечен значительный рост числа больных гастроэзофагеальной рефлюксной болезнью и связанных с ней осложнений, а также учащение случаев язвенного кровотечения и прободения язв.
Таким образом, всю проблему этиологии язвенной болезни нельзя свести только к инфекции Helicobacter pylori. По-видимому, вызванный этими микроорганизмами антральный гастрит способствует развитию язвенной болезни у лиц, генетически предрасположенных к этому заболеванию.
В возникновении заболевания могут играть роль нарушения режима и характера питания (например, систематическое употребление острой и грубой пищи, торопливая еда и еда в сухомятку), курение и злоупотребление алкоголем, крепким кофе, психоэмоциональные перегрузки (недостаточные отдых и сон, ненормированный рабочий день, стрессовые ситуации), физическое перенапряжение. Спровоцировать развитие язвенной болезни может длительный прием лекарственных препаратов, неблагоприятно воздействующих на слизистую оболочку желудка и двенадцатиперстной кишки (в первую очередь, нестероидных противовоспалительных средств).
Развитию язвенной болезни способствуют некоторые заболевания внутренних органов – обструктивные болезни легких, сердечно-сосудистой системы, печени, поджелудочной железы, сопровождающиеся функциональной недостаточностью этих органов и систем. Важную роль в образовании язв может играть гиперсекреторный синдром, например при гастриноме.
Непосредственное формирование язвы происходит в результате нарушения физиологического равновесия между агрессивными (протеолитически активный желудочный сок, заброс желчи, этанол, никотин, нестероидные противовоспалительные средства, инфекция Helicobacter pylori и др.) и защитными факторами (желудочная и дуоденальная слизь с растворенными в ней гидрокарбонатами, клеточная регенерация, нормальное состояние местного кровотока и др.).
Симптомы, течение. Ведущим симптомом язвенной болезни является боль, возникающая чаще в подложечной области слева от срединной линии (при язвах тела желудка) или справа от нее (при язвах в области канала привратника и луковицы двенадцатиперстной кишки), нередко иррадиирующие в левую половину грудной клетки, область мечевидного отростка грудины, грудной или поясничный отдел позвоночника. Боль может быть ноющей, режущей, схваткообразной, тупой или интенсивной. Она обычно четко связана с приемом пищи. Так, при язвах тела желудка боль возникает, как правило, через 30–60 мин после еды (ранние боли), при язвах канала привратника и луковицы двенадцатиперстной кишки – через 2–3 ч (поздние боли), а также натощак («голодные боли»), нередко ночью. Боль купируется антацидами, спазмолитиками, тепловыми процедурами на эпигастральную область, поздние и «голодные» боли прекращаются после приема пищи, особенно молочной. Нередко наблюдается рвота кислым желудочным содержимым на высоте боли, приносящая облегчение. Часто язвенная болезнь двенадцатиперстной кишки сопровождается запорами. Несмотря на хороший аппетит, может отмечаться похудание в связи с тем, что больные ограничивают себя в еде, опасаясь возникновения или усиления боли. При пальпации определяется болезненность в эпигастральной области, иногда некоторая резистентность мышц брюшного пресса.
Следует учитывать, что при язвах кардиального отдела желудка боль нередко локализуется в области мечевидного отростка грудины, что порой неправильно расценивается как проявление заболевания сердца. При внелуковичных язвах боль может локализоваться в области правого подреберья, симулируя обострение хронического холецистита. В ряде случаев болевой синдром вообще отсутствует, его эквивалентом выступают различные диспептические расстройства, например изжога, возникающая с той же периодичностью, что и боли. Встречаются бессимптомные формы язвенной болезни, у таких больных заболевание обнаруживается случайно либо его первыми клиническими проявлениями бывают осложнения.
Копрологическое исследование определяет скрытое кровотечение. При локализации язвы в желудке кислотность желудочного сока нормальна или несколько снижена, при язве двенадцатиперстной кишки – повышена. Наличие стойкой гистаминорезистентной ахлоргидрии исключает язвенную болезнь (возможна раковая, трофическая, туберкулезная и другая природа изъязвления).
При рентгенологическом исследовании в большинстве случаев (60–80 %) выявляется ограниченное затекание взвеси сульфата бария за контур слизистой оболочки – язвенная ниша. В желудке язвы обычно локализуются по малой кривизне, в двенадцатиперстной кишке – в луковице. Редко встречаются и трудно диагностируются язвы привратника, внелуковичные язвы двенадцатиперстной кишки.
Наиболее достоверным методом диагностики является гастродуоденоскопия, позволяющая обнаружить язву, определить ее характер, взять биопсию (при язвах желудка).
Для диагностики инфекции Helicobacter pylori используют следующие методы: бактериологический (посев биоптата на дифференциально-диагностическую среду, наиболее доказательный, но трудоемкий метод, применяется редко), гистологический (окраска бактерии в гистологических препаратах слизистой оболочки желудка), цитологический (окраска бактерии в мазкахотпечатках биоптатов, применяется редко), дыхательный уреазный тест (определение в выдыхаемом воздухе изотопов углерода, выделяемых в результате расщепления в желудке меченой мочевины под действием бактериальной уреазы), уреазный тест (определение уреазной активности в биоптате слизистой оболочки желудка), серологический тест (выявление антител к антигенам бактерий).
Дифференциальную диагностику проводят с изъязвленной опухолью (в том числе первично-язвенным раком), туберкулезной, сифилитической язвой; изъязвлениями при коллагенозах, амилоидозе. Особенностью язвенной болезни является характер болей (голодные, после еды через определенный срок, ночные), длительный анамнез заболевания с периодическими обострениями в весенне-осенние периоды, наличие хлористоводородной кислоты в желудочном соке при исследовании.
Течение обычно длительное с обострениями в весенне-осенний период и под воздействием неблагоприятных факторов (стрессовые ситуации, пищевые погрешности, прием крепких алкогольных напитков и пр.). Осложнения: кровотечение, перфорация, пенетрация, деформации и стенозы, перерождение язвы в рак.
Прогноз относительно благоприятный, за исключением тех случаев, когда возникают осложнения. Трудоспособность сохранена, однако не показаны все виды работ, связанные с нерегулярным питанием, большими эмоциональными и физическими перегрузками.
Лечение в период обострения может проводиться в стационаре, чаще осуществляется в амбулаторно-поликлинических условиях. В первые 2–3 нед режим постельный, затем палатный. Питание дробное и частое (4–6 раз в сутки), диета полноценная, сбалансированная, химически и механически щадящая (№ 1а, 1б, затем № 1).
Современные принципы медикаментозной терапии язвенной болезни желудка и двенадцатиперстной кишки не различаются. Основой противорецидивного лечения признана антихеликобактерная терапия, включающая применение антисекреторных и противомикробных средств. Рекомендуют следующие схемы эрадикационной терапии. Семидневная тройная схема лечения: омепразол 20 мг 2 раза в сутки, или лансопразол 30 мг 2 раза в сутки, или пилорид (ранитидин/висмут цитрат) 400 мг 2 раза в сутки + кларитромицин 250 мг 2 раза в сутки, или тетрациклин 0,5 г 4 раза в сутки либо по 1,0 г 2 раза в сутки, или амоксициллин 0,5 г 4 раза в сутки либо 1,0 г 2 раза в сутки + метронидазол 400–500 мг 2 раза в сутки или фуразалидон 0,2 г 2 раза в сутки. Семидесятидневная четвертная эрадикационная терапия: омепразол 20 мг 2 раза в сутки, или лансопразол 30 мг 2 раза в сукти, или ранитидин 150 мг 2 раза в сутки, или фамотидин 20 мг 2 раза в сутки + де-нол или вентрисол 120 мг 2 раза в сутки + тетрациклин 250 мг 5 раз в сутки, или амоксициллин 500 мг 4 раза в сутки либо 1,0 г 2 раза в сутки, или азитромицин 0,5 г 2 раза в сутки + метронидазол 200 мг 5 раз в сутки, или фуразалидон 0,1 г 3 раза в сутки.
Применение эффективных комбинаций лекарственных средств делает необязательным контроль эрадикации в случае неосложненной язвенной болезни двенадцатиперстной кишки. У пациентов с язвенной болезнью желудка, осложненным течением язвенной болезни, контроль эффективности эрадикационной терапии проводится не ранее чем через 4–6 нед после ее окончания, по меньшей мере, двумя диагностическими методами (обычно гистологическим и уреазным). При сохранении инфицирования хеликобактером в связи с вероятной резистентностью микроорганизмов к одному из компонентов проведенного лечения повторный курс эрадикационной терапии проводится по новой схеме.
После окончания эрадикационной терапии в целях окончательного купирования клинических симптомов и достижения рубцевания язвы проводится лечение антисекреторным средством (омепразол 20 мг 1 раз в сутки, или лансопразол 30 мг 1 раз в сутки, или ранитидин 300 мг 1 раз в сутки, или фамотидин 40 мг 1 раз в сутки, или пилорид 400 мг 1 раз в сутки) еще в течение 5–7 нед. Антацидные средства (альмагель, фосфалюгель, маалокс и др.) используются главным образом в качестве вспомогательных средств для быстрого купирования боли, диспепсии. Применение антацидов и селективных холинолитических средств (гастроцепина) в качестве базисной противоязвенной терапии возможно, по-видимому, при легком течении заболевания, редких обострениях, умеренном повышении кислотности желудочного сока, отсутствии осложнений.
При язвенной болезни, не ассоциированной с инфицированием Helicobacter pylori, лечение включает применение антисекреторных средств (ранитидин 300 мг в сутки или фамотидин 40 мг в сутки) в комбинации с антацидными средствами (маалокс и т. п.) или применение сукральфата (вентера) в дозе 4 г в сутки.
Контроль результатов рубцевания язв обычно проводят через 4 и 6 нед лечения при язвенной болезни двенадцатиперстной кишки и через 6 и 8 нед при язвенной болезни желудка. Если язва не рубцуется в течение 12 нед, целесообразно увеличить исходную дозу ингибитора протонного насоса вдвое либо перевести пациента на терапию ингибиторами протонного насоса (если он до того получал лечение блокатором Н2-гистаминовых рецепторов).
Поддерживающая терапия считается необходимой в тех случаях, когда язвенная болезнь не ассоциирована с инфицированием хеликобактером, когда две попытки антихеликобактерной терапии не увенчались успехом, в случае осложненного течения язвенной болезни (при наличии в анамнезе перфорации язв, кровотечений), а также при наличии сопутствующих заболеваний, требующих постоянного приема нестероидных противовоспалительных средств. Рекомендуется ежедневный прием антисекреторных средств (ранитидин 150 мг или фамотидин 20 мг 1 раз в сутки на ночь). Терапия «по требованию» подразумевает использование антисекреторных препаратов при появлении боли или дискомфорта в эпигастрии после успешной эрадикации Helicobacter pylori; применяют ранитидин, или фамотидин, или омепразол в течение 2–3 дней в полной суточной дозе и далее в течение 2 нед в половинной дозе.
Санаторно-курортное лечение рекомендуется проводить лишь в стадии стойкой ремиссии (Железноводск, Боржоми, Ессентуки, Пятигорск, Моршин, Старая Русса и др.).
Профилактика: соблюдение гигиенических норм труда, быта и питания, воздержание от курения и систематического употребления алкоголя, отказ (по возможности) от приема лекарственных средств, повреждающих слизистую оболочку желудка (в частности, нестероидных противовоспалительных средств). Больные должны находиться под диспансерным наблюдением с активным проведением курсов противорецидивного лечения при обострении язвенной болезни. Обследование проводится при каждом обострении и в плановом порядке – 1 раз в год при язвенной болезни желудка и 1 раз в 2 года при язвенной болезни двенадцатиперстной кишки.






