Группа сыпного тифа
К ней относятся: эпидемический сыпной тиф и эндемический (крысиный) сыпной тиф и соответственно два вида возбудителей: R. prowazekii и R. typhi. В эту же группу риккетсий включен еще один вид – R. canada, обнаруженный у клещей, паразитирующих на кроликах и зайцах. Серологическими методами были выявлены случаи заболевания людей, вызванные R. canada, клинически не отличимые от лихорадки Скалистых гор, но R. canada не имеет антигенного родства с риккетсиями группы пятнистой лихорадки. Характерной особенностью риккетсий этой группы является то, что они размножаются в цитоплазме эукариотных клеток (см. цв. вкл., рис. 109.4), но не в вакуолях (R. canada также и в ядре) и имеют антигенное родство между собой. Содержание Г + Ц в ДНК ? 30 мол %.
Сыпной тиф – острое инфекционное заболевание, характеризующееся глубокой интоксикацией, характерным поражением прекапиллярных разветвлений артерий и сыпью. Возбудитель – R. prowazekii – палочки размером от 0,3 – 0,6 до 0,8 – 2,0 мкм, иногда до 4,0 мкм, располагающиеся одиночно или короткими цепочками. Хорошо размножаются в желточном мешке куриного эмбриона, оптимальная температура для их размножения 35 °C. Эмбрион погибает через 6 – 13 дней после заражения (в зависимости от величины заражающей дозы). Хороший рост наблюдается и в культурах клеток различных линий с образованием через 8 – 10 дней бляшек диаметром ? 1 мм. К возбудителю сыпного тифа очень чувствительны морские свинки, которые обычно используются для первичного выделения риккетсий. У свинок приблизительно через неделю появляется лихорадка и у самцов иногда наблюдается скротальный феномен (периорхит – воспаление оболочек яичек). Иногда у морских свинок риккетсиозная инфекция протекает бессимптомно. Риккетсии выделяются из крови, селезенки, надпочечников, почек, но особенно много их в мозге.
Антигенное строение. Возбудитель сыпного тифа имеет термостабильный групповой антиген, общий с антигенами R. typhi и R. canada, и термолабильный видоспецифический антиген, располагающийся в поверхностных структурах возбудителя. Штаммы R. prowazekii, выделенные из разных источников, по антигенной структуре существенно не отличаются друг от друга.
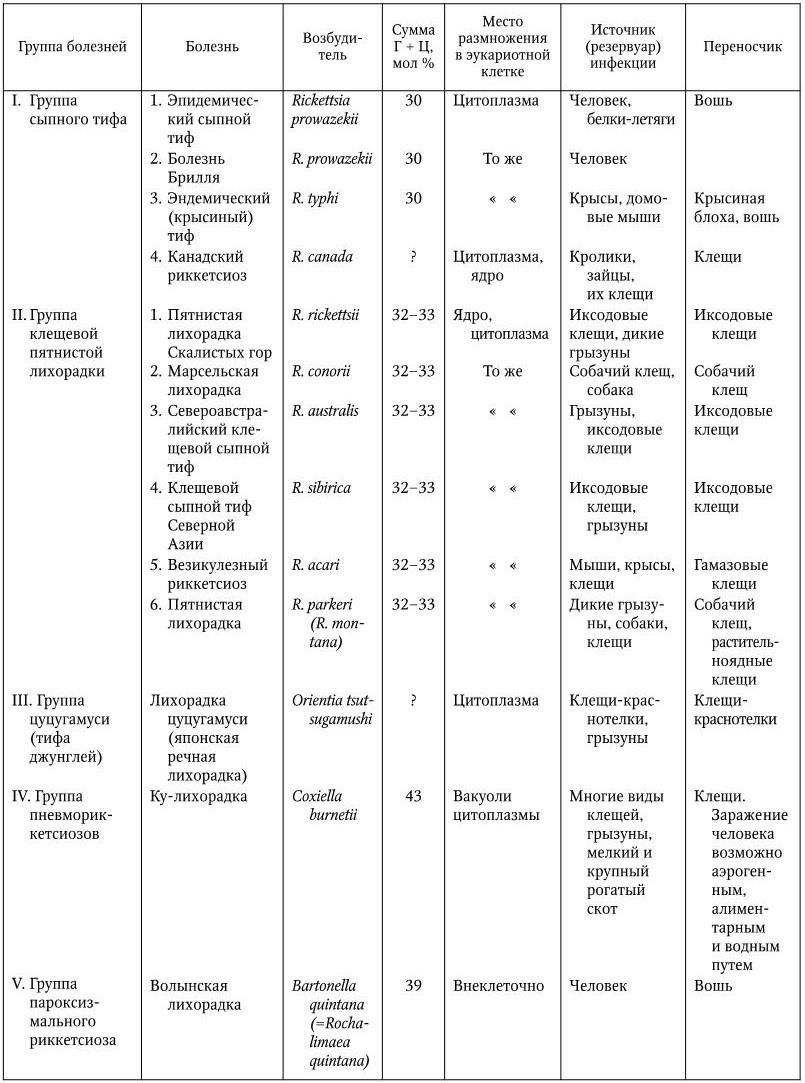
Таблица 50
Заболевания, вызываемые риккетсиями, ориенциями, коксиеллами и бартонеллами
Резистентность.
Факторы патогенности. Патогенность риккетсий связана с наличием у них пока не идентифицированных факторов адгезии и инвазии, с помощью которых они вначале прикрепляются к клеткам, а затем внедряются в них и размножаются. У риккетсий, как у всех грамотрицательных бактерий, имеется эндотоксин (ЛПС). Кроме того, у них обнаружен в капсулоподобном слое, покрывающем клетки, особый токсический термолабильный белок с м. м. 100 кД. Внутривенное введение взвеси риккетсий белым мышам вызывает их гибель через 4 – 24 ч от острой интоксикации. При интраназальном заражении риккетсиями белых мышей у них развивается смертельная пневмония.
Особенности эпидемиологии. Основным источником эпидемического (вшивого, европейского) сыпного тифа является человек. У него возбудитель находится в крови. Это было установлено опытом самозаражения в 1876 г. О. О. Мочутковским, а Г. Н. Минх еще в 1874 г. высказал предположение, что заражение сыпным и возвратным тифом происходит через укусы вшей и блох. Однако только в 1910 г. Ш. Николь окончательно доказал, что возбудитель сыпного тифа передается от больного человека здоровому через укусы вшей – Pediculus corporis (= Pediculus humanus), причем эту роль выполняют в основном платяные вши. Головная и лобковая вши также могут инфицироваться риккетсиями, но они реже покидают своего хозяина и их роль в эпидемиологии сыпного тифа гораздо меньше. Эта особенность передачи возбудителя делает сыпной тиф способным к широкому распространению всюду, где имеется вшивость. Вошь заражается при сосании крови больного, проявляя при этом одинаково высокую чувствительность к возбудителю во всех фазах своего метаморфоза после яйца. При этом вошь легче всего заражается при повторном сосании крови больного, особенно при тяжелых формах болезни и в первую неделю ее. Во время сосания вошь прокалывает кожу хоботком и потребляет около 1 мг крови сразу. Но для того чтобы ее всосать, она освобождает кишечник – выделяет экскременты. Кровь переваривается, а риккетсии проникают в эпителиальные клетки кишечника и размножаются в них в огромном количестве, так что клетки разрушаются, а риккетсии выделяются с экскрементами. Лишь после этого, через 4 – 5 дней, вошь способна заразить здорового человека. У вшей риккетсии вызывают смертельный риккетсиоз, они погибают через 2 – 2,5 нед. У зараженных вшей риккетсии размножаются только в кишечнике, в слюнных железах их нет. Поэтому сам по себе укус не заразен, но слюна вшей вызывает в месте укуса раздражение, и человек, почесывая, втирает риккетсии в ранку, нанесенную вошью. Являясь однохозяинным паразитом, вошь обитает на белье человека, переходя на его кожу через каждые 5 ч для питания. Оптимальная температура для ее существования – 30 °C, поэтому, когда у зараженного ею человека температура тела повышается до 39 – 41 °C, вошь возбуждается, стремится покинуть хозяина и поселяется на белье другого человека. Таким образом, эпидемиологическая цепь при сыпном тифе такова: больной человек – вошь – здоровый человек. Ликвидация вшивости – главное условие ликвидации эпидемии сыпного тифа.
Патогенез и клиника. Восприимчивость к болезни близка к 100 %. Риккетсии попадают в кровь и разносятся по всему организму, избирательно поражая эндоте-
лиальные клетки прекапиллярных разветвлений артерий различных органов, что проявляется в виде деструктивно-пролиферативного эндопериваскулита. Формирование своеобразных тромбоваскулитов приводит к резкому расстройству периферического кровообращения и глубоким нарушениям тканей; особенно тяжелые последствия наблюдаются при поражении мозговой ткани (продолговатый мозг), а также эндотелия капилляров надпочечников, сердечной мышцы и кожи. К этим нарушениям присоединяется сильная интоксикация, обусловленная эндотоксином и, особенно, токсическим белком с м. м. 100 кД. Инкубационный период составляет в среднем 10 – 12 дней. После небольшого продромального периода болезнь начинается сразу с повышения температуры до 39 – 40 °C и сильной головной боли. Больной может впадать в состояние бреда, иногда развиваются явления менингоэнцефалита и психоза. На 4 – 6-й день на боковых поверхностях груди, на спине и сгибательных поверхностях рук появляется характерная розеолезно-петехиальная сыпь. Лихорадка держится 1,5 – 2 нед., затем температура быстро снижается до нормы. Выздоровление происходит медленно вследствие глубоких нарушений со стороны сердечнососудистой и нервной систем. Летальность в прошлом составляла 20 – 40 %, сейчас, благодаря антибиотикотерапии, не превышает 1 %.
Постинфекционный иммунитет длительный, стойкий, но нестерильный: возбудитель сохраняется в организме в течение длительного времени в виде покоящихся форм. У лиц, перенесших сыпной тиф, нередко наблюдаются его повторные случаи через 10 – 15 – 20 и более лет, которые рассматриваются не как следствие повторного заражения (хотя оно и возможно), а чаще как рецидив, наступающий, очевидно, в результате ослабления иммунитета. Такой повторный сыпной тиф протекает значительно легче, без осложнений, наблюдается в отсутствие источника заражения и вшивости. Повторный сыпной тиф (рецидив сыпного тифа) получил название болезни Брилля – Цинссера.
Лабораторная диагностика. Для диагностики сыпного тифа могут быть применены различные методы: заражение кровью больного животных (морские свинки, белые мыши), куриных эмбрионов или культур клеток, серологические реакции и аллергическая проба. Однако чаще всего используют три серологические реакции – агглютинации, РСК и РПГА. Еще в 1916 г. Э. Вейль и А. Феликс установили, что выделенный ими штамм Proteus vulgaris OX19 (без жгутиков) способен давать положительную реакцию агглютинации, начиная с 10 – 12-го дня болезни, почти у 100 % больных сыпным тифом. Это свойство обусловлено наличием у риккетсий и протея общих полисахаридных антигенов. Поэтому реакция Вейля – Феликса применялась длительное время для диагностики сыпного тифа. Сыворотка больных различными формами клещевой пятнистой лихорадки давала положительную реакцию агглютинации с P. vulgaris OX19 и OX2, а больных тифом джунглей – с OXK. Однако для серологической диагностики сыпного тифа и всех других риккетсиозов ныне используют исключительно риккетсиозные антигены соответствующих видов. Это сделало серологические реакции более специфическими и надежными. Реакция агглютинации при сыпном тифе становится положительной (1: 100) с 4 – 5-го дня болезни, антитела достигают максимального титра к 12 – 16-му дню и держатся на этом уровне до 30-го дня, но через 3 – 5 мес. после болезни они исчезают. Комплементсвязывающие антитела обнаруживаются с 5 – 6-го дня болезни, достигают максимального титра к 14 – 16-му дню. Титр их через 1 – 1,5 мес. начинает снижаться, но эти антитела сохраняются в организме переболевших многие годы. РСК при сыпном тифе строго специфична (даже в разведении 1: 5 имеет диагностическое значение). Поэтому с помощью РСК диагноз сыпного тифа можно с уверенностью ставить ретроспективно у всех переболевших. РПГА при сыпном тифе позволяет отличить активную форму болезни и ближайшую реконвалесценцию, при которых она бывает положительной в разведении 1: 1000 и более, от ранее перенесенного заболевания. Для диагностики сыпного тифа предложены также реакции иммунофлуоресценции, непрямого гемолиза и иммуноферментный метод в модификации «захват» антител класса IgM, а также внутрикожная аллергическая проба, выявляющая аллергическую чувствительность замедленного типа.
Лечение. Наиболее эффективны для лечения сыпного тифа антибиотики – тетрациклины, макролиды, левомицетин и др.
Профилактика. В межэпидемическом периоде риккетсии сохраняются только в организме людей, переболевших сыпным тифом. Они являются главным источником и резервуаром возбудителя сыпного тифа. Существует, по-видимому, единственный природный очаг сыпного тифа в юго-восточном регионе США. Резервуаром риккетсий здесь являются белки-летяги, а переносчиком – их вши. Человек заражается от белок-летяг при переходе их вшей на него. Однако этот очаг существенного значения в эпидемиологии сыпного тифа не имеет. Поскольку заражение людей сыпным тифом происходит через вшей, основным условием успешной борьбы с сыпным тифом является ликвидация вшивости.
Для специфической профилактики, необходимость в которой может возникнуть только по эпидемическим показаниям, предложены различные вакцины: живая сыпнотифозная вакцина из ослабленного штамма риккетсии Провачека Е, живая комбинированная вакцина из штамма Е и антигенов риккетсий, химическая сыпнотифозная вакцина из антигенов клеточной стенки риккетсий.
Эндемический (крысиный) сыпной тиф. Крысиный тиф – относительно легкая лихорадочная болезнь продолжительностью 9 – 15 дней, которая характеризуется головной болью и пятнистой сыпью. Впервые заболевание было описано в 1922 г. Ф. Хоуном, а возбудитель – R. typhi (R. mooseri) – был обнаружен в 1931 г. Р. Диером и независимо от него Х. Музером.
R. typhi по своим размерам и форме очень сходна с R. prowazekii, но обладает меньшим полиморфизмом. По антигенной структуре риккетсии тифа отличаются от риккетсий группы клещевой пятнистой лихорадки, но сходны с R. prowazekii благодаря наличию общего с последними термостабильного антигена. В то же время они имеют свой специфический термолабильный антиген, что позволяет легко дифференцировать их серологически. R. typhi хорошо размножаются в желточных мешках куриных эмбрионов, вызывая их гибель через 6 – 8 дней после заражения. В желточных мешках обнаруживается обильное накопление мелких палочковидных риккетсий. Для этого вида риккетсий вообще характерно чрезвычайно интенсивное размножение их в цитоплазме поражаемых клеток мезотелия грызунов в виде кокковидных или мелких палочковидных форм. Они образуют огромные скопления, почти целиком замещающие цитоплазму разрушенных клеток, такие клетки получили название музеровских.
Подобно возбудителю сыпного тифа, патогенность риккетсии крысиного тифа связана с наличием у нее эндотоксина и своеобразного токсического поверхностного белка. Морские свинки проявляют к R. typhi примерно такую же восприимчивость, как и к риккетсиям сыпного тифа. Лихорадка у свинок появляется через 3 – 7 дней, кривая ее течения часто имеет седловидный характер. Наиболее характерным признаком для экспериментальной инфекции является скротальный феномен. Он воспроизводится только при внутрибрюшинном заражении и обнаруживается уже с первого дня лихорадки. Риккетсии находятся в большом количестве в воспаленных оболочках яичек (в музеровских клетках или внеклеточно), в мозге, почках, крови.
Мыши также очень чувствительны к возбудителю крысиного тифа как при парентеральном, так и при интраназальном заражении. Заражение через нос вызывает у них смертельную пневмонию с обильным накоплением риккетсий в легочной ткани.
Эпидемиология. Заболеваемость людей крысиным тифом связана с наличием эндемических очагов, которые распространены по всему свету, в основном в портовых городах теплых морей. Резервуаром возбудителя являются крысы и другие грызуны, главными переносчиками его – крысиная блоха (Xenopsylla cheopis) и крысиная вошь (Polyplax spinulosus). Крысиная блоха высокочувствительна к R. typhi, хотя инфекция у нее протекает скрытно; она выделяет риккетсии с экскрементами в большом количестве. Заражение человека происходит через укусы крысиной блохи так же, как при сыпном тифе. Блоха и вошь человека тоже высокочувствительны к R. typhi и могут выполнять роль его переносчика от человека к человеку. Заражение человека крысиным тифом возможно также алиментарным путем при употреблении продуктов, загрязненных мочой инфицированных грызунов. Допускается возможность распространения крысиного тифа среди грызунов и людей через укусы крысиного клеща.
Клиника крысиного тифа у человека в общем сходна с таковой при эпидемическом сыпном тифе, но отличается более доброкачественным течением, хотя наблюдались случаи тяжелых форм болезни. Инкубационный период обычно равен 8 – 12 дням. Болезнь, как правило, протекает благоприятно: осложнения, рецидивы и смертность практически отсутствуют.
Постинфекционный иммунитет стойкий, длительный, обусловлен антимикробными антителами и антителами, нейтрализующими токсический белок риккетсий. За счет общего с R. prowazekii антигена возникает перекрестный иммунитет между крысиным и сыпным тифом.
Для лечения крысиного тифа используют те же антибиотики, как и при лечении сыпного тифа.
Лабораторная диагностика. В связи с большим сходством клинической картины крысиного тифа с легкими формами сыпного тифа, основную роль в диагностике этого, как и других риккетсиозов, играют серологические реакции (агглютинации, РСК, РПГА, ИФМ и др.) с применением специфических антигенов риккетсий крысиного тифа.
Профилактика. Для специфической профилактики могут быть использованы вакцины из риккетсий крысиного тифа (убитая вакцина из риккетсий Провачека для этой цели не пригодна), но они применяются лишь по эпидемическим показаниям. Общие меры профилактики этого риккетсиоза сводятся к уничтожению крыс и мышей, охране пищевых продуктов от загрязнения мочой крыс, а также к предупреждению завоза крыс в портовые города прибывающими судами.
Недавно описан риккетсиоз у людей, вызываемый R. felis и протекающий очень сходно с сыпным тифом. Заражение происходит через укусы кошачьей блохи.






