Участие микроорганизмов в круговороте серы, фосфора и железа
Сера – составная часть некоторых белков. Одним из конечных продуктов гниения белков является H2S. Сероводород не усваивается высшими растениями. Биохимические превращения серы восстановительного и окислительного порядка осуществляются серобактериями. Для них H2S является источником энергии. Серобактерии окисляют H2S с выделением свободной серы, которая отлагается у них в цитоплазме в виде капель:
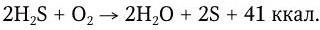
В клетках бактерий сера окисляется далее до серной кислоты:
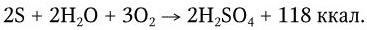
Образующиеся сульфаты (соли H2SO4) служат прекрасным питательным веществом для высших растений. H2S в серную кислоту окисляют различные виды пурпурных серобактерий:
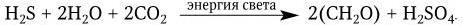
Наряду с такими сульфурирующими бактериями в природе не менее широко распространены и десульфурирующие микробы (аналоги денитрифицирующих бактерий), они восстанавливают сульфаты, вызывая образование H2S. Выделение H2S десульфурирующими бактериями происходит в глубинах морей, поэтому в Черном море на глубине 2500 м содержание H2S доходит до 6,5 мл в 1 л воды. Значительное накопление H2S в результате биологического восстановления серы наблюдается в целебных грязях, в лиманах и других водоемах. В санитарном отношении серобактерии являются важными агентами начальной стадии биологического очищения сточных вод и разложения органических отбросов, содержащих серу. Большинство серобактерий принадлежит к родам Thiobacillus, Sulfolobus и Thiospira. Общая схема круговорота серы представлена на рис. 54. Кроме биологического круговорота серы в атмосфере происходят небиологические превращения ее газообразных форм. Согласно некоторым подсчетам, в атмосферу ежегодно выделяется около 90 млн тонн серы в виде H2S, образующегося биологическим путем. Кроме того, еще 50 млн тонн поступает в атмосферу в виде SO2, образующейся при сжигании топлива, и около 0,7 млн тонн в форме H2S и SO2, возникающих в результате действия вулканов. В атмосфере H2S быстро окисляется до SO2 атомарным (О) и молекулярным (О2) кислородом или озоном (О3). SO2 может растворяться в воде с образованием H2SO3 или окисляться медленно до SO3, которая при растворении в воде превращается в H2SO4. Основная масса H2SO4 вместе с неокисленной H2SO3 возвращается на землю в форме кислоты, которая становится причиной разрушения различных каменных строений, в том числе многих каменных скульптур.
С химической стороны круговорот фосфора достаточно прост, поскольку он встречается в живых организмах только в пятивалентном состоянии в виде свободных фосфатных ионов (РО43 —) или в составе органических фосфатных компонентов клетки. Бактерии не способны поглощать большинство органических фосфорсодержащих соединений, свои потребности в фосфоре они удовлетворяют путем поглощения фосфатных ионов, из которых затем синтезируют органические фосфатные соединения. При разложении гнилостными бактериями белковых веществ одновременно с минерализацией азота происходит превращение органического фосфора в фосфатные ионы. Поскольку большая часть фосфатов, несмотря на быстрый круговорот фосфора, находится в виде нерастворимых солей кальция, железа или алюминия, фосфаты также служат
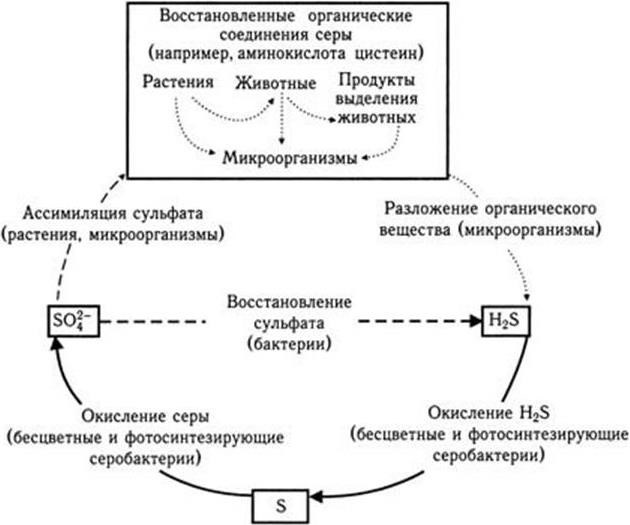
Рис. 54
Окисление атома серы показано сплошными стрелками; восстановление – точечными стрелками; реакции без изменения валентности – пунктирными стрелками
фактором, ограничивающим рост растений. Растворимые фосфаты постоянно переносятся из почвы в море вследствие выщелачивания. Этот перенос имеет однонаправленный характер. Лишь небольшая часть фосфатов возвращается на сушу, главным образом в виде отложений гуано морскими птицами. Поэтому доступность фосфатов для растений зависит от непрерывного перевода в раствор нерастворимых фосфатных отложений – процесса, в котором важную роль играют микроорганизмы. Образуемые ими кислые продукты метаболизма (органические кислоты, а также азотная и серная) растворяют фосфат кальция, а образуемый ими H2S способствует растворению фосфата железа. В круговороте в природе железа большую роль играют железобактерии, для которых железо служит источником окислительного дыхания (донором электронов). Железобактерии окисляют закисные соединения в окисные, а освобождающуюся энергию используют для усвоения углерода из СО2 или карбонатов. Окисление протекает по формуле:
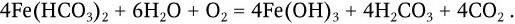
Из железобактерий лучше других изучена не образующая спор подвижная палочка Thiobacillus ferroxidans, которая окисляет и серу. К железобактериям относятся некоторые нитчатые бактерии из рода Leptothrix, а также Gallionella, состоящая из спиральных, закрученных в виде пучков тонких (0,01 – 0,3 мкм) нитей, образующих стебелек, на поверхности которого откладывается гидрат окиси железа. Нитчатые железобактерии в водоемах прикрепляются к различным подводным предметам. Нити бактерий одеты слизистым влагалищем, которое пропитывается гидратом окиси железа. Размножаясь в некоторых озерах в огромных количествах, железобактерии образуют накопления железной руды (например, в Карелии). При размножении в водопроводах железобактерии могут вызывать закупорку просвета труб.
Этапы круговорота различных элементов осуществляются микроорганизмами разных групп. Непрерывное существование каждой отдельной их группы зависит от химических превращений элементов, осуществляемых другими группами микроорганизмов. Разрыв цикла в какой-либо одной точке привел бы к прекращению жизни на Земле. Жизнь непрерывна на Земле потому, что все основные элементы, необходимые для ее проявления (C, N, H, O, P, S), подвергаются циклическим превращениям, во многом благодаря деятельности микроорганизмов.






