Мужское бесплодие
На протяжении последних десятилетий уровень рождаемости становится все менее предсказуемым. Снижение этого показателя продолжается как за счет добровольной бездетности, так и в результате бесплодия.
В мире в среднем 60–80 млн. пар не могут зачать ребенка, среди них 2–10% не имеют возможности иметь естественным путем даже одного ребенка, 10–25% – более одного. Примерно 40% случаев приходится на мужское бесплодие, 40% – на женское, 20% – на смешанное. В 30–75% причины мужского бесплодия остаются невыясненными (идеопатическое).
В России частота бесплодных браков составляет 17,5–29%, что выше критического уровня по ВОЗ (16%). В нашей стране сегодня только официально зарегистрированы 6 млн. бесплодных пар. На самом деле их гораздо больше! Около 25% семейных пар не достигают беременности в течение 1 года, среди них 15% лечатся по поводу бесплодия, но все же менее 5% так и остаются бесплодными.
В 2011 году среди причин расторжения браков бесплодие составляло около 7,5 %. На 2–годах совместной жизни уровень разводов среди бездетных пар в 2–4 раза был выше, чем среди тех, кто имеет детей.
Бесплодие – частая причина потери интереса к жизни, работе, тяжелых психосексуальных и эмоциональных расстройств. Поэтому проблема бесплодия в браке в настоящее время приобрела государственное значение.
Снижение мужской фертильности
Вопрос снижения мужской фертильности сегодня чрезвычайно актуален. Что же нужно делать, чтобы ее сохранить? Исследователи США установили: у тех, кто регулярно занимается спортом не менее 1 часа в день, количество сперматозоидов на 48% больше, чем у мужчин, уделяющих физическим упражнениям гораздо меньше времени.
У представителей сильного пола, тренирующихся на свежем воздухе более 1,5 часов в неделю, на 42% больше сперматозоидов, чем у тех, кто лишает себя активного времяпрепровождения на улице. Причина кроется в воздействии солнечного света, приводящего к увеличению уровня витамина D, повышающего фертильность.
У мужчин, умеренно занимающихся тяжелой атлетикой, сперматозоидов на 25% больше, чем у тех, кто не поднимает тяжести, что может быть связано с необходимым для успешных силовых занятий избытком тестостерона. Учитывая важную роль физических упражнений в поддержании мужской фертильности, в этой книге мы будем много говорить о гимнастике цигун, практиках «Железная рубашка», которые позволят мужчине сохранять здоровье на долгие годы.
Хочу обратить внимание на одну деталь: езда на велосипеде в течение 1,5 часов снижает мужскую фертильность на 34%, что, возможно, связано с давлением на мошонку и повышением температуры в ней. Поэтому мужчинам, планирующим зачатие, этот вид спорта рекомендую исключить из ежедневных тренировок.
Помимо малоподвижного образа жизни, хочу выделить другие причины снижения мужской фертильности:
–неблагоприятные экологические условия;
–отказ от сексуальных контактов;
–избыточное потребление алкоголя.
Классификация мужского бесплодия
По отношению к основному органу репродуктивной системы – яичку выделяются следующие причины мужского бесплодия:
–претестикулярные: гипогонадизм; гиперпролактинемия (повышение уровня пролактина); дефицит тестостерона; патология области гипоталамуса; изолированный дефицит гонадотропинов (синдром Кальмана); изолированный дефицит ЛГ («фертильный евнух») или ФСГ; гипофизарная недостаточность (опухоли, инфильтративные процессы, операции); избыток эстрогенов, андрогенов, глюкокортикоидов; ожирение; сахарный диабет; муковисцидоз; артериальная гипертония;
–тестикулярные: крипторхизм; вирусный орхит (воспаление яичек); перекрут яичка; цитостатическая, цитотоксическая терапия (химиотерапия); радиотерапия; генетические причины (синдром Клайнфельтера – генетическое заболевание, характеризующееся наличием одной или нескольких дополнительных женских половых хромосом Х в мужском кариотипе ХУ, синдром Нунан – наследственное заболевание, характеризующееся низкорослостью и аномалиями общего развития); анорхия (отсутствие яичек); травма; варикоцеле (расширение вен семенного канатика); нарушения синтеза андрогенов;
–посттестикулярные: врожденная аплазия придатка или семявыносящего протока; мюллеровы простатические кисты; обструкция придатка яичка; состояние после операций на мошонке и в паху; нарушения подвижности или функции сперматозоидов при инфекциях, передающиеся половым путем (хламидиозе, уреаплазмозе, микоплазмозе, гонорее, трихомониазе, сифилисе); антиспермальные антитела; сексуальная дисфункция; нарушения транспорта спермы; пережатие семявыводящих путей во время операции по поводу паховой грыжи.
Мужское бесплодие может также возникнуть в результате использования следующих лекарств: амиодарона, циметидина, колхицина, дигоксина, эритромицина, гентамицина, кетоконазола, метотрексата, нитрофурантоина, фенитоина, спиронолактона, сульфасалазина, глюкокортикоидов, а также противораковых препаратов.
В большинстве случаев, после прекращения приема указанных выше препаратов, репродуктивная способность мужчины восстанавливается.
Нормальная работа яичек и выработка активных сперматозоидов может быть нарушена при контакте с пестицидами и промышленными ядами. Наркотики, алкоголь и табак могут привести к временному снижению выработки сперматозоидов в яичках. Как правило, отказ от вредных привычек приводит к восстановлению репродуктивной способности мужчины.
Статистика демонстрирует различия в показателях фертильности разных регионов страны: максимум частоты мужского бесплодия отмечается в Магаданской области (386,5:100000), минимум – в Томской (1,5:100000).
Причины мужского бесплодия в нашей стране по частоте распределяются следующим образом: урогенитальные инфекции – у 32% пациентов, идиопатические нарушения качества эякулята – у 38%, варикоцеле – у 27,4%, иммунный фактор – 18%, неблагоприятные внешние воздействия и врожденные аномалии развития – по 7%, системные заболевания – 5%, эндокринная патология (гипогонадизм) – 2,5%, нарушения эрекции/эякуляции – 0,5%.
О чем расскажет спермограмма?
Основным методом диагностики мужского бесплодия является спермограмма. Сперма для исследования собирается путем мастурбации. Оптимально получение спермы непосредственно в клинике, где будет проводиться анализ. Можно привезти эякулят из дома в специальном транспортном контейнере или в стерильной, герметично закрытой посуде, не позже часа после получения.
Перед сдачей анализа следует воздерживаться от половой жизни 3–5 дней. В этот период нельзя принимать алкоголь, лекарства, посещать баню или сауну. По данным анализа определяют следующие параметры спермы.
Разжижение и вязкость. Сразу после эякуляции сперма густая и вязкая. Обычно в течение 10–30 минут происходит ее разжижение. Вязкая консистенция спермы может препятствовать движению сперматозоидов.
Вязкость определяют через 1 час после получения эякулята. Для этого в него опускают стеклянную палочку, затем поднимают и измеряют длину образующейся нити. В норме она не должна превышать 2 см. Повышенная вязкость может быть одним из факторов бесплодия.
Объем. В норме у здорового мужчины после 3–5 дневного полового воздержания объем эякулята колеблется от 1,5 до 6 мл.
Запах. Наличие неприятного запаха говорит о гнойно-воспалительных процессах в половых органах.
Цвет. Нормальный эякулят имеет мутный молочно-белый или серовато-желтый цвет. Степень мутности зависит от количества сперматозоидов.
Рh. В норме реакция эякулята слабощелочная, рh колеблется в пределах 7,2–8,0. Постоянная слабощелочная реакция обеспечивает активную подвижность сперматозоидов и частично компенсирует кислую среду влагалища до проникновения сперматозоидов в цервикальную слизь.
Лейкоциты. В 1 мл нормального эякулята содержится максимально не более 1 млн. лейкоцитов. При воспалении их количество резко возрастает. Сперма при этом может приобретать желтоватый или зеленоватый оттенок.
Эритроциты. При появлении крови сперма окрашивается в розовый, красный, бурый или коричневый цвет.
Агрегация – хаотическое скопление неподвижных сперматозоидов, нагромождение их на комочки или тяжи слизи, клеточные элементы и детрит.
Липоидные тельца – мелкие блестящие зернышки, содержащиеся в нормальной сперме в большом количестве. При длительном воспалении липоидные тельца могут исчезнуть из спермы.
Слизь в нормальном эякуляте отсутствует. Появляется она при воспалении мужских половых органов.
Агглютинация – это склеивание подвижных сперматозоидов между собой головками, хвостами или смешанно (головки с хвостами).
Вопрос. Планируем ребенка уже третий год. У мужа при обследовании спермы все показатели в норме, кроме агглютинации (++). После приема антибиотиков не может быть такого побочного эффекта? Возможно ли зачатие естественным путем с такими показателями?
У здоровых мужчин агглютинация у сперматозоидов отсутствует. Агглютинация «1+» расценивается как слабо выраженная; «2+» – значительная; «3+» – резко выраженная; «4+» – тяжелая степень агглютинации, при которой все подвижные сперматозоиды находятся в склеенном состоянии. Агглютинация позволяет предположить наличие иммунологического фактора бесплодия и требует выполнения дополнительного обследования.
Подвижность и морфология сперматозоидов: как оценить?
Помимо описанных общих характеристик спермы, основной составляющей частью спермограммы является микроскопический анализ эякулята, при котором определяют характеристики самих сперматозоидов: количество, подвижность и строение. В настоящее время нормальными считаются следующие показатели спермограммы:
–объем эякулята – 1,5 мл и более;
–общее количество сперматозоидов – 39 миллионов и более;
–концентрация сперматозоидов в 1 мл – 15 миллионов и более;
–общая подвижность сперматозоидов – 40% и более;
–сперматозоидов с прогрессивным движением – 32% и более;
–жизнеспособность – 58% и более;
–нормальных форм – 20% и более.
Вопрос. Мы с мужем получили заключение спермограммы. Но в ней ничего не понятно. В заключении указано, что у мужа «астенозооспермия». Объясните, пожалуйста, что это такое? И можем ли мы забеременеть?
Достаточно часто пациентам становится непонятным заключение спермограммы. Предлагаю рассмотреть основную терминологию, которая применяется при ее описании.
Олигоспермия – снижение объема эякулята. У здоровых она может наблюдаться при слишком частых половых актах и эпизодах мастурбации, а также у лиц старше 60 лет. Об истинной олигоспермии можно говорить только при условии исследования после 4–5-дневного воздержания от любых форм семяизвержения перед получением спермы.
Нормозооспермия – все показатели в пределах нормативных значений.
Олигозооспермия – уменьшение количества зрелых сперматозоидов в эякуляте.
Полиспермия – увеличение объем эякулята.
Астенозооспермия (или дискинезия) – снижение подвижности сперматозоидов.
Тератозооспермия – изменение строения и формы сперматозоидов.
Олигоастенотератозооспермия – нарушение всех трех показателей качества сперматозоидов (снижение концентрации, подвижности, морфологии).
Криптоспермия – единичные сперматозоиды в эякуляте.
Некроспермия – мертвые сперматозоиды в эякуляте.
Полизооспермия – концентрация сперматозоидов выше нормы.
Азооспермия – сперматозоиды в эякуляте отсутствуют.
Важно понимать, что заключение спермограммы не является диагнозом, а лишь отображает некоторые параметры спермы.
Половые инфекции и мужской фактор
Вопрос. Помогите, пожалуйста. Мы с мужем очень хотим ребенка, обследовались оба, инфекций нет. Вот только у мужа спермограмма плохая. Сказали, что высокая концентрация лейкоцитов – 3,5 млн, и низкая подвижность сперматозоидов – 45% неподвижных. Врач сказала, что при таких показателях трудно забеременеть. Правда ли это?
Чтобы выявить причины нарушения сперматогенеза в данном клиническом случае необходимо сделать расширенную спермограмму, сдать анализ крови и посев из уретры на половые инфекции, а также проверить концентрацию половых гормонов. Обследование и лечение мужчин проводится андрологом или урологом.
Вопрос. У моего мужа плохая сперма. При обследовании нашли уреаплазму. Может ли это заболевание делать неподвижными сперматозоиды?
У мужчин первыми проявлениями уреаплазмоза чаще всего являются признаки поражения мочеиспускательного канала (уретрита). Инфекция может постепенно распространяться на внутренние половые органы. В первую очередь поражаются предстательная железа и придатки яичка – развивается простатит и эпидидимит.
При этом снижается половая функция мужчины и развивается бесплодие из-за разрушения сперматозоидов в результате длительного воспалительного процесса, а также по причине снижения их двигательной активности под воздействием ферментов, выделяемых уреаплазмами.
Уреаплазмоз у мужчин диагностируют: методом полимеразной цепной реакции (ПЦР), основанной на выявлении ДНК уреаплазм; иммуноферментного анализа (ИФА), позволяющего определить антитела к возбудителю инфекции; при помощи посева отделяемого или соскоба из уретры на специальные питательные среды с одновременной оценкой чувствительности возбудителя к антибиотикам. Правильно подобранная комплексная антибактерильная и противовоспалительная терапия уреаплазмоза повышает шанс зачать ребенка.
Вопрос. У моего мужа недавно обнаружили небольшое воспаление простаты. Муж ходил к урологу-андрологу, тот назначил курс лечения – процедуры и антибиотики. Доктор сказал, что пока муж лечится, нужно предохраняться. Мне уже 25, уже очень хочется стать мамой, но никак не получается. Начинаю уже впадать в панику. Ответьте, пожалуйста, можно нам не предохраняться при приеме лекарств? Заранее большое спасибо!
Надо набраться терпения и окончить курс лечения прежде, чем приступать к зачатию. После завершения курса желательно сдать контрольные анализы.
Иммунологический фактор мужского бесплодия
Иммунная система играет важную роль в репродукции человека. Изменение иммунного гомеостаза может вызывать снижение способности к зачатию.
Одним из таких факторов, приводящих к бесплодию, является образование антиспермальных антител (АСАТ). Они обнаруживаются у каждой третьей бесплодной пары.
Антиспермальные антитела образуются в различных отделах репродуктивного тракта мужчин (в яичках и их придатках, семявыносящих протоках) и направлены против антигенов, расположенных на разных частях сперматозоида: головке, хвосте, средней части или их комбинации.
В норме антитела на свои собственные клетки (сперматозоиды) вырабатываться не должны, так как последние защищены от «всевидящего ока» иммунной системы так называемым гематотестикулярным барьером – физиологическим «фильтром» между семенными канальцами, где производятся и обитают сперматозоиды, и кровеносными сосудами, в которых циркулируют представители иммунной системы, способные вычислить «чужаков».
При нарушении гематотестикулярного барьера циркулирующие иммунные клетки могут проникать в мужской генитальный тракт. В ответ на обнаружение «чужеродных» клеток, к которым иммунная система относит сперматозоиды, вырабатываются антиспермальные антитела, которые вызывают склеивание (агглютинацию) сперматозоидов и их гибель.
Факторами риска продукции АСАТ у мужчин являются:
–травма;
–варикоцеле (расширение вен, окружающих семенной канатик);
–половые инфекции;
–онкологические заболевания мужских половых органов;
–крипторхизм (неопущение яичка в мошонку);
–хирургические операции на половых органах.
Выявляем антиспермальные антитела
В последнее время, учитывая возрастающую роль иммунного фактора «мужского» бесплодия, ВОЗ рекомендует в качестве рутинного скрининга проводить расширенную спермограмму, включающую MAR-тест (смешанный антиглобулиновый тест) на наличие антиспермальных антител.
MAR-тест позволяет оценить соотношение нормальных сперматозоидов, покрытых антиспермальными антителами, к общему количеству сперматозоидов, а также показывает процент выключенных из оплодотворения сперматозоидов, которые в стандартной спермограмме расцениваются как абсолютно нормальные.
Дополнением к расширенной спермограмме является определение АСАТ в плазме крови. Подобный анализ имеет особую важность при азооспермии – отсутствии сперматозоидов в сперме. АСАТ могут принадлежать к разным классам иммуноглобулинов (Ig G): M, G, A. Наиболее важным является определение Ig G, которые легко проходят через биологические барьеры, и IgA.
Выявление при MAR-тесте Ig G или/и Ig A в суммарном количестве менее 10% считается нормой; от 10% до 50% – расценивается как слабоположительный; более 50% – как положительный тест.
Обязательным является определение антиспермальных антител у пар, готовящихся к экстракорпоральному оплодотворению ЭКО. Если у мужчины высокий титр антиспермальных антител, особенно на головке сперматозоидов, паре могут предложить интрацитоплазматическая инъекция сперматозоида (ИКСИ) в яйцеклетку, для которой специалисты отбирают единичный сперматозоид, имеющий наилучшие характеристики, и помещают его внутрь яйцеклетки.
Несовместимость партнеров
Антиспермальные антитела могут производиться не только у мужчин, но и у женщин. При этом АСАТ вырабатываются в цервикальной слизи, препятствуя продвижению сперматозоидов, которые воспринимаются как чужеродные и уничтожаются.
Обнаружение антиспермальных антител в шейке матки указывает на их наличие и в других отделах репродуктивного тракта – в полости матки и в просвете маточной трубы. То есть антиспермальные антитела у женщины влияют не только на прохождение сперматозоидов через шейку матки, но и резко ухудшают качество оплодотворения.
Они вмешиваются в процесс взаимодействия половых клеток, не позволяя сперматозоиду проникнуть сквозь оболочку яйцеклетки. АСАТ подавляют акросомальную реакцию сперматозоидов, которая является необходимым условием успешного оплодотворения. При таких обстоятельствах зачатие является весьма затруднительным.
Для изучения совместимости партнеров и диагностики иммунологических форм бесплодия, связанных с выработкой АСАТ, проводят посткоитальный тест в одном из двух вариантов:
1. проба Шуварского – Симса – Хюнера (in vivo – внутри живого организма); пациентка приезжает на исследование через 3–12 ч после полового акта в дни, предшествующие овуляции; исследуется содержимое влагалища и шейки матки; при снижении подвижности сперматозоидов в половых путях женщины тест считается отрицательным («плохим»);
2. проба Курцрока – Миллера (in vitro – вне живого организма); супруги приезжают на исследование в дни, предшествующие овуляции; муж сдает сперму, а у жены берется капелька слизи шейки матки; оценивается взаимодействие сперматозоидов и слизи шейки матки под микроскопом; отрицательным («плохим») результатом теста является снижение поступательного движения сперматозоидов в слизи шейки матки.
При проведении посткоитального теста нередко обнаруживается явление «дрожания на месте» сперматозоидов, покрытых антиспермальными антителами. Предполагается, что наличие этого признака обусловлено взаимодействием антител с мицеллами цервикальной слизи.
Следует помнить, что самой частой причиной отрицательного посткоитального теста является наличие АСАТ в сперме, а не в шейке матки. Нередко наблюдается сочетание неблагоприятных мужских и женских иммунных факторов.
Посткоитальный тест является одним из самых «капризных» тестов в обследовании на бесплодие и дает довольно большой процент ложных результатов. Поэтому желательно провести дополнительный анализ на определение титра антиспермальных антител как в слизи шейки матки (непрямой MAR-тест), так и в плазме крови обоих партнеров.
Свободные радикалы и здоровье человека
Все формы жизни стремятся к поддержанию среды внутри своих клеток. Внутриклеточный баланс сохраняется благодаря постоянному притоку энергии. Для ее получения и высвобождения нужен кислород. Окисляя органические соединения, поступающие с пищей, этот газ дает нам энергию и жизненные силы.
В тоже время кислород может вызывать нежелательные реакции. Именно он заставляет ржаветь железо, а масло – становиться прогорклым. В нашем организме кислород способен окислять молекулы до активных форм – свободных радикалов, которые в небольшом количестве необходимы для участия во многих физиологических процессах.
Однако в некоторых ситуациях количество свободных радикалов начинает расти сверх нормы. И они становятся нашими врагами, так как разрушают молекулы, клетки, ДНК.
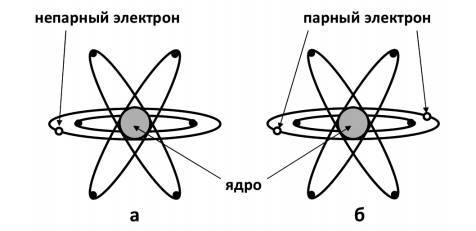
Свободные радикалы на внешней электронной оболочке имеют непарный электрон (рис. 20 а), что делает их чрезвычайно активными – они стремятся отнять его у других молекул, окисляя любые соединения.
Рисунок 21. Свободный радикал (а) и нормальный атом (б)
Перечислю свободные радикалы нашего организма:
–супероксид (02);
–перекись водорода (Н202);
–хлорноватистая кислота (HOCI);
–пероксинитрит (ONOO).
Свободные радикалы могут образовываться внутри организма при нарушении процессов метаболизма (сахарном диабете, хронической обструктивной болезни легких, язвенной болезни, артериальной гипертензии, ишемической болезни сердца, хронической почечной недостаточности, ожирении), а также попадать извне. Вот основные их источники:
–митохондрии – «энергетические станции» клетки; свободные радикалы формируются в процессе получения энергии из углеродов;
–внутренняя выстилка (эндотелий) сосудов, бронхов и пр.;
–тромбоциты и лейкоциты;
–продукты обмена веществ в толстом кишечнике;
–солнечное и радиационное излучения;
–загрязненный воздух;
–просроченная, испорченная еда.
Курение, алкоголь, стрессы, неправильное питание и долгое пребывание на солнце увеличивают количество свободных радикалов, а правильный образ жизни, полноценный отдых, занятия цигун и рациональное питание, наоборот, снижают их активность.
Перекисное окисление
Основной проблемой переизбытка свободных радикалов является перекисное окисление до конечных продуктов – перекисей. Окисляя ненасыщенные жирные кислоты, из которых состоят мембраны живых клеток, свободные радикалы, тем самым, повреждают их.
Так возникает окислительный стресс (ОС) – несостоятельность антиоксидантной системы организма, при которой клетки подвергаются чрезмерному воздействию молекулярного кислорода или свободных радикалов.
Окислительный стресс возникает при избыточном поступлении и/или нарастающем образовании внутри организма свободных радикалов и преобладании окислительных реакций над восстановительными.
Нарушается функция «зараженной» клетки, она теряют способность поглощать питательные вещества и кислород, но при этом хорошо пропускает болезнетворные бактерии и токсины. Такие клетки мало живут, плохо делятся и дают слабое «болезненное» потомство.
Клетка использует окисление для выработки энергии, но при большом количестве оксидантов разрушаются ее органеллы, и наступает истощение. Клетка как завод, обеспечивающий жизнь всего организма. ОС нарушает важнейшие процессы в клетке, заставляя ее paботать на резервных уровнях.
Свободные радикалы повреждают ДНК клетки, что приводит к изменениям в структуре генов, возникают мутации, образуются опухоли. Свободные радикалы взаимодействуют и с белком, в результате клетка стареет.
Доказано, что ОС причастен к развитию таких болезней, как: рак, атеросклероз, инфаркт, инсульт, ишемия, атеросклероз, заболевания нервной и иммунной систем и заболевания кожи.
Антиоксиданты спермы
Как мы уже сказали, эякулят взрослого здорового мужчины кроме сперматозоидов содержит антиоксиданты для защиты сперматозоидов от ОС.
Вот основные компоненты антиоксидантной система спермы: цинк, аскорбиновая и лимонная кислота, фруктоза, ?-токоферол, пируват, глутатион, L-карнитин, таурин и гипотаурин, урат, пируват, альбумин, бета-каротины и убиквинол.
Антиоксиданты поддерживают активность таких ферментов спермы, как супероксиддисмутаза, каталаза и глутатионпероксидаза. Их дефицит вызывает повреждение ДНК спермотозоидов и мужское бесплодие.
Поэтому в изучение качества эякулята должно входить измерение активных форм кислорода (АФК) – свободных радикалов в суспензии сперматозоидов; а также оценка хроматина сперматозоидов (нарушения упаковки, фрагментация ДНК).
Окислительный стресс в яичках
Окислительный стресс (ОС) в яичках является результатом дисбаланса между выработкой свободных радикалов и их захватом семенными антиоксидантами.
Семенной ОС повреждает ДНК сперматозоидов. У 25% бесплодных пациентов выявляются более высокие уровни свободных радикалов (АФК) в сперме по сравнению с фертильными мужчинами.
Выработка свободных радикалов незрелыми зародышевыми клетками и лейкоцитами в небольшом количестве необходима для активации спермы, акросомной реакции и естественного оплодотворения. Избыток АФК вызывает перекисное окисление липидов мембраны клеток, потерю подвижности сперматозоидов и повреждение их ДНК.
Сперматозоиды особенно чувствительны к окислительному повреждению (рис. 22) из-за содержания в них большого количества полиненасыщенных жирных кислот. Они обеспечивают подвижность сперматозоида и слияние его с яйцеклеткой.
Рисунок 22. Влияние окислительного стресса на сперматозоиды
При накоплении свободных радикалов возникает перекисное окисление липидов в цитоплазматической оболочке сперматозоидов, что сопровождается потерей подвижности, повреждением ДНК и последующим генетическим нарушениям.
ОС имеет место в среднем у 38–50% больных с нарушениями качества спермы. Хронический бактериальный простатит приводит к увеличению продукции свободных радикалов в сперме в среднем в 15 раз; антиспермальные антитела – в 1,8–8 раза; варикоцеле – в 1,9 раза; действие хлорорганических поллютантов и других вредных веществ окружающей среды – в 1,2–1,5 раза.
Поэтому в комплексной терапии мужского бесплодия особенно важно использовать антиоксиданты, эффективность которых была известна еще три тысячелетия назад.