Приложение 3. Дыхательная цепь
Термин «дыхательная цепь» означает последовательность реакций, ответственных за перенос атомов водорода или электронов от субстратов дыхания к молекулярному кислороду. Различают два типа дыхательных цепей: сопряженные с трансформацией энергии и не сопряженные с ней. Биологическое значение дыхания первого типа прояснилось благодаря работам В.А. Энгельгардта, открывшего в начале 1930-х гг. дыхательное фосфорилирование. Что касается дыхания второго типа, то первые указания на его активную роль были получены почти на 30 лет позже. Концепция, предполагающая, что несопряженное дыхание может быть биологически полезным, была сформулирована одним из авторов этой книги (В.П.С.) в 1960 г.
В клетках эукариот дыхание, сопряженное с трансформацией энергии, локализовано во внутренней мембране митохондрий. У дышащих бактерий тот же процесс обнаруживается в цитоплазматической мембране, мезосомах или тилакоидах.
Основным источником энергии для жизни на Земле является энергия солнечного света. Такие автотрофные организмы, как цианобактерии и растения, используют энергию квантов света для осуществления двух одновременно протекающих процессов, а именно — для запасания энергии в виде трансмембранной разницы электрохимического протонного потенциала (с последующим ее преобразованием в АТФ) и для разложения воды и переноса полученных электронов на NADP+. В ходе последнего процесса также запасается значительное количество энергии, но уже в виде разности окислительновосстановительных потенциалов, так как редокс-потенциал пары NADP+/NADPH (E0'= -320 мВ) значительно более отрицателен по сравнению с парой О2/Н2О (E0'= +820 мВ). Образованные в ходе фотосинтеза АТФ и NADPH используются для превращения углекислого газа в углеводы и далее для синтеза белков, жиров, нуклеиновых кислот, т. е. всех компонентов, необходимых для построения клетки. Гетеротрофные организмы не способны напрямую использовать энергию света, и поэтому основным доступным для них источником является энергия, накопленная растениями прежде всего в виде углеводов. По существу они обращают реакции фотосинтеза. При этом сначала окисляются углеродные атомы углеводов, жирных кислот и аминокислот до СО2 (гликолиз и цикл Кребса и ?-окисление жирных кислот), а полученные таким образом электроны используются для образования NADH. Далее NADH окисляется молекулярным кислородом с образованием воды. NADH-оксидазная реакция сопровождается выделением очень большого количества свободной энергии (порядка 1,1 электрон-вольта при переносе одного электрона с NADH на кислород), которая может быть запасена дыхательной цепью в виде трансмембранной разности электрохимических потенциалов ионов H+. Величина протон-движущей силы на биологических мембранах обычно составляет около 200 мВ, так как при больших величинах электрического потенциала возможен пробой липидного бислоя и утрата запасенной энергии. Показано, что запасание энергии NADH-оксидазной реакции осуществляется путем переноса электрона с NADH на кислород, сопряженного с транслокацией пяти протонов через мембрану. При этом NADH-оксидазная реакция разбита на несколько этапов (в митохондриях животных и человека таких этапов три). Сначала два электрона с NADH переносятся на убихинон NADH-^Q- редуктазой (комплексом I), затем полученный убихинол окисляется цитохромом с посредством CoQH2-цитoхpом с-редуктазы (комплекса Ьс1, или комплекса III) и в завершение восстановленный цитохром с окисляется молекулярным кислородом под действием цитохромоксидазы (комплекса IV). Активность всех этих трех ферментных комплексов сопряжена с генерацией протонного потенциала.
Как показано на рис. П-3.1, последовательность реакций дыхательной цепи начинается окислением NADH. В процессе участвует несколько редокс-центров NADH-CoQ-редуктазного комплекса: FMN и группа [Fe-S] кластеров. NADH-CoQ-редуктаза восстанавливает C0Q.
Полученный C0QH2 окисляется системой Q-цикла, включающей [Fe-S] кластер комплекса III (Fe-SIII Риске), цитохром с1 и два гема цитохрома b (высокопотенциальный Ьн и низкопотенциальный Ьь).
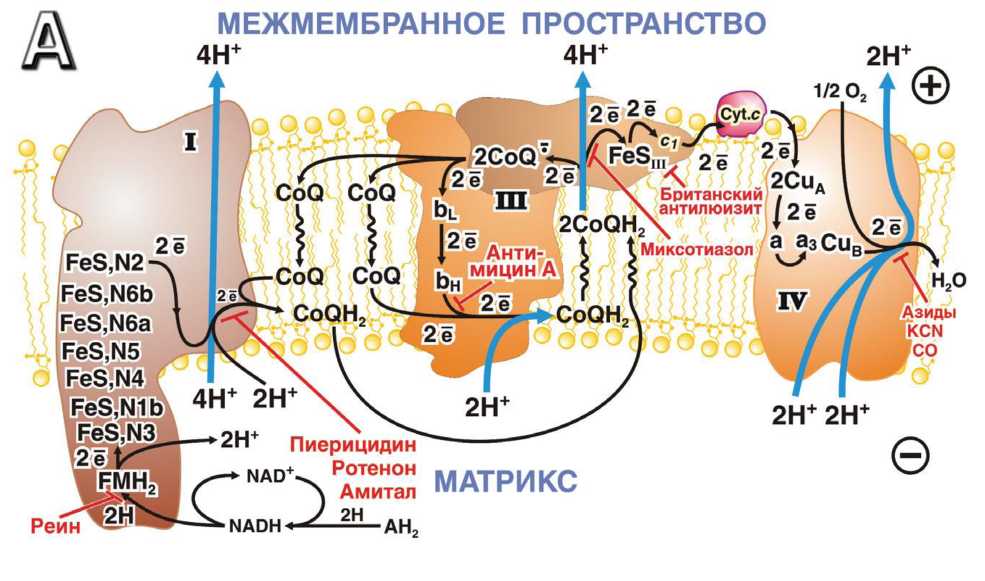
Рис. П-3.1.
Непосредственным акцептором электронов для C0QH2 служит Fe-SIII. От Fe-SIII электроны поступают на цитохром cl и далее на цитохром с. Последний используется как восстановитель конечного фермента дыхательной цепи — цитохромоксидазы, имеющей в своем составе два гема (а и аз) и три атома меди. Цитохромоксидаза восстанавливает кислород до воды. Процесс окисления одной молекулы NADH кислородом сопряжен с переносом 10 протонов из митохондриального матрикса (у бактерий — из цитоплазмы) в межмембранное пространство митохондрий (у грамотрицательных бактерий — в периплазму, а у грамположительных — во внешнюю среду). Образованный мембранный потенциал далее расходуется на синтез АТФ при помощи так называемого комплекса V (протонной АТФ-синтазы) либо на совершение некоторых других типов полезной работы.
Описанное выше многокомпонентное устройство дыхательной цепи, помимо обеспечения высокой стехиометрии Н+/О2, имеет еще ряд дополнительных преимуществ. Прежде всего, это придает ей известную гибкость в использовании субстратов с разными окислительновосстановительными потенциалами. Восстановительные эквиваленты могут поступать в дыхательную цепь на различных ее уровнях в зависимости от редокс-потенциала окисляемого субстрата. Если этот потенциал оказывается меньше, равен или лишь немногим больше -320 мВ (редокс-потенциал пары NADH/NAD+), то в окислении такого субстрата может участвовать вся дыхательная цепь. Именно так окисляется большинство субстратов дыхания. Если редокс-потенциал субстратов окисления намного отрицательней такового пары NADH/NAD+, то в систему переноса электронов может быть включен специальный механизм накопления энергии еще до дыхательной цепи. Такого типа реакции относят к разряду процессов трансформации энергии на уровне субстрата, или субстратного фосфорилирования. Если редокс-потенциал субстрата значительно более положительный, чем у пары NAD+/NADH, то восстановительные эквиваленты с такого субстрата переносятся на средний или конечный участок дыхательной цепи. Так окисляется один из субстратов цикла Кребса — сукцинат (редокс-потенциал +30 мВ), а также ацил-СоА — субстрат первой оксидоредукции в системе ?-окисления жирных кислот. И сукцинат, и ацил-СоА-дегидрогеназы подают электроны в дыхательную цепь, минуя комплекс I, т. е. переносят электроны сразу на убихинон. В очень редких случаях редокс-потенциал окисляемого субстрата более положителен, чем даже у C0Q. Тогда восстановительные эквиваленты входят в цепь на уровне цитохрома с, так что только цитохромоксидазный генератор участвует в трансформации энергии. Примером может служить окисление аскорбиновой кислоты у животных или окисление метанола, ионов Fe2+ или нитрита у различных бактерий.






