Глава 6. Диагностика СИБР тонкой кишки у пациентов с НБЗ и после ее хирургической коррекции – первые результаты
(В. Л. Мартынов, А. Г. Семенов, Н. В. Казарина, А. А. Тулупов, А. А. Чесноков)
Недостаточность баугиниевой заслонки (НБЗ) широко распространена среди населения. При изучении 900 протоколов ирригоскопий, выполненных по различным показаниям и не связанных с диагностическим поиском недостаточности баугиниевой заслонки, НБЗ была выявлена у 64 % пациентов как сопутствующая находка (Мартынов В. Л., 2013).
Широкое распространение НБЗ среди населения России обусловлено дисплазией соединительной ткани (ДСТ) и обширным спектром заболеваний толстой кишки и терминального отдела тонкой кишки, определяющие, соответственно, первичную и вторичную НБЗ (Мартынов В. Л., 2006).
Заболевания желудочно-кишечного тракта (ЖКТ) занимают видное место в структуре патологии внутренних органов, в России они составляют около 2500 на 100 тыс. населения (Филиппова Т. В., 2014). В последние годы большое внимание уделяется функциональным заболеваниям органов пищеварения, что объясняется прежде всего их высокой распространенностью и теми затратами, которые несет здравоохранение в связи с обследованием и лечением таких больных (Шептулин А. А., 2010). Ведущие специалисты говорят о том, что синдромом раздраженного кишечника (СРК) страдают от 10 до 20 % взрослого населения развитых стран, что составляет до 50 % от всех посещений гастроэнтеролога (Sperber A. D, 2012).
Согласно последним исследованиям частота ДСТ среди подростков достигает до 20 % (в когорте около 3000 исследуемых, по данным проф. Нечаевой Г. И., 1980–2010); и 8,5 % в выборке из 400 взрослых человек (Нечаева Г. И., 2009).
По нашим данным (Мартынов В. Л., 2006, 2013) проведение классической аппендэктомии, а тем более проведение аппендэктомии с техническими трудностями и аппендэктомии в условиях осложненного течения острого аппендицита, может приводить к несостоятельности баугиниевой заслонки. Факт интимной анатомической и функциональной близости клапанных структур илеоцекального перехода и аппендикса неоспорим. Аппендэктомия разрушает эти связи, и приводит к развитию вторичной приобретенной НБЗ.
Многими авторами (Oren Zaidel, 2003; Ардатская М. Д., 2001; Larry S Miller, 2012) признается факт восходящего ретроградного инфицирования слизистой тонкой кишки при НБЗ. Патологическое состояние, при котором титр микроорганизмов слизистой тонкой кишки превышает 105 КОЕ / мл, либо происходит заселение толстокишечной флорой получило название Синдром избыточного бактериального роста (СИБР) (Small Intestinal Bacterial Overgrowth syndrome – SIBO).
СИБР – это патологическое состояние, развивающееся вследствие бактериальной контаминации тонкой кишки различной микрофлорой и сопровождающееся функциональными нарушениями работы пищеварительного конвейера (Кучерявый Ю. А., 2010; Маев И. В., 2011).
Прямым доказательством возникновения СИБР при несостоятельности баугиниевой заслонки (НБЗ) является опыт Larry S Miller (2012). В клиническом эксперименте автор моделировал недостаточность илеоцекального клапана путем заведения 4-х просветного зонда за губы баугиниевой заслонки в направлении подвздошной кишки 19 здоровым волонтерам при проведении колоноскопии. Через 1 месяц после манипуляции с помощью водородного дыхательного теста у всех исследуемых выявлен синдром избыточного бактериального роста тонкой кишки. Таким образом, фактически разрушив баугиниевую заслонку, автор добился возникновения СИБР у волонтеров.
В настоящее время СИБР признается ключевым патогенетическим механизмом в развитии и персистировании многих заболеваний пищеварительного тракта и ассоциированных внепищеварительных состояний (бронхиальная астма, дерматологические атопии, сахарный диабет, аутоимунные аллергические состояния, артриты, облигатные предраковые состояния и т. д.).
Реальная распространенность СИБР на сегодняшний день неизвестна. Клинически это патологическое состояние плохо диагностируемо ввиду неспецифичности его симптомов, которые часто относят к основному производящему СИБР заболеванию (Bures J., 2010). Фактически СИБР чрезвычайно распространен в присутствии одного или более предрасполагающих патологических состояний. Так, Ардатская М. Д. (2011), указывает на то, что частота выявления избыточного роста бактерий в тонкой кишке при различных заболеваниях (хронический гастрит, язвенная болезнь, хронический холецистит, патология гепатобилиарной системы, воспалительные и др. заболевания кишечника (в т. ч. синдром раздраженного кишечника), склеродермия, нейропатия (как осложнение сахарного диабета), последствия хирургического вмешательства и пр.) составляет 40–99 %. Результаты последнего мета-анализа (Ford A. C., 2009), включающего 11 исследований, показали, что патологические дыхательные тесты значительно чаще регистрируются у больных с СРК, чем у здоровых лиц (OР=4,46; 95 % ДИ=1,69–11,80). Аналогичные результаты достигнуты и во втором мета-анализе, опубликованном годом позже, – патологические результаты тестов достоверно чаще встречались у пациентов с СРК: отношение шансов (ОШ) 4,46, 95 % доверительный интервал (ДИ) 1,69–11,80. При этом учет возраста и пола продемонстрировал еще более значимый результат (OШ 9,64, 95 % ДИ 4,26–21,82) (Кучерявый Ю. А., 2014).
По данным литературы проблема СИБР в настоящее время является сугубо терапевтической. Лечение синдрома избыточного роста бактерий в тонкой кишке предусматривает терапию основного заболевания, заместительную терапию синдрома мальабсорбции и антибактериальную терапию (Авдеев В., 2010; Кучерявый Ю. А., 2014).
Основная группа препаратов, используемая при СИБР – внутрикишечные антибиотики (Плотникова Е. Ю., 2013; Полуэктова Е. А., 2013; Кучерявый Ю. А., 2010). Стоит признать, что при отсутствии воздействия на причину успешное патогенетическое лечение является временным, что подтверждается на примере терапии рифаксимином. Частота рецидива СИБР после эффективной терапии рифаксимином достигала 44 % спустя 9 месяцев (Gabrielli M., 2011).
Многие авторы (Кучерявый Ю. А., 2014; Lauritano E. C., 2008) отдельно останавливаются на очевидном выводе – прогноз СИБР и риск его рецидива после успешной антибиотикотерапии зависит, прежде всего, от терапевтического воздействия на первичное фоновое заболевание, которое способствовало контаминации тонкой кишки. Gabrielli M. (2013) справедливо указывает, что рецидив СИБР в случае сохранения предрасполагающих причин часто приводит к хронизации процесса и сложной, а порой невозможной, консервативной коррекции.
Таким образом, мы не встречали литературных данных, где описывалась бы этиотропная терапия. На наш взгляд проблема СИБР у больных с функциональной патологией ЖКТ во многих случаях обусловлена повреждением конкретной анатомической структуры, а именно, баугиниевой заслонки и является проблемой хирургической.
Мы не встречали отечественных исследований, посвященных проблеме этиотропного воздействия на синдром избыточного бактериального роста у пациентов с доказанной недостаточностью баугиниевой заслонки. Немногочисленные зарубежные работы (Oren Zaidel, 2003; Larry S Miller, 2012) посвящены лишь констатации факта наличия СИБР при НБЗ.
Поэтому нами поставлена была цель исследования – определение синдрома избыточного бактериального роста тонкой кишки у пациентов с доказанной недостаточностью баугиниевой заслонки и после ее хирургической коррекции.
Исследование проводилось на базе хирургического отделения ГБУЗ НО «Городская клиническая больница № 12 г. Нижнего Новгорода» в период с сентября 2014 г. по декабрь 2014 г. В основную группу вошли 20 пациентов (16 женщин, 8 мужчин, возраст от 23 до 57 лет) с доказанной по результатам ирригоскопии недостаточностью баугиниевой заслонки. Всем пациентам основной группы выполнена баугинопластика по методикам проф. Мартынова В. Л. Также сформирована контрольная группа из 20 пациентов (11 женщин 9 мужчин, возраст от 28 до 49 лет), которым с целью диагностики болезней толстой кишки была проведена ирригоскопия, по результатам которой илеоцекальный клапан оказался состоятельным.
Симультанно пациентам основной группы выполнялась аппендэктомия. Удаленный червеобразный отросток направлялся на гистологическое исследование. В случае интраоперационной диагностики мезаденита брыжейки подвздошной кишки измененный лимфоузел резецировался, выполнялся бакпосев со среза лимфоузла и его гистологическое исследование.
Подготовка к ирригоскопии производилась двое суток и заключалась в запрещении приема пищи, содержащей шлаки, в постановке высоких клизм общим объемом от 1,5 до 3 литров 3–4 раза в день. Обязательным является тщательное опорожнение слепой кишки от кишечного содержимого, так как наличие его в виде замазкоподобной массы может препятствовать прохождению рентгеноконтрастного вещества в подвздошную кишку при несостоятельности баугиниевой заслонки. Это может привести к ложноотрицательному заключению. Необходимо тугое наполнение слепой кишки рентгеноконтрастным веществом. Принципиально важным является повторное рентгенологическое исследование после дефекации, так как во время дефекации в кишке создается максимальное давление, что при несостоятельности илеоцекального запирательного аппарата будет сопровождаться выраженным забросом рентгеноконтрастного вещества в подвздошную кишку.
Нами интраоперационно проводилась дигитальная диагностика недостаточности баугиниевой заслонки. В норме щель тонко-толстокишечного перехода не более 2 см и не пропускает первый палец левой кисти хирурга. В условиях НБЗ в среднем этот переход имеет диаметр 3–3,5–4 см, что определяет почти беспрепятственное прохождение 1 пальца левой кисти (так удобно) хирурга в подвздошную кишку. Методика заключается в следующем: после выделения илеоцекального угла из правой подвздошной ямки хирург 1 пальцем левой кисти приближает участок латеральной стенки восходящей ободочной кишки, расположенный напротив илеоцекального соустья, к данному соустью и пытается внедрить его и палец в подвздошную кишку. При его внедрении в подвздошную кишку, по нашему мнению, диагноз НБЗ установлен. При невозможности выполнения данной манипуляции диагноз НБЗ можно отвергнуть.
С целью определения синдрома избыточного бактериального роста в тонкой кишке у пациентов основной группы выполнялись прямые и косвенные методы диагностики.
Прямой интраоперационный метод диагностики СИБР тонкой кишки – бактериологическое исследование аспирата внутрипросветного и мукозного содержимого дистального отдела подвздошной кишки (рис. 32). Методика забора материала заключается в следующем: в 20 см проксимальнее илеоцекального перехода после изоляции мягкими кишечными жомами участка петли подвздошной кишки длинной 10 см производится пункция ее просвета. Игла проводится косо относительно стенки кишки, в полость кишки вводится 10 мл стерильного физиологического раствора NaCl. Выдерживается экспозиция 5 мин., содержимое изолированного участка подвздошной кишки аспирируется, вплоть до прохождения иглы через слизистый слой кишки, игла извлекается. Место пункции перитонизируется. Аспират направляется на бактериологическое исследование.
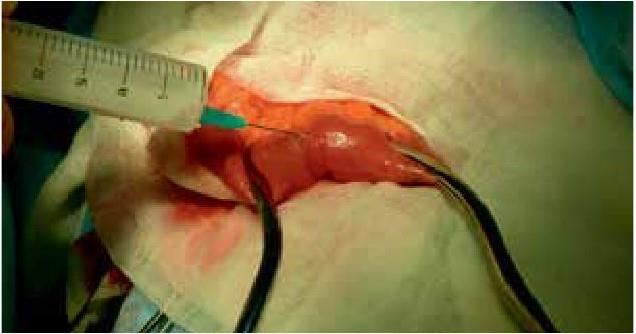
Рис. 32. Интраоперационный забор смыва внутрипросветного и мукозного содержимого дистального отдела подвздошной кишки с последующим бактериологическим исследованием
Непрямые методики включали в себя определение индикана мочи (по методике Обермейера) до операции и на 7-е и 45-е сутки после баугинопластики; водородный дыхательный тест (ВДТ) с нагрузкой лактулозой, который проводился с помощью аппарата Gastrolyser до операции и на 7-е и 45-е сутки после операции. Дооперационное исследование пациентов с НБЗ указанными методиками проводилось предваряя рентгеноконтрастное исследование кишечника, либо спустя 4 недели после ирригоскопии. Пациенты основной группы в послеоперационном периоде антибиотикотерапию не получали. Предоперационная подготовка заключалась в 3-х кратных очистительных клизмах, что не могло повлиять на биоценоз тонкого кишечника.
С целью определения синдрома избыточного бактериального роста у пациентов контрольной группы выполнялись косвенные методы диагностики, которые включали в себя определение индикана мочи (по методике Обермейера) и ВДТ с нагрузкой лактулозой, выполняемый с помощью аппарата Gastrolyser. Исследование предваряло ирригоскопию.
Подготовка пациентов к ВДТ с лактулозой проводилась согласно методике предложенной Ledochowski M. (2008). Диагностическим критерием наличия СИБР у пациентов являлось повышение выделения Н2 после нагрузки в период от 0 до 60 мин на 10 ррм (при отсутствии после приема лактулозы абдоминальных симптомов, таких как, абдоминальная боль, урчание, метеоризм, диарея) и на 5 ррм (при наличии абдоминальных симптомов). В группу включались пациенты с базальной секрецией водорода до 5 ррм.
Статистическая обработка результатов ограничилась описательной статистикой проведенной с помощью программы Excel ввиду недостаточной репрезентативности выборки.
Результаты и обсуждение. Послеоперационных осложнений у пациентов основной группы не наблюдалось. Предложенная интраоперационная дигитальная диагностика полностью совпадала с данными дооперационной ирригоскопии. Гистологическое исследование резецированных червеобразных отростков подтвердило наличие хронического воспалительного катарального процесса в слизистом и подслизистом слоях червеобразного отростка с характерной лимфоидной инфильтрацией во всех 20 случаях.
Мезаденит интраоперационно выявлен у 16 пациентов основной группы. При морфологическом исследовании резецированных лимфоузлов брыжейки подвздошной кишки выявлена тотальная лимфоидная инфильтрация ткани лимфоузла без четких границ между корковым и мозговым слоями. Бактериологическое исследование мазка со среза резецированных лимфоузлов представлено следующим результатом: E. сoli гемолитические определялись в 9 случаях (104 КОЕ / мл), St. аureus – в 7 случаях (103–4 КОЕ / мл),
Бактериологическое исследование смывов содержимого дистального отдела подвздошной кишки, взятых интраоперационно у 20 пациентов основной группы, выявило изменения количественного и качественного состава биоценоза. Спектр микроорганизмов представлен следующими микроорганизмами: E. сoli гемолитические определялись у 10 пациентов (105– 107 КОЕ / мл), St. аureus – у 6 пациентов (106– 108 КОЕ / мл), C. аlbicans – у 4 пациентов (105– 109 КОЕ / мл). Высеваемая флора из резецированного лимфоузла и просвета подвздошной кишки у одного и того же пациента была идентичной.
По результатам ВДТ с нагрузкой лактулозой у пациентов основной группы до проведения баугинопластики (БП) (рис. 33) у всех обследуемых определяется СИБР 1–3 степени с замедлением оро-цекального клиренса (толстокишечный пик на 90-й минуте).
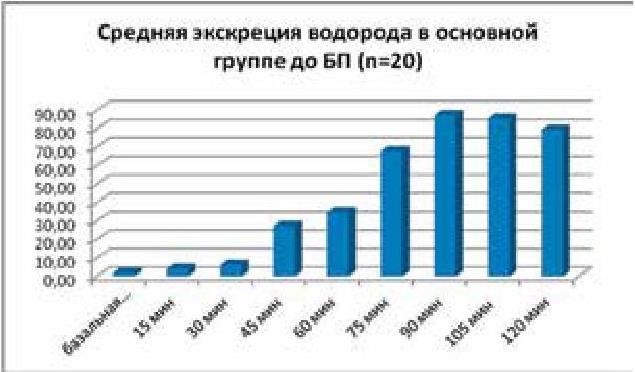
Рис. 33. Результаты экскреции Н2 у пациентов основной группы до операции
По результатам водородного дыхательного теста с нагрузкой лактулозой пациенты основной группы распределились следующим образом (табл. 6).
Таблица 6
Распределение пациентов основной группы (n=20).
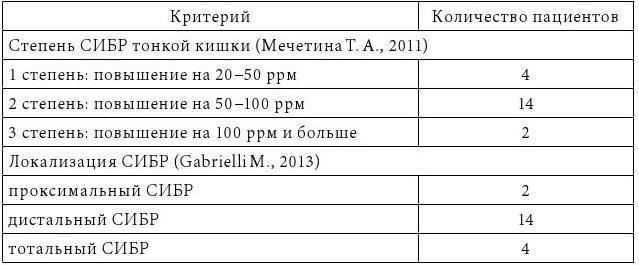
Определение индикана мочи у пациентов основной группы до хирургической коррекции дало положительные результаты в 16 случаях. Наличие незначительного (1 степени – повышение до 50 ррм) дистального синдрома избыточного бактериального роста у 4 пациентов, у которых индикан мочи оказался отрицательным, может говорить о недостаточной чувствительности этого скрининг-теста по сравнению с ВДТ.
На 7-е и 45-е сутки послеоперационного периода при отсутствии антибиотикотерапии индикан мочи у всех оперированных пациентов (n=20) был отрицательным.
По результатам ВДТ с нагрузкой лактулозой у пациентов основной группы на 7-е сутки после проведения баугинопластики (БП) (рис. 34) у всех обследуемых отмечалась значительная редукция количества выделяемого водорода, при этом нормализовалось время пассажа лактулозы по кишечнику (толстокишечный пик определяется на 75 минуте). На 45-е сутки после баугинопластики ВДТ соответствовал норме у всех пациентов (рис. 35).
Индикан мочи у пациентов контрольной группы с доказанной при ирригоскопии состоятельностью баугиниевой заслонки был отрицательным. Результаты водородного дыхательного теста в группе контроля (рис. 36) не отличались от нормальных показателей, описываемых в литературе (Ledochowski M., 2008).
Наши исследования подтверждают наличие СИБРа тонкой кишки у пациентов с НБЗ, что согласуется с данными зарубежных авторов (Oren Zaidel, 2003; Larry S. Miller, 2012) и укладывается в логику патогенеза рефлюкса толстокишечного содержимого в тонкую кишку. О достоверности полученных данных в настоящем исследовании говорить не приходится. Тем не менее, обнаруживается очевидная разница в результатах ВДТ у пациентов сравниваемых групп: значительное снижение концентрации выделяемого водорода после оперативного пособия (рис. 37). Первые полученные факты объективно указывают на эффективность баугинопластики, положительные клинические результаты которой мы наблюдали у 500 оперированных пациентов с НБЗ (Мартынов В. Л., 2006).
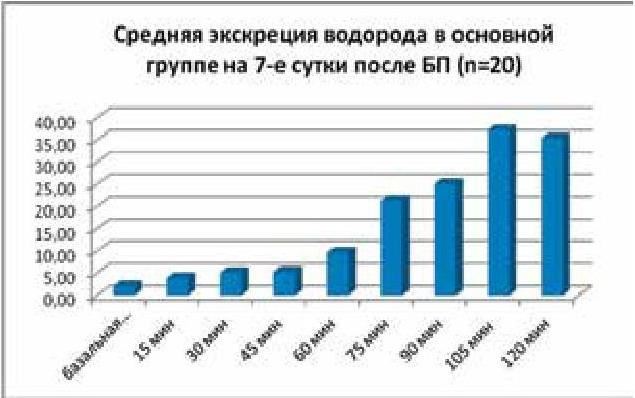
Рис. 34. Результаты экскреции Н2 у пациентов основной группы на 7-е сутки после операции
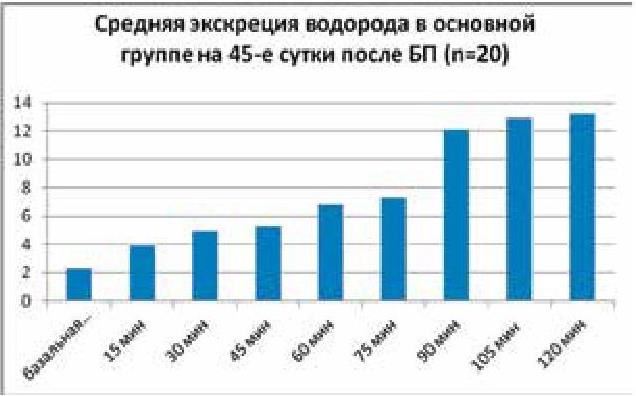
Рис. 35. Результаты экскреции Н2 у пациентов основной группы на 45-е сутки после операции
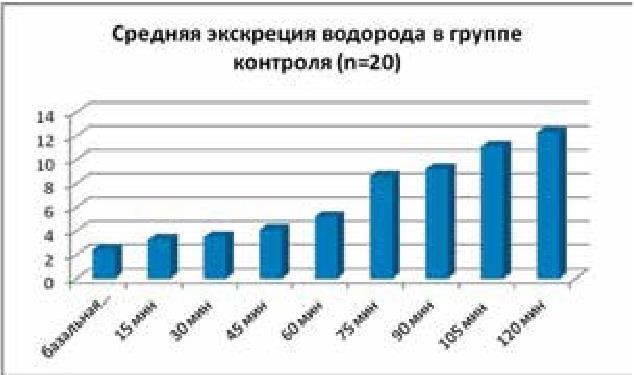
Рис. 36. Результаты экскреции Н2 у пациентов контрольной группы
Результаты бактериологического исследования аспирата подвздошной кишки пациентов с НБЗ подтверждают наличие СИБРа, выявленного с помощью ВТД с нагрузкой лактулозой. При этом установлено соответствие между степенью СИБР (по результатам ВДТ) и степенью обсемененности аспирата подвздошной кишки (табл. 7). Это согласуется с данными Е. Mendoza (2007), который установил чувствительность (85,7 %) и специфичность (90,9 %) водородного дыхательного теста с лактулозой по сравнению с «золотым стандартом».
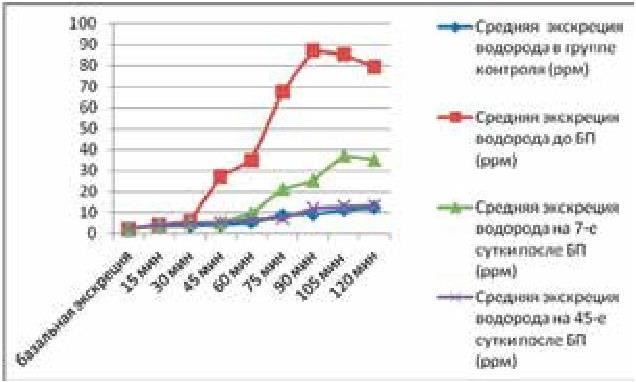
Рис. 37. Сравнительная характеристика экскреции Н2 у пациентов контрольной и основной групп до и после баугинопластики
Таблица 7
Соотношение степени СИБР и степени обсеменённости аспирата подвздошной кишки у пациентов с НБЗ (n=20).
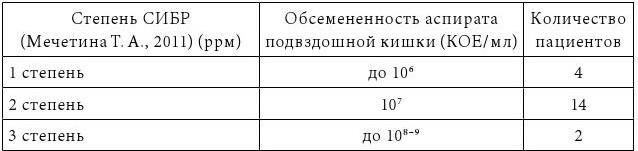
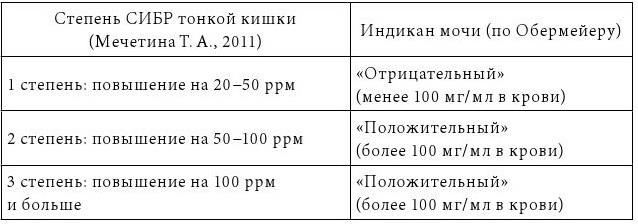
Определение индикана мочи позволяет заподозрить СИБР у пациентов с выраженной степенью обсемененности тонкой кишки (повышение выделения Н2 выше 50 ррм), но не информативно у пациентов с СИБР 1 степени (повышение выделения Н2 до 50 ррм) в сравнении с ВДТ. Выявленная диагностическая ценность этого метода, сохраняет его значение как скринингтеста СИБР тонкой кишки 2 и 3 степени.
Явления мезаденита и наличие в лимфоузлах микроорганизмов подтверждают транслокацию микроорганизмов через кишечную стенку. Факт бактериальной транслокации диагностированный у пациентов с СИБР тонкой кишки в условиях НБЗ согласуется с данными литературы (Wiest R., 2005; Hashimoto N., 2002; Heuman D. M., 2004; Жаркова М. Д., 2012).
Выводы:
1. СИБР у пациентов без НБЗ не выявлялся;
2. СИБР определялся у 20 (100 %) пациентов с НБЗ: 1 степени – у 4 (20 %) пациентов; 2 степени – у 14 (70 %) пациентов; 3 степени – у 2 (10 %) пациентов;
3. На 7-е сутки после баугинопластики СИБР 1 степени определялся у 8 (40 %) пациентов, у 12 (60 %) оперированных пациентов данных за СИБР по результатам ВДТ не выявлено;
4. На 45-е сутки после баугинопластики концентрация выделяемого водорода соответствовала норме;
5. Баугинопластика является хирургическим методом этиопатогенетического лечения СИБР.
Список литературы:
1. Мартынов, В. Л. Хирургическое лечение рефлюксной болезни: Монография / В. Л. Мартынов. – Нижний Новгород, Издво ООО «Центр оперативной печати», 2013–535 с.
2. Мартынов, В. Л. Рефлюксы пищеварительного тракта и их хирургическая коррекция: дис. … докт. мед. наук: 14.00.27 / Мартынов Владимир Леонидович. – Саранск., 2006. – 261 с.
3. Филиппова, Т. В. Значение медико-генетического консультирования при заболеваниях органов пищеварения / Т. В. Филиппова // РЖГГК. – 2014. – № 1. – С. 56–61.
4. Шептулин, А. А. Гастроэзофагеальная рефлюксная болезнь и функциональные заболевания желудочно-кишечного тракта: есть ли какая-то связь? / А. А. Шептулин, М. А. Визе-Хрипунова // РЖГГК. – 2010. – Т. 20. – № 4. – С. 44–48.
5. Sperber A. D., Drossman D. A., Quigley E. M. The global perspective on irritable bowel syndrome: a Rome Foundation-World Gastroenterology Organisation symposium // Am. J. Gastroenterol. – 2012. – Vol. 107 (11). – P. 1602–1609.
6. Нечаева Г. И., Яковлев В. М., Громова О. А., Торшин И. Ю. с соавт. Дисплазии соединительной ткани у детей и подростков. Инновационные стационар-сберегающие технологии диагностики и лечения в педиатрии. М.: Союз педиатров России, 2009, 96 с.
7. Oren Zaidel, Uninvited Guests: The Impact of Small Intestinal Bacterial Overgrowth on Nutritional Status / Oren Zaidel, Henry C. Lin. // Practical Gastroenterology. – 2003. – Vol. XXVII (7). – P. 24–37.
8. Ардатская, М. Д. Синдром избыточного бактериального роста: учебное пособие / М. Д. Ардатская. – Москва: Форте принт, 2011. – 56 с.
9. Larry, S. Miller Ileocecal valve dysfunction in small intestinal bacterial overgrowth: A pilot study / Larry S. Miller, Anil K. Vegesna, Aiswerya Madanam Sampath, Shital Prabhu, Sesha Krishna Kotapati, Kian Makipour // WGJ. – 2012. – V.18 – Р. 6801–6808.
10. Кучерявый, Ю. А. Взаимосвязь синдромов раздраженного кишечника и избыточного бактериального роста: есть ли она? / Ю. А. Кучерявый, С. В. Черёмушкин, Е. А. Маевская, Е. А. Сутугина // РЖГГК. – 2014. – № 2. – С. 5–14.
11. Маев И. В. Диагностика и лечение синдрома избыточного бактериального роста в тонкой кишке / И. В. Маев, Н. Ю. Ивашкина, Ю. А. Кучерявый, Т. С. Оганесян // Экспер. клин. гастроэнтерол. – 2011. – № 3. – С. 125–129.
12. Bures, J. Small intestinal bacterial overgrowth syndrome / Bures J., Cyrany J., Kohoutova D., Forst L. M., Rejchr T. S., Kventin A. J., Vorisek V., Kopasova M. // World J. Gastroenterol. – 2010. – Vol.28. – P. 2978–2990.
13. Ford, A. C. Small intestinal bacterial overgrowth in irritable bowel syndrome: systematic review and meta-analysis / Ford A. C., Spiegel B. M., Talley N. J., Moayyedi P. // Clin. Gastroenterol. Hepatol. – 2009. – Vol. 7. – P. 1279–1286.
14. Авдеев, В. Диагностика и лечение синдрома избыточного роста бактерий в тонкой кишке / В. Авдеев // Врач. – 2010. – № 12. – С. 1–3.
15. Плотникова, Е. Ю. Некоторые аспекты диагностики и лечения избыточной бактериальной контаминации тонкой кишки в клинической практике [электронный ресурс] / Е. Ю. Плотникова, М. В. Борщ, М. В. Краснова, Е. Н. Баранова // Лечащий врач. – 2013. – № 4. – режим доступа: http://www.lvrach.ru / 2013 / 02 / 15435625.
16. Полуэктова, Е. А. Лечение синдрома раздраженного кишечника с позиций современных представлений о патогенезе заболевания / Е. А. Полуэктова, С. Ю. Кучумова, А. А. Шептулин, В. Т. Ивашкин // РЖГГК. – 2013. – Т.23. – № 1. – С. 57–65.
17. Кучерявый, Ю. А. Синдром избыточного бактериального роста / Ю. А. Кучерявый, Т. С. Оганесян // РЖГГК. – 2010. – № 5. – С. 63–68.
18. Gabrielli, M. Prevalence of small intestinal bacterial overgrowth in Parkinson’s disease / Gabrielli M., Bonazzi P., Scarpellini E., Bendi A. E., Lauritano E. C., Fasano A., Ceravolo M. G., Capecci M., Rita Bentivoglio A., Provinciali L., Tonali P. A., Gasbarrini A. // Mov. Disord. – 2011. – Vol.26. – P. 889–892.
19. Lauritano, E. Small intestinal bacterial overgrowthrecurrenceafter antibiotictherapy / Lauritano E., Gabrielli M., Scarpellini E., Lupascu A., Novi M., Sottilii S., Vital E. G., Cesarino V., Serricchio M.,Cammarota G., Gasbarrini G., Gasbarrini A. // Am. J. Gastroenterol. – 2008. – Vol.103. – P. 2031–2035.
20. Gabrielli, M. Diagnosis of small intestinal bacterial оvergrowth in the clinical practice / M. Gabrielli, G. D. Angelo, T. D. I. Rienzo, E. Scarpellini, V. Ojetti // European Review for Medical and Pharmacological Sciences. – 2013. – V.17. – Р. 30–35.
21. Mendoza, E. Diagnosis of small intestinal bacterial overgrowth in children: the use of lactulose in the breath hydrogen test as a screening test / Mendoza E., Crismatt C., Matos R. // Biomedica. – 2007. – Vol. 27 (3). – P. 325–332.
22. Wiest, R. Bacterial translocation in cirrhosis / Wiest R., Garcia-Tsao G. // Hepatology. – 2005. – Vol. 41. – P. 422–433.
23. Hashimoto, N. Effect of acute portal hypertension on gut mucosa / Hashimoto N., Ohyanagi H. // Hepatogastroenterology. – 2002. – Vol.49. – P. 1567–1570.
24. Heuman, D. M. Persistent ascites and low sodium identify patients with cirrhosis and low MELD score who are at high risk for early death / Heuman D. M., Abou-assi S. G., Habib A. // Hepatology. – 2004. – Vol.40. – P. 802–810.
25. Жаркова, М. С. Влияние синдрома избыточного бактериального роста и бактериальной транслокации на течение заболевания у больных циррозом печени / М. С. Жаркова, М. В. Маевская, В. Т. Ивашкин // РЖГГК. – 2012. – Т.22. – № 5. – С. 56–63.
26. Мечетина, Т. А. Синдром избыточного бактериального роста в тонкой кишке после холецистэктомии: дис. … канд. мед. наук: 14.01.28 / Татьяна Анатольевна Мечетина. – Москва., 2011. – 134 с.






