Механизм токсического действия, патогенез интоксикации.
Отек легких – патологическое состояние, при котором транссудация сосудистой жидкости не уравновешивается ее резорбцией и сосудистая жидкость изливается в альвеолы.
Отек (oedema) – скопление избыточного количества жидкости в тканях. Скопившаяся невоспалительная жидкость называется транссудатом.
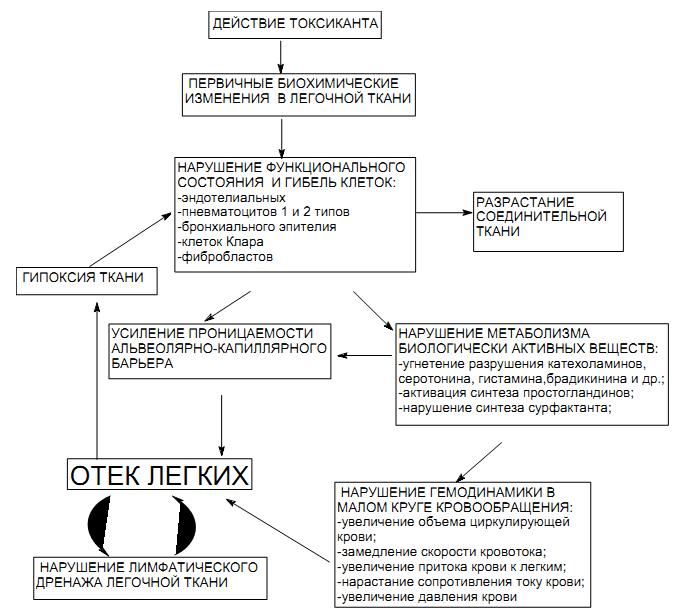
Токсическим он называется потому, что возникает в результате действия токсического вещества. В основе токсического отека легких (ТОЛ) лежит повышение проницаемости капиллярной и альвеолярной стенок, что приводит к пропотеванию жидкой части крови и протеинов (рис.2).
Обмен жидкости между кровью и тканями происходит в микроциркуляторном русле через стенку капиллярных сосудов и венул. В артериальном капиллярном сосуде жидкая часть крови поступает в межтканевое пространство, а в венозном и в посткапиллярной венуле – возвращается в кровь.
При токсическом отеке легких под влиянием нервно- рефлекторных механизмов происходит увеличение гидродинамического давления крови. В легочной ткани происходят биохимические изменения, которые полупроницаемую сосудистую мембрану превращают в проницаемую. Нейроэндокринные факторы существенное влияние оказывают на коллоидно-осмотические свойства легочной ткани.
Рис. 2. Схема развития токсического отека легких
Рассмотрим сущность нервно-рефлекторных, биохимических и эндокринных механизмов, участвующих в возникновении и развитии токсического отека легких.
Впервые в опытах А.В. Тонких (1944, 1964) была выявлена пусковая роль нервно-рефлекторных механизмов в патогенезе токсического отека легких. У кошек атравматично перерезались шейные симпатические узлы. Последующая затравка животных в камере с дифосгеном показала, что у таких животных по сравнению с контрольными (неоперированными) не возникает токсический отек легких. Следовательно, симпатические нервы несут к легким (эфферентно) чрезвычайную импульсацию, которая вызывает развитие патологического процесса.
Афферентным звеном рефлекторной дуги являются рецепторы блуждающего нерва в нижнем отделе дыхательных путей, которые подвергаются прямому воздействию паров фосгена (дифосгена). Достигая центра блуждающего нерва, возбуждение иррадиирует на гипоталамус, на высшие центры симпатической регуляции. Выброс катехоламинов в легочные сосуды увеличивает гидродинамическое давление крови, нарушает трофические процессы в легочной ткани, что подтверждается экспериментально. Внутривенное введение животным избыточного количества адреналина вызывает у них развитие отека легких. Показано также, что водная нагрузка, которая еще не вызывала отек легких, сопровождается гибелью животных от отека, если им нанести нервно-эмоциональную травму (Г.С. Кан).
Другой фактор, приводящий к легочной гипертензии – гипоксия. Известно, что легочная ткань по отношению к биологически активным веществам (БАВ) осуществляет метаболические функции, аналогичные тем, которые присущи тканям печени и селезенки. Способность микросомальных энзимов легких инактивировать или активировать вазоактивные гормоны очень высока. Вазоактивные вещества, такие как норадреналин, серотонин, брадикинин, способны оказывать влияние непосредственно на гладкие мышцы сосудов и бронхов и в определенных условиях повышать тонус сосудов малого круга, вызывая легочную гипертензию. Поэтому понятно, что тонус сосудов малого круга зависит от интенсивности метаболизма этих БАВ, происходящего в эндотелиальных клетках легочных капилляров. Обнаружено, что при гипоксии нарушается инактивация в легких норадреналина, серотонина и брадикинина. В крови, оттекающей от легких, возрастает их количество.
Следовательно, легочной гипертензивный эффект можно связать с увеличением уровней конкретных вазоактивных веществ: норадреналина, серотонина и брадикинина.
Помимо нервно-рефлекторных механизмов пусковую роль способны сыграть и местные биохимические изменения в легочной ткани, возникающие под действием фосгена. Объектом воздействия (т.е. клетками-мишенями) отравляющего вещества являются: клетки Эрлиха, альвеолоциты, клетки эндотелия сосудов. Повреждающее действие яда на клетки Эрлиха приводит к тому, что они перестают удерживать в себе запасы гистамина, серотонина и других активных веществ. Их освобождение активирует фермент гиалуронидазу в легочной ткани, под влиянием которого возникает диссоциация кальциевой соли гиалуроновой кислоты – основного вещества соединительнотканной стенки легочного сосуда. Сосудистая мембрана из полупроницаемой становится проницаемой. Этому способствует повреждение ядом эндотелиоцитов, приводящее к увеличению промежутков между ними, вследствие их сморщивания и последующего лизиса.
К местным нарушениям следует отнести повреждение поверхностно-активного вещества (ПАВ) или сурфактанта. При токсическом отеке легких содержание сурфактанта в альвеолах снижается в результате деструкции клеток-продуцентов (альвеолоцитов I, II типа). В норме внутренняя поверхность альвеол покрыта сурфактантом – поверхностно-активными веществами, основную массу которых составляют липопротеиды. За счет высокой поверхностной активности сурфактантов поверхностное натяжение в легком близко к нулю, что предотвращает транссудацию жидкости в просвет альвеол из капилляров и предохраняет альвеолы от слипания. К сурфактантной системе легких относятся пневмоциты I и II типов, принимающие участие в синтезе сурфактантов, депонировании готового материала и его секреции, а также макрофаги, с помощью которых отработанный сурфактант удаляется с альвеолярной поверхности. Это приводит к снижению поверхностного натяжения в альвеолах и повышению проницаемости альвеолярной мембраны для отечного транссудата.
Со степенью проницаемости стенки капиллярных сосудов тесно связана интенсивность лимфообразования. Повышение лимфообразования и ускорение оттока лимфы из межальвеолярного пространства играют важную компенсаторную роль при развивающемся отеке легких. Эта приспособительная реакция оказывается недостаточной при токсическом отеке легких, так как лимфатическая система не выполняет свою основную функцию – осуществление постоянного и эффективного дренажа интерстиция. При токсическом отеке развивается динамическая недостаточность лимфатической системы легких – объем транссудации межтканевой жидкости превышает возможности лимфатической системы обеспечивать эффективный дренаж межуточной ткани.
Проницаемость капиллярной и альвеолярной стенок нарушаются неодновременно. Вначале становятся проницаемыми капиллярные мембраны, и сосудистая жидкость пропотевает в интерстиций, где временно накапливается. Такую фазу развития отека называют интерстициальной. Она характеризуется постепенным развитием и скудными клиническими признаками. Во время интерстициальной фазы происходит компенсаторное ускорение лимфотока примерно в 10 раз. Эта приспособительная реакция оказывается недостаточной, и внесосудистая жидкость, переполнив интерстиций, прорывается в полость альвеол через их деструктивно измененные стенки. Развивается альвеолярная фаза токсического отека легких. Она характеризуется внезапностью развития и выраженными клиническими симптомами.
Работами русских ученых (К.М. Быков и сотр.) выявлено изменение нервно-гуморальной регуляции водно-электролитного обмена в организме в условиях интоксикации фосгеном. В эксперименте доказано, что усиленное кровенаполнение малого круга кровообращения и нарушение водно-электролитного обмена у животных, отравленных фосгеном, является следствием повышенного продуцирования гипофизом вазопрессина, удерживающего в организме воду путем задержки мочеотделения, и гиперсекреции альдестерона корой надпочечников, что способствует задержке ионов натрия в организме. Уменьшение объема циркулирующей крови при токсическом отеке легких вследствие выхода транссудата за пределы сосудистой стенки, рефлекторно приводит к гиперсекреции вазопрессина и альдестерона. Так возникает «ошибка регуляции», которая способствует развитию отека.
Обсуждение механизмов возникновения и развития токсического отека легких показало, что цепь причинно- следственных отношений складывается из следующих основных звеньев:
1. Повышение гидростатического давления в сосудах малого круга кровообращения (нервно-рефлекторные влияния, гипоксия).
2. Повышение проницаемости капиллярно-альвеолярной мембраны (повреждение эндотелиоцитов, клеток Эрлиха, альвеолоцитов I и II типов, нарушение сурфактантной системы).
3. Недостаточность лимфатической системы легких.
4. Нарушение нервно-гуморальной регуляции водно- электролитного обмена («ошибочное» включение антидиуретической и антинатрийурической систем).