3.2. Стенокардия
Потенцирование аскорбиновой кислотой лечебного эффекта NO-доноров (нитроглицерина) при стенокардии. Сильный адренергический компонент стресс-реакции может приводить к стойкому спазму гладкой мускулатуры анатомически неизмененных коронарных артерий с последующим развитием вторичных ишемических повреждений миокарда [98]. Транзиторный спазм венечных сосудов выявляется примерно у каждого четвертого больного при проведении коронарографии, что указывает на важную роль этого звена в патогенезе ишемической болезни сердца (ИБС) [124]. Вазоконстрикторное действие катехоламинов реализуется с уровня ?-адренорецепторов сосудов при участии цАМФ [95].
Как и в поперечнополосатой мышце, транзиторный спазм гладкой мускулатуры сосудов может приводить к их контрактуре с развитием очаговых поражений сердца и других органов, типичных для стресса [98]. Например, обнаруженные Г. Селье стрессорные язвы желудка есть не что иное, как ишемические некрозы слизистой оболочки, вызванные адренергическим спазмом сосудов [140].
Современные методы исследования позволяют наблюдать развитие спазма коронарных артерий у больных ИБС визуально [268]. В литературе описан случай, когда введение нитроглицерина при проведении экстренной коронароангиографии у 4 из 36 больных с типичной клинической картиной инфаркта миокарда привело к тому, что первичная картина полной коронароокклюзии одной из крупных коронарных артерий сменилась контрастированием сосуда на всем протяжении [124]. Данный факт может служить обоснованием и одновременно зримым результатом эффективности патогенетической терапии стрессорного спазма сосудов сердца с помощью этого классического вазодилятатора, который известен медикам уже 150 лет [107, 292, 307].
Считается, что вазоспазм коронарных артерий при приступе стенокардии объективно отражает депрессия сегмента ST на ЭКГ [111]. Разработаны схемы ежечасной дозированной провокационной велоэргометрии и синхронного электрокардиографического мониторинга этого показателя, используемые как для диагностики стенокардии, так и для оценки эффективности антиангинозных препаратов и разработки индивидуального суточного регламента их применения [3]. Антиишемический эффект в каждой временной точке исследования определяют по уменьшению выраженности депрессии сегмента ST в процентах от исходного уровня (ST %) по данным компьютерного мониторинга ЭКГ, фиксирующего любое его смещение с точностью до 0,1 мм. Из сравнительного анализа профилей временной динамики изменений этого показателя, описывающих начало, продолжительность и выраженность эффекта, выявляют преимущества тех или иных вазодилятаторов [104].
В отличие от дозированной велоэргометрической нагрузки при проведении острой фармакологической пробы (внутримышечная инъекция 600 мг компламина – [163]) более информативным ЭКГ-критерием развития транзиторной ишемии миокарда является изменение положения электрической оси сердца [21]. Поэтому для выявления факта наличия или отсутствия потенцирующего действия витамина С в отношении антиангинозных эффектов нитратов мы использовали информативность сочетания провоцирующих ишемию миокарда нагрузок и электрокардиографического мониторинга, только вместо повторяющейся велоэргометрии применили однократное введение компламина, а ежечасный режим измерений заменили ЭКГ-исследованием (в 12 основных отведениях) с компьютерной обработкой данных через 5, 10 и 15 мин, когда четко фиксировалось изменение положения электрической оси сердца (? < ?) в ответ на острую фармакологическую пробу.
В результате проведения компламиновой пробы у одних и тех же больных стабильной стенокардией напряжения II и III ФК до (5-я группа) и после введения витамина С (6-я группа) выявлено изменение ряда клинических и ЭКГ показателей.
Боль. У 2 больных (ФК II + постинфарктный кардиосклероз) после введения компламина на 5-й и 10-й минутах появилась загрудинная боль стенокардического характера, которая прошла самостоятельно. При повторном введении компламина на фоне предшествующего однократного введения 500 мг аскорбиновой кислоты за 2–3 ч до исследования болевого синдрома не было.
У 1 больного, которому днем вводили компламин, вечером и ночью возникли кратковременные приступы стенокардии, купированные сублингвальным приемом нитроглицерина. На следующий день, когда компламиновую пробу проводили через 2–3 ч после введения аскорбиновой кислоты, болевого синдрома не наблюдалось.
ЧСС. В нашем исследовании ЧСС через 5 мин после введения компламина увеличилась у 8 больных, у 2 уменьшилась и у 2 не изменилась. В этот же период времени после аналогичной фармакологической нагрузки на фоне предшествующего введения витамина С ЧСС увеличилась только у 4 больных, а уменьшилась у 8 больных. Через 10 мин в обеих группах увеличение ЧСС выявлено у 8 пациентов, а через 15 мин – у 8 и 9 (соответственно в 5-й и 6-й группах).
Нарушение сердечного ритма. После введения компламина у 2 пациентов возникли суправентрикулярная экстрасистолия и у 1 – синусовая аритмия. На следующий день, когда компламиновая проба проводилась на фоне предварительного введения витамина С, суправентрикулярная экстрасистолия возникла только у одного пациента.
Анализ II, aVF, V1 и V5отведений. Во II, aVF, V1 и V5 отведениях общепринятой системы ни в одном случае не выявлено ишемических изменений сегмента ST по сравнению с исходными данными.
Критерии ЭКГ картирования. В данном исследовании мы применили анализ суммарных показателей ЭКГ в 6 грудных отведениях общепринятой системы (? ST, ? R). Использованы следующие критерии ишемической реакции: а) суммарный подъем сегмента ST более 1,2 мм;
б) суммарная депрессия сегмента ST более 1,2 мм; в) суммарное повышение амплитуды зубца R более 2 мм; г) локальное суммарное снижение амплитуды зубца R более 10 мм в одном или двух прекордиальных отведениях [21].
По критериям ЭКГ картирования достоверных отличий между обследуемыми группами больных не обнаружено.
Положение электрической оси сердца. Выполнен анализ изменений положения электрической оси сердца
в исследуемых группах путем определения разницы величины угла ? (? < ?) в исходном состоянии, а также через 5, 10 и 15 мин после ишемической нагрузки. Из 12 пациентов у 9 при повторном обследовании угол ? в исходном состоянии (до введения компламина) не изменился или изменился только на 1°, что свидетельствует о высокой воспроизводимости метода и обоснованности его применения для оценки ишемических реакций.
Как видно из табл. І-11, на высоте ишемической нагрузки (5, 10 и 15 мин действия компламина) положение электрической оси сердца изменилось соответственно на 6, 8 и 6 градусов. Если у тех же больных компламиновая проба проводилась после введения витамина С, то во все сроки исследования положение электрической оси сердца оставалось на исходном уровне.
Таблица І-11.
Изменение угла ? (арифметическая разница в градусах между исходным положением электрической оси сердца и ее положением через 5, 10 и 15 мин после введения препаратов) в исследуемых группах
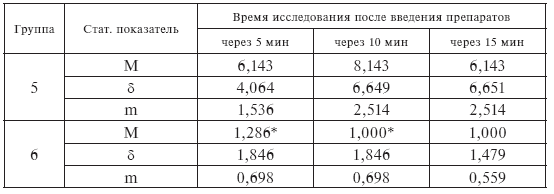
* Достоверное отличие между группами – p < 0,05.
Таким образом, данные клинического обследования (боль, ЧСС, нарушения сердечного ритма) и ЭКГ-мониторинга (стабилизация положения электрической оси сердца) показывают, что аскорбиновая кислота существенно усиливает антиангинальные вазодилятаторные эффекты нитратов и тем самым предотвращает развитие ишемической реакции миокарда в ответ на введение компламина.
Инкубация в анаэробных условиях раствора аскорбиновой кислоты с NO-донорами (нитрит натрия, нитроглицерин) или с кровью больных ИБС, длительно лечившихся нитровазодилятаторами пролонгированного действия, приводит к выделению в сосудике Варбурга пузырьков газа, идентифицированного нами по реакции нитрозилирования гемоглобина как NO (рис. І-24). После смешивания и инкубации аскорбиновой кислоты с NaNO2 в сосуде Варбурга в анаэробных условиях при 37° наблюдали выделение NO, выход которого количественно регистрировали по образованию нитрозоНв. Из сосуда Варбурга оксид азота дифундировал в кювету, содержащую раствор дезоксиНв. Содержание кюветы перемешивали с помощью магнитной мешалки для ускорения растворения газа. Постепенно дезоксиНв превращался в нитрозоНв, что сопровождалось характерными изменениями в спектре поглощения. Полоса Соре исходного дезоксиНв при 429 нм смещалась до 418 нм, а широкая асимметричная полоса поглощения с максимумом при 555–560 нм заменялась двумя полосами с максимумами при 545 и 574 нм, принадлежащими нитрозоНв (рис. І-25). В спектре поглощения гемоглобина наблюдали наличие изобестических точек при 548,5 и 565,5 нм, молярные коэффициенты поглощения (М—1 см—1) которых были равны соответственно 12 300 и 11 700 (рис. І-26) и использовались для количественных расчетов концентраций форм гемоглобина.
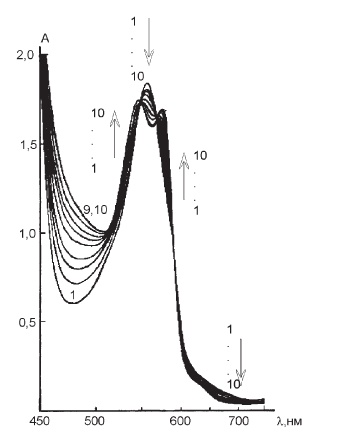
Рис. І-24. Кинетика образования нитрозогемоглобина (спектры поглощения) при взаимодействии аскорбиновой кислоты с плазмой крови больного стенокардией напряжения II ФК, получавшего нитроглицерин пролонгированного действия. Концентрация в 0,05 М натрий-фосфат– ном буфере, рН 7,4: плазмы ? 1,2?10–4, аскорбиновой кислоты – 1,2?10–4 М. Объем: 3,8 мл (в сосуде Варбурга), 5 мл Hв (10–4 М). Время: 1 – 0?, 2 – 15?, 3 – 30?, 4 – 45?, 5 – 60?, 6 – 1,5 ч, 7 – 2 ч, 8 – 4 ч, 9 – 6 ч, 10 – 10 ч
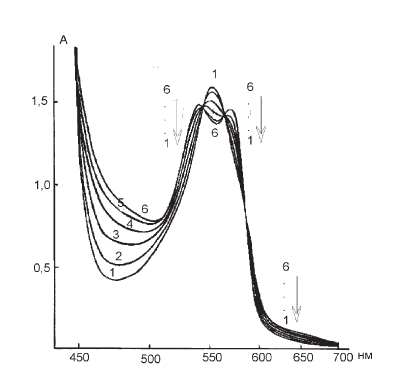
Рис. І-25. Образование нитрозоНв из дезоксиНв (2·10–5М) при выделении NO в результате взаимодействия аскорбиновой кислоты (3·10–3М) и нитрита натрия (3,7·10–2М) в анаэробных условиях. Реакция запускалась после переливания нитрита натрия (0,4 мл) из бокового отростка в центральную часть сосуда Варбурга, содержащего раствор аскорбиновой кислоты (1 мл). Спектры поглощения гемоглобина записывали через: 0 (1), 3 (2), 6 (3), 10 (4), 15 (5), 25 (6) мин после смешивания при 37 °C в натрий-фосфатном буфере, рН 7,4
Как известно, NO с высоким сродством связывается с дезоксиНв. Равновесная константа связывания NO с Нв равна 1,4?1012 М–1 с–1, что более чем в 2000 раз превышает равновесную константу связывания СО с Нв.
Причем сродство NO одинаково как для ?-, так и ?-субъединиц [285]. Исходя из значения равновесной константы ассоциации, можно предположить, что, уже начиная с таких, практически следовых концентраций NO, как 10–10 М, в основном весь NO будет связан с дезоксиНв. Исходя из того, что в условиях наших опытов образование нитрозогемоглобина происходило в течение нескольких минут, а равновесие устанавливается даже при концентрациях NO 10–12 М в течение миллисекунд, то можно считать, что измеренное количество нитрозоНв отражает конечную концентрацию NO.
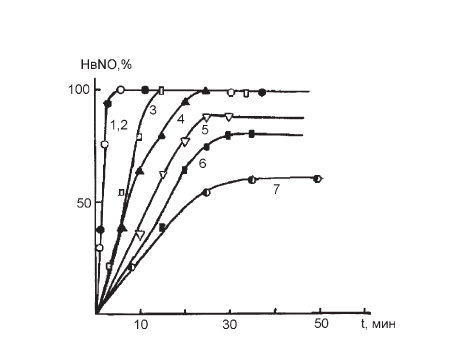
Рис. І-26. Зависимость образования NO (регистрация по НвNO) в реакции взаимодействия нитрата натрия с аскорбиновой кислотой от концентрации витамина С. Концентрации в 0,05 М натрий-фосфатном буфере, рН 7,4: нитрита натрия – 5,7 · 10–2, аскорбиновой кислоты – 1,5 · 10–1 М (1), 7,5 · 10–2 М (2), 3 · 10–2 М (3), 3 · 10–3 М (4), 1,2 · 10–3 М (5), 6 · 10–4 М (6), 310–4 М (7). Объем: 1,4 мл (в сосуде Варбурга), 5 мл Нв (10–4 М)
На основании полученных данных можно заключить, что витамин С принимает активное участие в обмене NO. Являясь сильным восстановителем, аскорбиновая кислота in vitro защищает оксиНв от окисления нитритом натрия и дозозависимо усиливает выделение NO из состава NaNO2, что зафиксировано с помощью реакции нитрозилирования дезоксигемоглобина (рис. І-26), которая сопровождается характерными изменениями в его спектре поглощения (рис. І-25). Факт влияния витамина С на выделение NO из широко используемых в клинике антиангиозных препаратов in vitro доказан спектрофотометрически.
При смешивании нитроглицерина с раствором аскорбиновой кислоты происходит медленное выделение NO2- (NO).
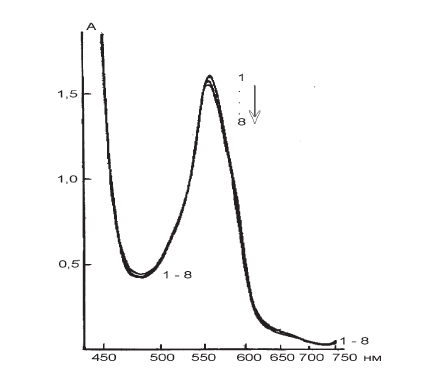
Рис. І-27. Спектры поглощения дезоксигемоглобина после откачки воздуха и смешивания в сосуде Варбурга аскорбиновой кислоты (3·10—1М) в 0,8 мл 0,05 М натрий-фосфатного буфера с аликвотой (0,8 мл) того же буфера. Изменение спектров записывали через 0 (1), 0,5 (2), 1 (3), 1,5 (4), 2 (5), 3 (6), 4 (7), 24 (8) часов при 37 °C
Связывание NO2- (NO) дезоксигемоглобином легко фиксируется по возрастанию оптической плотности раствора гемоглобина в районе 460–510 нм и ее падению при 555 нм, что свидетельствует об образовании мет– и нитрозогемоглобина в процессе длительной инкубации (рис. І-27, І-28).
Известно, что у больных с сердечной недостаточностью уровень нитритов в плазме крови более высок, чем у здоровых субъектов [215]. Причина этого не выяснена. Дополнительный нитрат может возникать эндогенно, например, в результате более быстрого образования NO в сосудах или активации макрофагов. Альтернативно, большие уровни нитрата в плазме больных могут быть обусловлены предыдущим внутривенным введением больших доз нитровазодилятаторов.
Инкубация аскорбиновой кислоты с плазмой крови больных ишемической болезнью сердца приводит к выделению NO, которое уменьшается после предварительного отделения низкомолекулярных соединений с помощью гельфильтрации через сефадекс. In vitro максимальный выход NO наблюдали при взаимодействии аскорбиновой кислоты с плазмой крови больных, получивших нитратсодержащие препараты, до ее пропускания через колонку с сефадексом G-25 (рис. І-29).
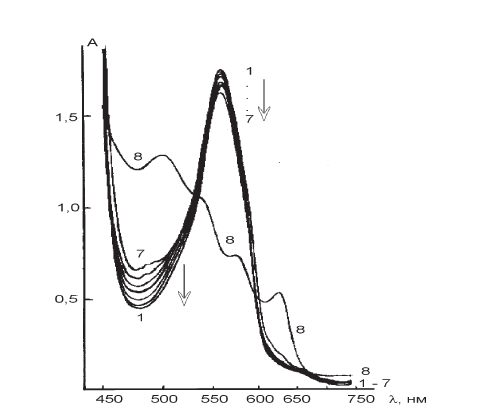
Рис. І-28. Спектры поглощения дезоксигемоглобина после откачки воздуха и смешивания в сосуде Варбурга аскорбиновой кислоты (3·10–1 М) в 0,8 мл 0,05 М натрийфосфатного буфера с 15 таблетками нитроглицерина (0,0005 мг каждая). Изменение спектров записывали через 0 (1), 0,5 (2), 1 (3), 1,5 (4), 2 (5), 3 (6), 4 (7), 24 (8) часов при 37 °C
Предполагаемый механизм взаимодействия витамина С с нитритом натрия in vitro может быть следующим:
AKH2 + 2NO2- + 2H+ ? AK + 2NO + 2H2O,
т. е. аскорбиновая кислота восстанавливает NO2- в NO со стехиометрией 1: 2.
Этот процесс протекает очень эффективно, что доказано нами по образованию нитрозоНв. Гораздо менее эффективно в присутствии аскорбиновой кислоты происходит гидролиз алкилнитратов, являющихся лекарственными соединениями, судя по регистрируемому изменению поглощения в области 470 нм.
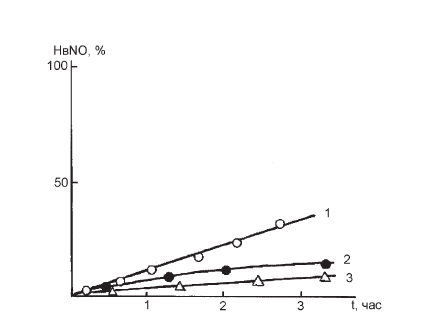
Рис. І-29. Инициируемое аскорбиновой кислотой выделение NO из плазмы больного ишемической болезнью сердца, получавшего нитритсодержащие препараты, отделенной от низкомолекулярных соединений на колонке с G-25 (2) и неотделенной (1). Кривая 3 – выделение NO из плазмы больного ИБС до лечения (без гельфильтрации через сефадекс). Концентрации в 0,05 М натрий-фосфатном буфере, рН 7,4: плазмы ~ 1,2 · 10–4 М, аскорбиновой кислоты – 4,2 · 10–2 М. Объем: 3,8 мл (в сосуде Варбурга), 5 мл Нв (10–4 М)
Здесь выход NO был примерно на 2 порядка меньшим, чем для неорганического нитрита (NO2-). Однако в плазме крови возможны реакции обмена между тиольными соединениями, аскорбиновой кислотой и органическими нитратами, которые могут существенно ускорять процесс освобождения NO:
R – CH2 – O – NO2 + GSH ? RCH2 – OH + GS – NO2
GS – NO2 + AKH2 ? GSH + NO2- + AK + H+
Исходя из этого механизма, не исключено, что аскорбиновая кислота может потенцировать действие нитровазодилятаторов in vivo при совместном применении.
Учитывая способность аскорбиновой кислоты в аэробных условиях восстанавливать трехвалентное железо до двухвалентного и роль последнего в образовании и распаде транспортных форм NO (S-нитрозотиолы ? ДНКЖ), можно допустить, что витамин С in vivo способен высвобождать фактор релаксации сосудов из эндогенного депо, например из динитрозильного комплекса железа с цистеином (ДНКЖ). Считается, что при воздействии восстановителей стабильные диамагнитные d6 (Fe2+) – комплексы ДНКЖ переходят в неустойчивое состояние с парамагнитной конфигурацией железа d7 (Fe+), что приводит к их распаду и высвобождению NO [10].
В организме есть и другие потенциальные NO-доноры. Это нитриты и нитраты, которые накапливаются в нем при нарушениях обменных процессов [324] или в результате избыточного поступления с пищей, питьевой водой, медикаментами. Проблема в том, как превратить временно депонируемые в организме невазоактивные нитросоединения в источник оксида азота, необходимый для купирования или профилактики стенокардии. И в этом смысле витамин С может играть самостоятельную роль [260]. При обследовании мужчин одного из районов Киева, проведенном НИИ кардиологии имени Н. Стражеско и НИИ гигиены питания (г. Киев), обнаружено, что при низком потреблении витамина С с пищей достоверно повышается частота ИБС (в 2,3 раза) и факторов риска: артериальной гипертензии (в 2,9 раза), гиперлипопротеидемии (в 2,4 раза), избыточной массы тела (в 2,8 раза) [50].
Известно, что при длительном использовании эффективность лечебного действия нитратов снижается. Добавление витамина С в дозе 1 г 3 раза в сутки предупреждает прогрессирование повышения активности тромбоцитов, отмечаемого во время развития толерантности к нитратам при их непрерывном приеме. Предполагается, что в этом случае проявляется антиоксидантное действие аскорбиновой кислоты, поскольку повышенное образование кислородных радикалов и пероксинитрита играет доминирующую роль в развитии толерантности к нитратам [106]. С другой стороны, при повышении содержания супероксида в толерантных сосудах снижается активность гуанилатциклазы. Поэтому ослабление внутриклеточной продукции цГМФ рассматривается как важный механизм развития толерантности к нитратам.
В последней связи интересные результаты были получены в перекрестном рандомизированном исследовании. Применение витамина С снижает риск возникновения коронарной болезни [305], компенсирует эндотелиальную дисфункцию эпикардиальных коронарных артерий у больных с гипертензией [321], уменьшает количество осложнений острого ИМ [254] и его размеры [194], предотвращает рестеноз после коронарной ангиопластики [340] и снижает толерантность к нитратам [353].
У больных, получавших аскорбат (2 г 3 раза в сутки), с помощью плетизмографии предплечья определяли венодилятирующий эффект в ответ на принятый сублингвально нитроглицерин (0,5 мг) – до и через 5 мин. В пробах крови измеряли содержание цГМФ в тромбоцитах. Препарат предупреждал ослабление продукции цГМФ, вызываемое продолжительным применением трансдермального нитроглицерина (0,4 мг/ч, 2 раза в сутки, через каждые 12 ч в течение 3 дней) и был способен поддерживать венодилятацию [353]. По нашим данным, активация аскорбиновой кислотой эндогенных NО-доноров и потенцирование ею антиангинальных эффектов экзогенного нитроглицерина позволяет существенно увеличить эффективность нитратотерапии и нитратопрофилактики стенокардии.






