ЛЕЧЕНИЕ
Объем терапевтических мероприятий при лечении больных с ПСА определяется основными параметрами патологического процесса, которые включают клинико-анатомический вариант суставного синдрома, спектр возможных системных проявлений и их выраженность, степень лабораторной активности, характер псориаза и стадию его развития.
Существенную роль при лечении ПСА играет диета. Рекомендуют достаточное обеспечение потребностей организма полноценным белком со сбалансированностью аминокислотного состава, лучше с ограничением мяса, но достаточным употреблением в пищу рыбы, молока, яиц. Рацион больных ПСА должен содержать достаточное количество овощей, зелени, богатых кальцием и витаминами С, Р, Е, А, каротином (морковь, тыква, фасоль, капуста, кукуруза, свекла, помидоры). Особенно эффективен при ПСА сок капусты, применяемый по 1 стакану в день на протяжении нескольких месяцев.
Для больных ПСА необходимо достаточное количество жидкости, не менее двух литров в сутки.
Близость клинических проявлений ПСА к РА и ББ дала основание использовать при осложненном ПСА те принципы терапии, которые разработаны и с успехом применяются при основных воспалительных заболеваниях суставов и позвоночника и которые направлены на подавление иммунопатологических нарушений — главной мишени терапевтического воздействия. Но лечение ПСА имеет и свои отличительные особенности. Среди базисных препаратов, применяющихся при этом заболевании, фигурируют не только метотрексат, циклоспорин, сульфасалазин, лефлуномид и препараты биологического действия, но и колхицин, дериваты фумаровой кислоты, микофенолат мофетил, ароматические ретиноиды, дериваты витамина D, соматостатин и др., многие из которых способствуют разрешению как суставных, так и кожных проявлений заболевания. Далеко не все они нашли широкое применение в терапии осложненного ПСА из-за относительно низкой эффективности и возможности развития серьезных побочных реакций при их длительном применении. Производные хинолина при ПСА оказывают более слабое действие на суставной синдром, чем при РА, и в то же время они способствуют переходу стационарной стадии дерматоза в прогрессирующую, пуспулезную или эксфолиативную эритродермию и даже появлению первых псориатических эффлоресценций. Отрицательная динамика кожного синдрома при таком лечении достигает 41,7 %, поэтому их применение не рекомендуется при этом заболевании.
При ПСА целесообразно применение таких препаратов, которые активно воздействовали бы одновременно на основные синдромы ПСА — суставной и кожный. Это тем более актуально, что между этими синдромами существует тесная взаимосвязь и взаимообусловленность. Параллелизм течения кожного и суставного синдромов является одним из диагностических критериев данного заболевания. Эта взаимообусловленность находит свое выражение в одновременном развитии кожного и суставного синдромов в дебюте заболевания, синхронности обострений этих синдромов, изменении характера дерматоза при возникновении артрита или спондилоартрита, что выражается как в появлении более распространенных его форм, так и в трансформации ограниченного вульгарного ПСА в распространенный вульгарный или в экссудативный, в возникновении торпидных форм дерматоза к ранее эффективной терапии, а также исчезновении четко выраженной сезонности обострений ПСА, наблюдавшейся до поражения суставов.
В настоящее время осуществляют многоцентровое двойное слепое рандомизированное плацебо-контролируемое исследование, проводимое в параллельных группах с целью оценки эффективности и безопасности применения двух доз апремиласта (СС-10004) у пациентов с активным псориатическим артритом и псориатическим очагом (материалы, вынесенные на заседание Совета по этике от 09.02.2011 г. № 11).
При остеолитическом и спондилоартритическом вариантах, наиболее тяжелых и неблагоприятных в прогностическом плане, необходимо проведение особенно активной терапии, с включением интенсивных методов лечения. Напротив, при олигоартритическом и дистальном вариантах, характеризующихся мало прогрессирующим течением и длительным сохранением функциональной способности опорно-двигательного аппарата, терапия может быть ограничена лишь применением нестероидных противовоспалительных препаратов, локальным применением глюкокортикостероидов и назначением сульфасалазина.
При ПСА, как и при других аллергических заболеваниях, необходим постоянный прием аскорбиновой кислоты (0,5 г/сут) вместе с рутином (1 табл. 3 раза в день). Витамин С не только укрепляет сосудистую стенку, уменьшая экссудацию тканей, но и увеличивает выработку полноценных глюкокортикоидов в собственных надпочечниках, так как участвует в их синтезе.
Монотерапия НПВП показана на протяжении 2–6 мес. только при благоприятном течении ПСА (олигоартрит, поражение дистальных межфаланговых суставах). Наименьшая выраженность побочных эффектов характерна для мелоксикама и целебрекса.
Конкретными показаниями к проведению базисной терапии метотрексатом являются злокачественная форма ПСА, быстро прогрессирующее течение заболевания, генерализованное поражение суставов, высокая лабораторная активность на протяжении 3 и более месяцев, экссудативный, пустулезный или эритродермический ПСА, выраженные трофические нарушения, упорный диффузный гломерулонефрит. С учетом современных представлений показания к иммуносупрессивной терапии могут быть расширены. Ее следует начинать в ранней стадии ПСА, особенно при тяжелых формах, еще до появления деструктивных изменений в костно-суставном аппарате (Насонов Е. Л., 2008).
На фоне лечения БПВП деструкция суставов может прогрессировать, несмотря на снижение клинической активности или достижения клинической ремиссии.
Метотрексат обладает высокой терапевтической эффективностью в отношении кожных проявлений ПСА. Он является препаратом выбора при лечении генерализованного экссудативного, пустулезного и эритродермического ПСА, т. е. наиболее тяжелых вариантов этого дерматоза, которые, как правило, протекают с системными проявлениями и часто способствуют развитию артрита и/или спондилита. Метотрексат, являясь структурным аналогом фолиевой кислоты, тормозит синтез нуклеиновых кислот, активно вмешивается в репродукцию клеток и тем самым угнетает ускоренный эпидермопоэз. Длительный, на протяжении ряда лет прием метотрексата существенно влияет на течение ПСА, обеспечивая низкие значения лабораторных показателей воспалительного процесса. Отмечая высокую эффективность метотрексата у больных ПСА, следует иметь в виду, что он полностью не подавляет воспалительный процесс. Отрицательную рентгенологическую динамику при лечении метатрексатом наблюдали у каждого третьего больного, что проявлялось возникновением новых эрозий, увеличением выраженности остеолиза или формированием новых синдесмофитов. На фоне базисной терапии прогрессирование костной деструкции обычно протекает субклинически, без четких симптомов обострения ПСА (Насонов Е. Л., 2008).
Метотрексат влияет не только на иммунокомпетентные клетки, но тормозит деление и вызывает гибель других клеток, что приводит к развитию «цитостатической болезни», своеобразного полисиндромного заболевания, обусловленного действием на организм цитостатических факторов. Метотрексат обусловливает целый ряд осложнений (стоматит, пневмонит, депрессия кроветворения и др.).
Лефлуномид по сравнению с метотрексатом и сульфосалазином значительно улучшает качество жизни. Частота побочных действий ниже, чем у других БПВП. Дозировка — начинать с 10–20 мг/сут, повышать постепенно до 100 мг/сут. Дополнять низкими дозами ГК (5 — 10 мг). Лефлуномид эффективен при ПСА, он способен контролировать не только активность заболевания, но и течение основных синдромов — суставного и кожного. Лефлуномид тормозит темпы рентгенологического прогрессирования заболевания, снижает прирост эрозий, уменьшает индекс площади и тяжести псориаза (PASI). Инфликсимаб, алалимумаб — химерные моноклональные антитела к ФНО-a, реже дают побочные действия, более эффективны. Дозировка — 3 мг/кг веса, внутривенно медленно 1 раз через 2 и 6 нед. повторно, затем каждые 8 нед., чаще в комбинации с метотрексатом. Лечение ингибиторами ФНО может сопровождаться развитием инфекционных осложнений, в первую очередь туберкулезом.
Новый препарат — ритуксимаб — представляет собой химерные высокоаффинные моноклональные антитела к мембранному антигену В-лимфоцитов. Комбинированная терапия им с метотрексатом более эффективно тормозит деструкцию суставов. Осложнения — умеренные инфузионные реакции, умеренное нарастание частоты тяжелых инфекций, но отсутствует риск туберкулеза (Насонов Е. Л., 2008).
Глюкокортикоиды применяют при ПСА с высокой степенью активности как дополнительную терапию. Низкие дозы ГК добавляют для усиления эффекта метотрексата, других БПВП.
Введение ГКС внутрисуставно не более 3 инъекций в один сустав в течение года или в пораженные энтезы при ПСА оказывает отчетливое положительное действие. Показанием к внутрисуставному их введению является, прежде всего, активный артрит в ограниченном числе пораженных суставов. Лечение бетаметазоном проводят при наличии высокой местной активности и упорном синовите. Его целесообразно вводить и в пораженные энтезы при наличии дактилита, талалгии или энтезитов иной локализации. Топические ГКС широко применяют и для лечения ПСА. В ряде случаев без них невозможно провести эффективную терапию кожного синдрома. Хотя локальная терапия ГКС также может привести к дестабилизации ПСА и развитию распространенных его вариантов, но это происходит реже, чем при их системном применении.
Литературные данные позволяют дать высокую оценку натрия ауротиомалата, как одного из базисных препаратов в лечении ПСА (Насонов Е. Л., 2008). Ауротерапия позволяет контролировать течение этого заболевания, воздействует на симптоматику поражения периферических суставов и осевого скелета, уменьшает число рецидивов суставного синдрома, снижает клиническую и лабораторную активность заболевания. Препараты золота могут быть назначены при низкой эффективности или плохой переносимости метотрексата и сульфасалазина, отсутствии выраженных системных проявлений. Сульфасалазин является одним из стандартных препаратов в лечении ПСА. Доказана высокая терапевтическая эффективность сульфасалазина при всех ПСА. По данным Medline и Eхcerpta Medica, наиболее выраженная положительная динамика отдельных параметров патологического процесса отмечена при лечении сульфасалазином и высокими дозами метотрексата. Эффективность азатиоприна, этретината, колхицина была выше по сравнению с плацебо, но явно уступала сульфасалазину и метотрексату. Этот препарат активно воздействует на проявления периферического артрита и практически не влияет на воспалительный процесс в осевом скелете. Сульфасалазин не вызывает обострение дерматоза, а у части больных способствует разрешению псориатических эффлоресценций (Бадокин В. В. [и др.], 2001).
НПВП используют при лечении благоприятно текущих форм ПСА, преимущественно суставных, с минимальной активностью. Иногда под влиянием традиционных НПВП возможно обострение кожного ПСА, что связано с их влиянием на продукцию лейкотриенов. У пациентов с тяжелым течением следует начинать с комбинированной терапии (метотрексат вместе с циклоспорином, или метотрексат с лефлуномидом, или метотрексат с инфликсимабом, или метотрексат с салазопиридазином).
При умеренной активности ПСА следует начинать с монотерапии, в последующем переходя на комбинированную терапию при неэффективности лечения. Наиболее перспективна комбинация метатрексата с инфликсимабом или ритуксимабом (Насонов Е. Л., 2008). Способствуют уменьшению отечности суставов, их скованности антигистаминные препараты (димедрол, дипразин, тавегил).
При осложнении длительно текущего ПСА амилоидозом, помимо активной терапии для лечения, можно, как и при РА, использовать ДМСО. Начинают с приема внутрь 1 г/сут (100 мл 1 % раствора ДМСО в 3 приема после еды). Через 1–2 нед. суточную дозу при хорошей переносимости целесообразно увеличить на 1 г и постепенно довести до 3–5 г/сут. То есть больной принимает в день 100 мл 3–5 % раствора. Для улучшения вкуса ДМСО разводят фруктовым соком или добавляют мяту. Применение особенно эффективно в начальной стадии амилоидоза.
При ПСА, особенно в пожилом возрасте, необходимо использовать арсенал фитотерапии (см. гл. 4 «Ревматоидный артрит»).
При ПСА нередко необходимы лекарства, направленные на нормализацию обмена веществ и восстановление функции пораженных органов и систем организма. Например, назначение аллопуринола при развитии вторичной подагры у больных с генерализованным поражением кожи, коррекция гипергликемии или гиперлипидемии, которые при ПСА встречаются существенно чаще, чем в популяции, антиаритмических препаратов, гепатопротекторов, коррекция гипопротеинемии, отеков или азотвыделительной функции при вторичном реактивном амилоидозе и т. д. Терапевтическая тактика при распространенном вульгарном или экссудативном ПСА (и тем более пустулезном и эритродермическом) предполагает применение активной наружной терапии с использованием индифферентных мазей, препаратов цинка, кортикостероидных мазей, дериватов витамина D, ароматических ретиноидов, десенсибилизирующих средств. В зимний период необходимо использование УФО. Обязательно применение антиоксидантов, витаминов группы А, В1, В6, В12.
Физиотерапия включает магнитотерапию, транскутанную лазеротерапию, электро— и фонофарез 50 % раствора димексида. Необходима лечебная физкультура. Хирургическое лечение — эндопротезирование суставов.
Пример наблюдения.
Больная, 54 лет. С 2006 г. является инвалидом III группы с ОСТ 1-й степени с причиной инвалидности «Общее заболевание». Проф. маршрут — выжигальщица, официантка, повар. Не работает с 2004 г.
Анамнез: больная около 25 лет (с 1982 г.) страдает псориазом с регулярными обострениями заболевания, сопровождающимися множественными псориатическими элементами на коже туловища и конечностей. С 1987 г. — бронхиальная астма. Около 10 лет применяла глюкокортикоиды перорально и ингаляционно. В 2000 г. (через 18 лет после дебюта псориаза) остро возникли боли и отечность суставов обеих кистей с последующим развитием деформации суставов кистей. В 2002 г. отмечает появление болей в стопах с затруднением ходьбы. В 2004 г. впервые выявлен сахарный диабет 2-го типа, с 2003 г. на инсулинотерапии.
Объективно: распространенные псориатические элементы на коже конечностей, туловища. Выраженные деформации дистальных фаланг с подвывихами в тыльную сторону, атрофия межостных мышц. Кожа кистей отечна, истончена. Подвывихи пястно-фаланговых суставов кнаружи. Затруднена функция схвата, удержания предметов. Фокусы псориаза в области проксимальных межфаланговых суставов. Суставы III, IV и V пальцев стоп отечны, подвывихи в плюснефаланговых суставах кнаружи. Объективно — диффузный цианоз, цианоз губ, экспираторная одышка. Одышка при разговоре. Грудная клетка эмфизематозна, перкуторно коробочный звук. Дыхание жесткое с удлиненным выдохом, рассеянные сухие хрипы, шум трения плевры.
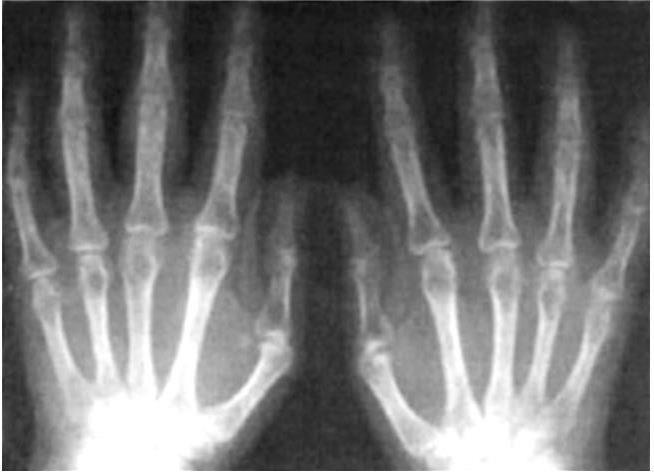
Рис. 21
На фоне остеопороза видны малозаметные кистовидные изменения диафизов в фалангах средних и основных, в основаниях пястных костей, остеолиз дистальных фаланг I пальцев обеих кистей, V пальца правой кисти и II пальца левой кисти, подвывих всех концевых фаланг в тыльную сторону. Межфаланговые суставные щели сужены. На этом фоне единичные островки склероза, преимущественно в области средних фаланг.
Выраженные лабораторные признаки воспаления — лейкоцитоз 8,3 — 10,5 ? ? 109/л, повышение СОЭ 37–43 мм/ч, СРБ 2+, повышение уровня фибриногена до 15,44 мкмоль/л. Сахар крови натощак — 8,9; 5,5 ммоль/л, постпрандиальная гликемия — 13 ммоль/л. В моче — белок 0,014 — 0,040 г/л.
УЗИ органов брюшной полости и почек: Гепатомегалия. Гепатоз. ЖКБ. Хронический калькулезный холецистит. Диффузные изменения в почках. Микролиты обеих почек. Правосторонний нефроптоз.
Рентгенологически — остеолиз концевых фаланг кистей и стоп, подвывихи фаланг пальцев кистей и стоп (см. рис. 21, 22).
Диагноз: Псориаз. Псориатический артрит, активность 3-й степени. Остеопороз, остеолиз концевых фаланг кистей и стоп, подвывихи всех концевых фаланг кистей в тыльную сторону, подвывихи пальцев стоп кнаружи. Атрофия межостных мышц обеих кистей. Спондилоартрит. Деформирующий артроз межфаланговых суставов кистей, лучезапястных, локтевых, плечевых, коленных, голеностопных суставов. Выраженное нарушение функции кистей (схвата и удержания предметов).
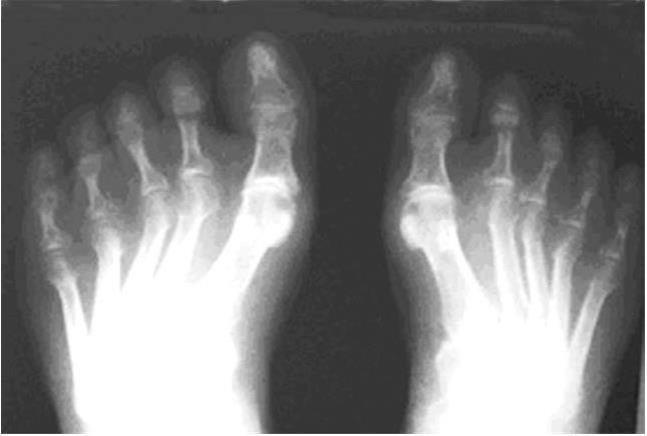
Рис. 22
Поперечная распластанность стоп. Кости порозны, суставные головки фаланг, плюсневых костей с кистовидными разряжениями, остеолиз дистальных фаланг IV и V пальцев обеих стоп, подвывихи III, IV и V пальцев стоп кнаружи. В I плюснефаланговых суставах округлые очаги деструкции костной ткани — симптом «пробойника» — вторичная подагра
НФС 2-й степени. Нарушение статодинамической функции 2-й степени.
Бронхиальная астма (атопическая, физического усилия), гормонозависимая, средней степени тяжести. Хронический обструктивный бронхит вне обострения.
Плевропневмосклероз. ДН 2-й степени.
Сахарный диабет 2-го типа, инсулинопотребный, субкомпенсированный. Диабетическая нефропатия в стадии стойкой протеинурии. ХПН I стадии. Диабетическая полинейропатия верхних и нижних конечностей, чувствительная форма, с выраженным стойким болевым синдромом, преимущественно в нижних конечностях, с умеренными вегетососудистыми и трофическими нарушениями. Диабетическая ангиопатия нижних конечностей, хроническая артериальная недостаточность 1-й степени.
Артериальная гипертензия 2-й степени. Миокардиодистрофия. ХСН I стадии, IIФК.
Ожирение 2-й степени. Гепатоз. ЖКБ. Хронический калькулезный холецистит.
Киста селезенки. Варикозное расширение вен нижних конечностей.
Заключение: Клинико-рентгенологические признаки псориатического артрита проявляются с преимущественным поражением суставов кистей и стоп, спондилоартритом, стойким выраженным суставным болевым синдромом, выраженными анатомо-морфологическими изменениями кистей и стоп (остеопороз, остеолиз концевых фаланг, подвывихи фаланг пальцев кистей и стоп, амиотрофия межкостных мышц обеих кистей), нарушением функций схвата и удержания предметов, опорной функции, сопровождаются клинико-лабораторными признаками выраженной активности процесса — отечность и болезненность в области суставов, субфебрилитет, лейкоцитоз до 10,5 ? 109/л, повышение СОЭ до 43 мм/ч, СРБ 2+, повышение уровня фибриногена до 15,44 мкмоль/л, что требует безотлагательного стационарного лечения для подбора адекватной терапии, достижения ремиссии процесса. Следует отметить, что возможности терапии данной больной, купирование артралгического синдрома крайне затруднены в связи с сопутствующей патологией бронхолегочной системы, органов пищеварения, АГ — ограничениями для назначения БПВП.
Бронхиальная астма, осложненная эмфиземой легких, плевропневмофиброзом, сопровождается выраженным нарушением функции внешнего дыхания: по данным спирографии — значительное снижение ЖЕЛ, значительное нарушение проходимости дыхательных путей (с отрицательной пробой с бронхолитиком через 15 мин, положительной — лишь через 30 мин после ингаляции). В период обследования больной в клинике отмечено ухудшение в течении бронхиальной астмы: учащение приступов удушья (без эффекта от ингаляционных бронхолитиков), в связи с чем больную наблюдали дежурные врачи клиники, проводили повторную инфузионную терапию с глюкокортикоидами, бронхолитиками.
Прогностически неблагоприятным является присоединение сахарного диабета 2-го типа, потребовавшего назначения инсулинотерапии, с развитием за короткий срок (длительность заболевания 3 года) множественных осложнений — диабетической нефропатии в стадии стойкой протеинурии, диабетической полинейропатии сенсорной формы, с выраженным стойким болевым синдромом (значительно усугубляющим имеющийся артралгический синдром), с вегетососудистыми и трофическими нарушениями, в сочетании с диабетической ангиопатией нижних конечностей с хронической артериальной недостаточностью.
Таким образом, имеющийся у больной псориатический артрит со стойко выраженной активностью процесса, со стойко выраженным нарушением функций опорно-двигательного аппарата, поражением дыхательной системы, эндокринной системы, центральной и периферической нервной систем, требующих длительного комплексного лечения, приводит в настоящее время к противопоказанности и невозможности выполнения больной любых видов трудовой деятельности, в том числе надомных видов труда, что обусловливает ограничение жизнедеятельности больной в способности к трудовой деятельности 3-й степени, передвижению 1-й степени, способности к самообслуживанию 1-й степени и дает основание для установления II группы инвалидности (Приказ № 1013 Министерства здравоохранения и социального развития РФ от 23.12.2009 г.).






