Гипоксия плода
Под гипоксией плода подразумевают комплекс изменений в его организме под влиянием недостаточного снабжения кислородом тканей и органов или неадекватной утилизации ими кислорода.
Терминология.
Термин "гипоксия плода" предложен ВОЗ (1995), но он не единственный: существуют также термины "дистресс плода" (от distress – страдания) и "асфиксия" (от а – без, sphyxis – пульс), при этом подразумевают удушье, т.е. недостаток кислорода и накопление углекислого газа в организме. Из этого следует, что термин "асфиксия" условный, так как кислородная недостаточность не всегда сопровождается отсутствием сердцебиения и гиперкапнией. В настоящее время термин "асфиксия" исполь-зуется для характеристики состояния новорожденных, родившихся с явлениями кислородной недостаточности.
В различные периоды беременности кислородная недостаточность имеет неодинаковые последствия для эмбриона и плода. В период органогенеза выраженная гипоксия может сопровождаться замедлением развития эмбриона и появлением аномалий развития. Кислородное голодание в период фетогенеза может привести к гипоксии, задержке роста плода, поражению ЦНС плода и новорожденного, нарушению процессов адаптации в постнатальном периоде, послужить причиной мертворожденна и гибели новорожденных в ранний неонатальный период.
Гипоксия плода отмечается в 10,5 % случаев (от общего числа родов), и этот показатель не имеет тенденции к снижению.
Гипоксия плода не является первичной нозологической формой или самостоятельным заболеванием, осложняющим внутриутробное развитие плода, а возникает как следствие различных патологических процессов в системе мать – плацента – плод.
Классификация.
Гипоксию плода классифицируют по длительности течения, интенсивности и механизму развития.
В зависимости от длительности течения различают хроническую, подострую и острую гипоксию. Хроническая гипоксия плода развивается при недостаточном снабжении плода кислородом в течение длительного периода, осложненном течении беременности и в основном связана с морфофункциональными изменениями плаценты, в частности с нарушением ее кровоснабжения вследствие дегенеративных, воспалительных и других поражений. Подострая гипоксия обычно развивается за 1-2 дня до родов и характеризуется снижением адаптационных возможностей плода. Острая гипоксия, как правило, возникает в родах и реже – во время беременности. Нередко наблюдается сочетание острой и хронической гипоксии плода, что является крайне неблагоприятным прогностическим фактором для плода.
По интенсивности гипоксия может быть функциональной (легкая форма): имеют место лишь гемодинамические нарушения; метаболической: более глубокая гипоксия с нарушениями всех видов обмена, но нарушения метаболизма обратимы; деструктивной (тяжелая форма): необратимые изменения на уровне клеток.
В зависимости от механизма развития выделяют следующие формы гипоксии:
1. артериалъно-гипоксемическую:
• гипоксическую, являющуюся следствием нарушения доставки кислорода в маточно-плацентарный кровоток,
• трансплацентарную – результат маточно-плацентарной или фетоплацентарной недостаточности и нарушения газообменной функции плаценты;
2. гемическую:
• анемическую, в том числе гемолитическую и постгеморрагическую;
• гипоксию в результате снижения сродства фетального гемоглобина к кислороду;
3. ишемическую:
• гипоксию, развивающуюся как следствие низкого сердечного выброса при аномалиях развития сердца и крупных сосудов, тяжелых нарушений сердечного ритма, сниженной сократимости миокарда;
• гипоксию в результате повышенного сосудистого сопротивления, в том числе из-за изменения реологических свойств крови;
4. смешанную, для которой характерно сочетание двух и более патогенетических форм кислородной недостаточности у плода.
Наиболее часто наблюда-ются артериально-гипоксемическая и смешанная формы гипоксии.
Даже при неосложненной беременности снабжение плода кислородом значительно хуже, чем взрослого человека. Однако на всех этапах развития благодаря наличию компенсаторно-приспособительных механизмов кислородное снабжение находится в полном соответствии с потребностями плода.
Устойчивость плода к гипоксии определяется следующими физиологическими особенностями его внутриутробного развития: большим минутным ^бъемом сердца, достигающим 198 мл/кг (у новорожденного 85 мл/кг, у Рослого человека 70 мл/кг); увеличением частоты сердечных сокращений до 150-160 уд/мин; значительной кислородной емкостью крови плода (в среднем 23 %) ; наличием фетального гемоглобина, составляющего 70 % от общего количества гемоглобина в эритроцитах; особенностями строения сердечно-сосудистой системы – наличием трех артериовенозных шунтов (венозный, или аранциев, проток, межпредсердное овальное отверстие и артериальный, или боталлов, проток), за счет которых почти все органы плода получают смешанную кровь (смешение различных потоков крови в желудочках сердца плода обеспечивает более медленное в случае развития гипоксии снижение Рс , чем у взрослого); большим удельным весом анаэробиоза в энергетике плода, который обеспечивается значительными запасами гликогена, энергетических и пластических продуктов обмена в жизненно важных органах. Развивающийся при этом у плода метаболический апидоз повышает его устойчивость к кислородному голоданию (табл. 16.1).
Этиология и патогенез.
Многочисленные этиологические факторы, способствующие развитию гипоксии плода, можно разделить на 3 группы. К 1-й группе относятся экстрагенитальные заболевания матери (сердечно-сосудистые, бронхолегочные и т.д.), синдром сдавления нижней полой вены, анемия, отравления, интоксикации, кровопотеря, шок различной этиологии, а также осложнения беременности и родов, при которых отмечается недостаток кислорода или избыток углекислого газа в организме матери. Наиболее обширную 2-ю группу составляют нарушения плодовоплаценгарного кровотока (гестоз, перенашивание беременности, угрожающие преждевременные роды, аномалии расположения плаценты, преждевременная отслойка нормально расположенной плаценты, инфаркты плаценты, аномалии родовой деятельности, патология пуповины: обвитие вокруг шеи и туловища, выпадение и натяжение). В 3-ю группу включены заболевания плода: гемолитическая болезнь, анемия, гипотензия, инфицирование, врожденные пороки развития, длительное сдавление головки во время родов.
Кислородная недостаточность является основным патогенетическим фактором, приводящим к нарушениям функций организма, обменных процессов и в конечном итоге – к возникновению терминального состояния.
Уменьшение насыщения крови кислородом обусловливает существенные изменения дыхательной функции крови и развитие ацидоза. В этих условиях изменяются многие параметры гомеостаза, направленность которых зависит от степени тяжести гипоксии. На ранних этапах как проявление компенсаторных реакций организма происходит активация функций большинства систем, В дальнейшем наступает их угнетение, и в конечном итоге кислородная недостаточность вызывает деструктивные процессы в жизненно важных органах. Наиболее значительными считаются изменения макрои микрогемодинамики, метаболизма.
В начальных стадиях гипоксии плода наблюдается универсальная компенсаторно-защитная реакция, направленная на сохранение функции жизненно важных органов и систем. Под влиянием дефицита кислорода происходят активация функции мозгового и коркового слоев надпочечников, выработка большого количества катехоламинов и других вазоактивных веществ, которые вызывают тахикардию и повышение тонуса периферических сосудов в органах, не имеющих жизненно важного значения. Вследствие тахикардии, централизации и перераспределения кровотока увеличиваются минутный объем сердца, кровообращение в мозге, сердце, надпочечниках, плаценте и уменьшается – в легких, почках, кишечнике, селезенке, коже, в результате чего развивается ишемия этих органов. На фоне ишемии возможны раскрытие анального сфинктера и выход мекония в околоплодные воды.
Длительная или тяжелая гипоксия, наоборот, приводит к резкому угнетению функции надпочечников, сопровождающемуся снижением уровня кортизола и катехоламинов в крови. Угнетение гормональной регуляции сопровождается угнетением жизненно важных центров, уменьшением частоты сердечных сокращений, снижением артериального давления, венозным застоем, скоплением крови в системе воротной вены.
Одновременно с изменениями макрогемодинамики происходят выраженные нарушения в системе микроциркуляции. Расстройства микрогемодинамики при кислородной недостаточности происходят по трем направлениям: снижение тонуса резистивных сосудов, повышение проницаемости стенок сосудов, изменение агрегатного состояния крови с нарушением ее текучих свойств. Снижение тонуса артериол и прекапилляров вызывает расширение сосудов и увеличение объема сосудистого русла, что в сочетании с уменьшением минутного объема сердца приводит к замедлению кровотока вплоть до стаза. В условиях ацидоза и снижения скорости кровотока повышаются вязкость крови, агрегационная активность клеток крови и коагуляционный потенциал с развитием синдрома диссеминированного внутрисосудистого свертывания крови и сладж-синдрома со снижением газообмена в эритроцитах, уменьшением адекватного газообмена в тканях. Нарушение трофики сосудистой стенки приводит к повышению ее проницаемости и выходу первоначально жидкой части крови, а затем и форменных элементов крови из сосудистого русла. Результатом этих изменений являются гиповолемия, гемоконцентрация, отек тканей, диапедезные кровоизлияния в жизненно важные органы.
Под влиянием кислородной недостаточности происходят значительные изменения параметров метаболизма: повышается активность ферментов, Участвующих в окислительно-восстановительных процессах, что приводит к Усилению тканевого дыхания и энергообразования в печени плода. Основной компенсаторно-приспособительной реакцией организма плода, способствующей меньшему повреждению его тканей при недостатке кислорода, является усиление процессов анаэробного гликолиза. В результате этого происходят уменьшение количества гликогена и накопление кислых продуктов обмена (молочная кислота, кетоновые тела, лактат) в печени, сердце, мозге, мышцах и крови плода, что приводит к метаболическому или реслираторно-метаболическому ацидозу. Одновременно происходит активация перекисного окисления липидов с высвобождением токсичных радикалов которые наряду с недоокисленными продуктами обмена при прогрессировании гипоксии угнетают ферментативные реакции, снижают активность дыхательных ферментов, нарушают структурно-функциональные свойства клеточных мембран с повышением их проницаемости для ионов. Наиболее значительны изменения баланса ионов калия, которые выходят из клеточного пространства, и уровень их в плазме крови плода повышается. Аналогичные изменения происходят в отношении ионов магния и кальция. Клиническое значение этих нарушений велико. Гиперкалиемия наряду с гипоксией и ацидозом играет важную роль в перевозбуждении парасимпатической нервной системы и развитии брадикардии. Следствием повышенной проницаемости клеточных мембран являются энергетический голод и гибель клеток.
Вследствие выраженных изменений макрои микрогемодинамики, метаболизма в тканях жизненно важных органов могут развиваться ишемия и некрозы, приводящие к необратимым деструктивным нарушениям. Эти патологические изменения не исчезают после рождения плода, а сохраняются тем дольше, чем более тяжелую гипоксию перенес плод, определяя развитие ребенка в дальнейшем. Последствия гипоксии прежде всего про-являются в головном мозге, в котором отек и микрокровоизлияния вызывают нарушение функций центров регуляции, в первую очередь дыхательного и сердечно-сосудистого. При повышении внутричерепного давления даже при физиологических родах указанные изменения могут быть фоном для кровоизлияний, в том числе массивных, что в последующем может привести к развитию церебральных параличей.
Клиническая картина и диагностика.
Клинические проявления гипоксии плода во время беременности скудны. К ним относят изменения двигательной активности плода, ощущаемые беременной. В начальной стадии внутриутробной гипоксии беременная отмечает беспокойное поведение плода, которое выражается в учащении и усилении его двигательной активности. При про фесе ирующей или длительной гипоксии происходит ослабление движений плода, вплоть до их прекращения. Уменьшение числа движений плода до 3 в течение 1 ч и менее является признаком внутриутробного страдания плода и служит показанием к проведению срочного дополнительного исследования.
Диагностика гипоксии плода во время беременности состоит в непосредственной оценке его состояния и анализе результатов применения косвенных методов, позволяющих определить функциональное состояние фето плацентарной системы (кард иото ко граф ия, эхография, допплерометрия кровотока в системе мать-плацента-плод, определение биофизического профиля плода, РО2 и РСО2 , уровня лактата и показателей КОС в крови матери, околоплодных водах и крови плода, уровня хорионического гонадотропина, плацентарного лактогена, эсгриола).
Наиболее информативными и точными методами оценки состояния плода во время беременности (в последнем триместре) являются кардиомониторный контроль и ультразвуковое сканирование. К начальным признакам гипоксии плода при кардиотокографии относятся тахикардия (до 170 уд/MHHj или умеренная брадикардия (до 100 уд/мин), понижение вариабельности сердечного ритма, кратковременная (до 50 % записи) монотонность ритма»
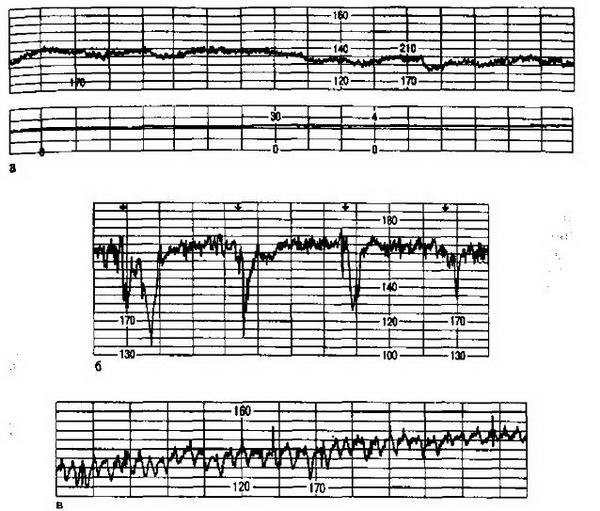
Рис. 16.3. Выраженные признаки гипоксии плода: монотонность (а), парадоксальная реакция на функциональные пробы (б), синусоидальный ритм (в).
Ослабление реакции на функциональные пробы.
Кардиограмма при этом оценивается в 5-7 баллов. При выраженном страдании плода наблюдаются значительная брадикардия (ниже 100 уд/мин) или тахикардия (более 170 уд/мин), монотонность ритма (свыше 50 % записи), парадоксальная реакция на функциональные пробы (поздние децелерации в ответ на шевеление плода при нестрессовом тесте) или ее отсутствие (рис. 16.3). О выраженной гипоксии плода свидетельствует оценка кардиотокограммы в 4 балла и менее.
Дополнительным критерием оценки состояния плода во время беременности является его биофизический профиль (БФП). При гипоксии происходит прогрессивное угнетение биофизических функций плода. Параметры БФП при гипоксии плода делят на "острые", или быстрореагирующие (нестрессовый тест, дыхательные движения, двигательная активность и Тонус плода), и "хронические" показатели длительности страдания плода, Которые возникают в результате повторяющейся или прогрессирующей гипоксии (маловодие и преждевременное созревание плаценты). В начальной стадии развития гипоксии в первую очередь осуществляют постановку неРеактивного нестрессового теста (НСТ), при котором с целью оценки степени тяжести гипоксии проводят ультразвуковое исследование и определение остальных биофизических параметров. При этом определение БФП заменяет проведение стрессового теста. Вслед за НСТ происходит снижение дыхательной активности плода вплоть до исчезновения его дыхательных движений, при прогрессирующей гипоксии исчезают движения и тонус плода Изменения биофизической активности в процессе нарастания гипоксии плода происходят в обратной последовательности от сроков созревания в эмбриои фетогенезе регулирующих центров ЦНС. Суммарная оценка БФП 6-7 баллов указывает на сомнительное состояние плода, в связи с чем требуется проведение повторного исследования, а оценка 4-5 баллов и менее свидетельствует о наличии выраженной внутриутробной гипоксии плода.
В диагностике гипоксии плода важное значение придают допплерометрической оценке кровообращения в аорте и сосудах головного мозга плода. Допплерометрия позволяет несколько раньше, чем кардиотокография, диагностировать внутриутробную гипоксию, что способствует выявлению группы беременных, подлежащих тщательному наблюдению и лечению. Гемодинамические нарушения в аорте и сосудах головного мозга плода вторичны и свидетельствуют о нарушении центральной гемодинамики плода в ответ на уменьшение плацентарной перфузии. Увеличение диастолической скорости кровотока в головном мозге плода при гипоксии указывает на сохранение церебрального кровотока плода в этих условиях за счет вазодилатацци. Компенсаторный механизм поддержания нормального кровоснабжения головного мозга при сниженной плацентарной перфузии носит название "охранный круг кровообращения". Существует коррелятивная связь между средней скоростью кровотока в аорте и средней мозговой артерии плода, рН, Рс0 и Ро в его крови. При тяжелой гипоксии уменьшение ПИ в средней мозговой артерии достигает максимума, что отражает максимальную дилатацию этого сосуда. Крайне неблагоприятный прогностический признак для плода – появление нулевых или отрицательных значений диастолического компонента кровотока в аорте, что свидетельствует о декомпенсации фетоплацентарной системы. Как правило, эти изменения сочетаются с патологическим кровотоком в артерии пуповины, однако показатели пуповинного кровотока могут быть и нормальными. В более поздних стадиях по мере прогрессирования гипоксии возникают нарушения венозного кровотока (венозный проток, печеночные вены).
С целью диагностики кислородной недостаточности у плода проводят осмотр и биохимическое исследование околоплодных вод. В случае гипоксии плода при амниоскопии обнаруживают окрашивание околоплодных вод меконием. Наиболее информативными тестами при исследовании околоплодных вод, получаемых при амниоцентезе, являются рН ниже 7,02; Рсо2 выше 55 мм рт.ст., Р°Л ниже 80 мм рт.ст., концентрация калия выше 6,5 ммоль/л. О кислородной недостаточности плода, кроме того, свидетельствуют повышение активности щелочной фосфатазы в околоплодных водах более чем в 2 раза. Определение концентрации плацентарных гормонов в сыворотке крови и моче беременных позволяет диагностировать плацентарную недостаточность, приводящую к гипоксии плода. Уровень плацентарного лактогена в сыворотке крови беременных при гипоксии плода снижается в 3 раза (норма 10 мкг/мл). Из фракций эстрогенов наиболее информативен показатель экскреции эстриола: экскреция гормона менее 12 мг/сут (в околоплодных водах менее 50 мг/100 мл) свидетельствует о плацентарной недостаточности. Заслуживает внимания используемый в настоящее время новый метод диагностики гипоксии плода на основании результатов изучения различных параметров его крови (КОС, уровень гемоглобина и др.), полученной с помощью кордоцентеза.
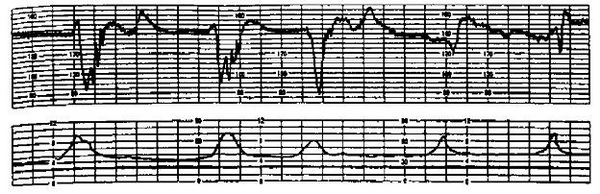
Рис. 16.4. Признаки гипоксии плода в родах (Vи W-образные децелерации).
Диагностика гипоксии плода в родах основывается на выявлении нарушений его сердечной деятельности. Помимо аускультации, наиболее доступным методом выявления гипоксии плода в родах является кардиотокография (рис. 16.4). При кардиомониторном наблюдении к начальным признакам гипоксии плода в первом периоде родов относятся брадикардия до 100 уд/мин как при головном, так и тазовом предлежании плода, периодическая монотонность сердечного ритма. Реакция на схватку проявляется кратковременными поздними децелерациями до 70 уд/мин. Во втором периоде родов начальными признаками гипоксии служат браликардия до 90 уд/мин или тахикардия до 200 уд/мин, регистрируется периодическая монотонность ритма. В ответ на потугу возникают поздние децелерации до 60 уд/мин. К выраженным признакам гипоксии плода в первом периоде родов относятся брадикардия до 80 уд/мин при головном предлежании, брадикардия ниже 80 уд/мин или тахикардия до 200 уд/мин при тазовом предлежании плода. Независимо от предлежания плода регистрируются стойкая монотонность ритма и аритмия. Реакциями на схватку являются возникновение длительных поздних W-образных децелерации при головном предлежании и комбинация акцелераций с децелерациями до 80 уд/мин при тазовом предлежании плода.
В периоде изгнания к выраженным признакам гипоксии относится появление на кард иото ко грамме выраженной брадикардии до 80 уд/мин или т11ахикардии более 190 уд/мин; регистрируется стойкая монотонность ритма аритмия, в ответ на потугу отмечаются длительные поздние децелерации До 50 уд/мин как при головном, так и тазовом предлежании плода. При головном предлежании вне схватки регистрируются W-образные децелерации до 50 уд/мин.
В процессе родов в отличие от антенатального периода прогностически неблагоприятным фактором в отношении гипоксии следует расценивать Появление дыхательной или двигательной активности плода. Регулярная Ыраженная дыхательная активность плода как в первом, так и во втором Периодах родов представляет собой большую угрозу для новорожденного, являясь причиной развития у него аспирационного синдрома.
Большое значение в выявлении гипоксии плода имеет исследование КОС крови, полученной из предлежащей части. В первом периоде родов рН ниже 7,2 свидетельствует о гипоксии, а от 7,20 до 7,24 – о преацидозе в связи с чем требуется повторное исследование. Нижняя граница нормы рН во втором периоде родов 7,14.
Выделение мекония в процессе родов не столько характеризует состояние плода, сколько заставляет обратить внимание на угрожающую ситуацию и имеет значение лишь при головном предлежании. В зависимости от длительности и глубины гипоксии примесь мекония в водах имеет разный характер: от взвешенных кусочков в начальной стадии гипоксии до образования грязной эмульсии при тяжелой гипоксии. Наличие мекония в околоплодных водах может указывать не только на острую, но и кратковременную или длительную гипоксию плода, возникшую до родов, и плод в отсутствие новых эпизодов гипоксии может родиться без асфиксии.
Лечение, Во время беременности лечение хронической гипоксии плода должно быть комплексным. Кроме лечения основного заболевания, беременной необходимо проводить терапию, направленную на нормализацию плацентарного кровообращения, улучшение снабжения плода кислородом и энергетическими веществами, повышение адаптационных возможностей в системе мать-плод и устойчивости плода к гипоксии, создание условий, благоприятствующих течению обменных процессов. Для решения этих задач в первую очередь следует воздействовать на кислородотранспортную функцию плаценты путем:
1. расширения маточно-плацентарных сосудов;
2. расслабления мускулатуры матки;
3. нормализации реокоагуляционных свойств крови;
4. активации метаболизма миометрия и плаценты.
Прежде всего беременным необходимо обеспечить покой. Постельный режим, при котором улучшается кровоснабжение матки, показан при выявлении гипоксии плода и отставании его в развитии, особенно при недоношенной беременности.
Снабжение организма матери кислородом улучшается в результате ингаляции его с помощью маски. При этом оптимальным вариантом является вдыхание беременной 40-60 % кислородно-воздушной смеси в количестве 4- 5 л/мин в течение 30-60 мин 1-2 раза в день. Выраженный эффект дает применение кислородного коктейля или кислородной пены. Кислородный коктейль всасывается медленно; его принимают по 150-200 мл в течение 5- 10 мин и более за 1,5 ч до или через 2 ч после еды. Для профилактики и лечения гипоксии у матери и плода при сердечно-сосудистых заболеваниях с успехом применяют гипербарическую оксигенацию.
С целью улучшения маточно-плацентарного кровообращения в состав комплексной терапии включают эстрогены, которые влияют на обменные процессы в эндометрии, повышают проницаемость плаценты, увеличивают переход глюкозы и питательных веществ к плоду. Одним из препаратов, оказывающих слабое эстрогенное действие и улучшающих маточно-плацентарный кровоток, является сигетин, который вводят в виде 1-2 % раствора по 2-4 мл в 20 мл 40 % раствора глюкозы. Его целесообразно применять на фоне введения сосудорасширяющих средств (2,4 % раствор эуфиллина внутривенно струйно или капельно в дозе 5-10 мл, компламин по 0,15 г 3 раза в день во время еды или по 2 мл 15 % раствора 1-2 раза в день, курантил по 0,5 мл/кг внутривенно капельно в течение 2-5 ч или перорально по 0,025 г 2-3 раза в день после инфузии).
Для нормализации маточно-плацентарного кровотока и активации метаболизма в плаценте применяют токолитики (р-адреномиметики) нового поколения – бриканил, гинипрал в виде внутривенных инфузии (на растворе глюкозы) по 0,5 мг, длительно.
С целью нормализации реокоагуляционных свойств крови используют дезагреганты (трентал, низко молекулярные декстраны) и антикоагулянты (гепарин по 20.000 ЕД/сут в виде подкожных инъекций или внутривенных инфузии).
К препаратам, влияющим непосредственно на метаболические процессы, относятся АТФ, кокарбоксилаза, фолиевая кислота, концентрированные растворы глюкозы, метионин, ударные дозы витамина В12, галаскорбин.
При лечении хронической гипоксии плода обязательно применяют мембраностабилизаторы (эссенциале-форте или липостабил по 2 капсулы 3 раза в день либо внутривенно по 5 мл) и антиоксиданты (витамин Е по 600 мг/сут, аскорбиновая кислота по 600 мг/сут, глутаминовая кислота по 0,3 г/сут).
Коррекцию баланса кислот и щелочей у беременных следует проводить под контролем параметров КОС крови, поскольку патологические состояния у них не всегда сопровождаются ацидозом. Лечение ацидоза должно быть направлено на коррекцию баланса кислот, щелочей и улучшение периферической циркуляции. Введение таких лекарственных препаратов, как глюкоза, витамин С, кокарбоксилаза, АТФ, приводит к нормализации КОС крови, поэтому проведение инфузионной терапии само по себе кор-ригирует нарушения кислотно-основного обмена, а иногда может наблюдаться тенденция к алкалозу.
Хороший эффект дают вещества, повышающие устойчивость ткани мозга к недостатку кислорода (седуксен, оксибутират натрия). Наряду с улучшением энергетического обеспечения мозга они обеспечивают снижение потребления кислорода ЦНС без существенного подавления функций ее жизненно важных центров. В условиях гипоксии выраженное защитное действие ГОМК оказывает также на клетки миокарда, печени, почек.
Особенно важны терапия и подготовка к родоразрешению при преждевременных родах, когда гипоксия плода усугубляется незрелостью легочной ткани. Для ускорения созревания легочной ткани показаны глюкокортикоиды: дексаметазон 4 раза в день в течение 2-3 сут, разовая доза 2 мг, суточная – 8 мг, курсовая – 16-24 мг.
При отсутствии эффекта от комплексной терапии хронической гипоксии плода при сроках гестации 28-32 нед и более выраженные изменения кардиото ко граммы и биофизического профиля плода, обнаружение мекония а околоплодных водах, маловодие, острая гипоксия плода являются показаниями к экстренному родоразрешению независимо от срока гестации. При этом предпочтение следует отдавать кесареву сечению.
В родах терапию изменяют в зависимости от акушерской ситуации, выбирая быстродействующие эффективные препараты (глюкоза, увлажненный кислород, эуфиллин, кокарбоксилаза, сигетин, аскорбиновая кислота), введение которых предшествует оперативному родоразрешению (кесарево сечение, акушерские щипцы, извлечение плода за тазовый конец, вакуумэкстракция, перинеоили эпизиотомия).
Профилактика гипоксии плода и асфиксии новорожденного должна основываться на ранней дородовой диагностике и состоять из следующих компонентов:
1. своевременной госпитализации беременной из группы риска развития гипоксии плода;
2. проведения интенсивной терапии акушерской и экстрагенитальной патологии беременных;
3. выбора адекватных методов родоразрешения;
4. комплексной терапии гипоксии плода, включающей коррекцию расстройств гемодинамики, микроциркуляции, нарушений метаболизма функции фетоплацентарного комплекса;
5. досрочного родоразрешения при отсутствии эффекта от проводимой терапии.
В процессе родов лечение и профилактика гипоксии плода, асфиксии новорожденного обязательны в следующих случаях:
1. слабость родовой деятельности и длительный безводный промежуток при несвоевременном излитии вод;
2. перенашивание беременности;
3. гестозы (длительно текущие или тяжелые формы);
4. тазовое предлежание плода;
5. изосерологическая несовместимость крови матери и плода;
6. сахарный диабет, сердечно-сосудистые заболевания и другие состояния, влияющие на плод.


![Дочки-матери [Все, о чем вам не рассказывала ваша мама и чему стоит научить свою дочь]](https://img-lib.med-tutorial.ru/3386939452/cover.jpg)



